Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Portuguesa de Imunoalergologia
versión impresa ISSN 0871-9721
Rev Port Imunoalergologia vol.22 no.1 Lisboa mar. 2014
ARTIGO ORIGINAL
A anafilaxia em Portugal: Primeiros registos do Catálogo Português de Alergias e outras Reacções Adversas
Anaphylaxis in Portugal: First registries of the Portuguese Catalog of Allergies and Other Adverse Reactions
Rita Amaral1, Mário Morais-Almeida1,2, Ângela Gaspar2, Ana Sa‑Sousa1, Henrique Martins3, João Fonseca1,4,5
1 CINTESIS – Centro de Investigação em Tecnologias e Sistemas de Informação em Saúde, Faculdade de Medicina da Universidade do Porto
2 Centro de Imunoalergologia, Hospital CUF Descobertas, Lisboa
3 Serviços Partilhados do Ministério da Saúde
4 Serviço de Imunoalergologia, Centro Hospitalar São João, Porto
5 Unidade de Imunoalergologia, Instituto e Hospital CUF, Porto
RESUMO Introdução: A anafilaxia é usualmente sub-diagnosticada e sub-notificada, estando em causa a segurança do utente nos cuidados de saúde. O Catálogo Português de Alergias e outras Reacções Adversas (CPARA) foi desenvolvido para registar e partilhar informação destas reacções em todo o sistema de saúde português. Objectivo: Caracterizar clínica e demograficamente todos os casos de reacções de anafilaxia notificados no CPARA durante os primeiros 10 meses da sua implementação. Métodos: Foram analisados todos os registos (n = 20 389) introduzidos no CPARA desde Julho 2012 a Maio 2013, seleccionando os registos notificados como Anafilaxia. Foram analisados separadamente os grupos de doentes em idade pediátrica (< 18 anos) e adulta (≥ 18 anos). Resultados: Foram notificados 1209 casos de anafilaxia relativos a 1045 utentes, com ratio médio de registos de 11,2 por 100 000 habitantes em cada região continental de Portugal. A idade média (± desvio‑padrao) foi de 51,8 (±20,2) anos, sendo 71% do género feminino. Os principais alergénios relacionados com anafilaxia foram: medicamentos (83%), alimentos (7%) e venenos de insectos (3%). Nos 77 utentes (7%) com idade < 18 anos, a principal causa foi alimentar (43%; p<0,001), principalmente do grupo leite e lacticínios (24%). Nos adultos, foi maioritariamente provocada por medicamentos (87%; p<0,001), com os antibióticos beta‑lactamicos (46%) como causa principal. Dentro de cada grupo etário, os alergénios mais frequentes foram significativamente diferentes entre os géneros. Conclusões: O CPARA é uma ferramenta de elevado potencial na monitorização e conhecimento da anafilaxia em Portugal. Os alergénios mais frequentes em reacções de anafilaxia diferem consoante o grupo etário e o género, conforme descrito em outros tipos de estudos.
Palavras-chave: Anafilaxia, alergénios, alergia a fármacos, registo de reacções adversas.
ABSTRACT
Introduction: Anaphylaxis is usually under-diagnosed and under-reported involving the safety of the patient in health care. The Portuguese Catalog of Allergies and other Adverse Reactions (CPARA) was developed to track and share information from these reactions, across the Portuguese health system. Aim: To characterize clinical and demographically all cases of anaphylaxis reactions, inserted in CPARA, during the first 10 months of its implementation. Methods: We analyzed all records (n = 20389) inserted in CPARA from July 2012 to May 2013, selecting all records reported as Anaphylaxis. We analyzed separately the groups of pediatric (< 18 years) and adult (≥ 18 years) patients. Results: There were 1209 reported cases of anaphylaxis related to 1045 users, with a mean ratio of 11.2 records per 100000 inhabitants, in each Portuguese continental region. The mean age (± standard deviation) was 51.8 (±20.2) years and 71% were female. The major allergen in anaphylaxis reactions were drugs (83%), food (7%) and insect venom (3%). In 77 patients (7%) with age <18 years, the main cause of anaphylaxis reaction was food (43%; p<0.001), most of them due to milk and dairy products (24%). In adults, it was mostly induced by drugs (87%, p<0.001), particularly with beta‑lactam antibiotics (46%). Within each age group, the most frequent allergens were significantly different between sexes. Conclusions: CPARA is an essential tool of great potential in monitoring and understanding the reactions of anaphylaxis in Portugal. The most common allergens in anaphylaxis reactions differ depending on the age group and sex as previously described in other types of studies.
Keywords: Adverse reaction report, allergens, anaphylaxis, drug allergy.
INTRODUÇÃO
A anafilaxia é uma reacção de hipersensibilidade aguda, sistémica e grave, com início rápido e potencialmente fatal1,2. É usualmente sub-diagnosticada devido aos múltiplos factores de risco e doenças concomitantes associadas, conduzindo a um sub‑reconhecimento por parte dos doentes e, igualmente, dos seus prestadores de cuidados de saúde3,4.Os critérios para definição de anafilaxia foram inicialmente publicados pela American Academy of Allergy, Asthma and Immunology2, sendo posteriormente recomendados pela World Allergy Organization4, permitindo globalizar a sua abordagem e tratamento, assim como a comparação de estudos que estimam a incidência e prevalência desta reacção em diferentes países5-9.
A prevalência de anafilaxia durante a vida será de 0,05 a 2%8, sendo estimado que, no Reino Unido, uma em cada 1333 pessoas sofreram um episódio, durante a sua vida10.
A incidência de anafilaxia será de 4 a 50 por 100 000 indivíduos/ano na população em geral3,11-13, com uma mortalidade de 1 a 3 casos por milhão de habitantes/ano14.
Em Portugal, foi encontrada uma prevalência de anafilaxia de 1,34% em ambulatório de Imunoalergologia15, em que as causas mais frequentes na população estudada foram os alimentos (59%), os fármacos (17%) e o látex (13%).
Na literatura, os alergénios mais frequentemente descritos como causa das reacções de anafilaxia são: os alimentos, os fármacos e os venenos de insectos2,7,8,11,15-17, sendo que o primeiro grupo tem sido demonstrado como a causa mais frequente dos episódios na infância e na adolescência15,18-21, estando os restantes grupos mais associados à idade adulta7,22.
Apesar das reacções de anafilaxia ocorrerem em todos os grupos etários, tem sido observado que a distribuição do género difere consoante idade pediátrica, mais frequente no género masculino19-21, em comparação com idade adulta, em que é mais frequente no género feminino7,22,23.
A expressão to avoid is to identify utilizada pelos autores Makinen-Kiljunen e Haahtela23 evidencia a importância da identificação imediata e do conhecimento prévio de episódios alérgicos na evicção do potencial alergénio. Assim como o acesso facilitado e partilhado é necessário para o conhecimento epidemiológico da anafilaxia, que muitas vezes é erradamente percepcionada como sendo uma doença rara1.
Visto que a potencial falha no registo e na partilha da informação sobre alergias e reacções adversas comporta um risco grave para a segurança dos utentes dos serviços de saúde, cada vez mais surgem estudos sobre análise dos registos de reacções de anafilaxia. No entanto, a maioria é baseada em entrevistas telefónicas ou questionários sobre um alergénio específico e o seu registo é feito de forma voluntária7,16,23,24.
Recentemente, foi proposto um registo pan-europeu sobre as reacções alérgicas graves para permitir aumentar o conhecimento sobre a anafilaxia25. A Sociedade Portuguesa de Alergologia e Imunologia Clínica (SPAIC) tem vindo a promover junto dos seus sócios a notificação voluntária, anónima, dos casos de anafilaxia observados (www.spaic.pt), o qual já permitiu a caracterização de cerca de setecentos doentes com clínica grave de anafilaxia, em que as causas mais frequentes identificadas foram os fármacos, os alimentos, os venenos de insectos e o látex (dados não publicados).No âmbito das actividades da Sociedade Latino‑Americana de Asma, Alergia e Imunologia, Portugal está ainda integrado no inquérito OLASA (Online Latin American Survey of Anaphylaxis) que recolhe informações sobre as manifestações clínicas, desencadeantes e tratamentos destas reacções em doentes seguidos por Alergologistas de 15 países latino-americanos e Portugal7.
No intuito de ultrapassar a ausência ou insuficiente informação clínica de cada doente em Portugal, foi desenvolvida o Resumo Clínico Único do Utente (RCU2), baseado no projecto epSOS (European Patient Smart Open Service) (www.epsos.eu) e acessível no Portal do Utente, inserido na Plataforma de Dados da Saúde (PDS-PU).
O RCU2 permite a partilha dos dados clínicos essenciais à prestação de cuidados de saúde, nomeadamente alergias, medicação, diagnósticos, cirurgias e vacinações, sempre que exista a necessidade de um atendimento urgente, ou programado, numa entidade de saúde nacional (disponibilizada no Portal do Profissional – PDS-PP) ou estrangeira (Portal Internacional – PDS-epSOS).
As informações podem ser adicionadas pelo profissional de saúde e pelo próprio utente, requerendo validação clínica posterior.
Integrado na Plataforma de Dados da Saúde, a Comissão para a Informatização Clínica de Portugal propôs e implementou, em 2012, o Catálogo Português de Alergias e outras Reacções Adversas (CPARA), elaborado em conjunto pelos Serviços Partilhados do Ministério da Saúde e pela SPAIC, que permite aos profissionais de saúde registarem qualquer episódio de alergia ou outra reacção adversa observada ou prévia. A publicação das Normas n.º 002/2012, n.º 004/2012 e n.º 014/2012 da Direccao-Geral de Saúde (DGS)26-28, tornou obrigatório o registo dos quadros de anafilaxia observados e prévios, independentemente do grupo etário do doente ou da identificação do agente causal, com uma estrutura de registo comum para todas as aplicações informáticas no sector da saúde, quer do sector público, quer do sector privado.
Visto que este catálogo está assente no RCU2, a sua finalidade é recolher e permitir a partilha de informações sobre as reacções alérgicas / adversas em Portugal. Como referido, esta informação está já acessível em território nacional e, futuramente, a nível internacional.
Com base nestes pressupostos, este estudo teve como objectivo caracterizar clínica e demograficamente todos os casos de reacções de anafilaxia inseridos no CPARA durante os primeiros 10 meses da sua implementação.
MÉTODOS
Participantes
A população-alvo foi a população portuguesa, em geral, que refere ou referiu alergias ou outras reacções adversas, tendo sido documentadas no CPARA numa consulta, internamento, emergência ou noutros episódios de prestação de cuidados de saúde. Foram analisados todos os registos inseridos por profissionais de saúde, desde a sua implementação ( Julho 2012) até Maio 2013. Foram incluídos no estudo somente os registos notificados como Anafilaxia, na variável Tipo de reacção.
CPARA
Para a recolha de dados foi utilizado o CPARA, publicado e implementado em Portugal de acordo com a Norma 002/2012 de 04/07/2012 da DGS28.
Os registos têm tipologia definida e referem episódios de alergias ou outras reacções adversas documentados, por profissionais de saúde, numa consulta, internamento, emergência ou noutros episódios de cuidados de saúde.
Cada registo contém a informação dos elementos identificativos da alergia / intolerância, de preenchimento obrigatório:
– Origem da informação (provém do médico, do imunoalergologista, de outros profissionais de saúde ou do próprio utente);
– Data da reacção;
– Categoria da reacção adversa (identifica se a reacção está relacionada com fármacos, alimentos ou outra substância / agente);
– Alergénio (identifica o alergénio / agente contra o qual a pessoa desenvolveu uma reacção adversa);
– Tipo de reacção;
– Gravidade;
– Estado (quando existe confirmação de uma determinada reacção alérgica, indicar se se confirma o estado do registo como activo/inactivo).
Os grupos de alergénios são identificados de acordo com o tipo de reacção adversa, i.e., quando são alergénios medicamentosos, é utilizada a codificação Anatomical Therapeutic Chemical Code (www.whocc.no); quando são alergénios alimentares e/ou outras substâncias / agentes é utilizada a codificação descrita no CPARA28.
O ratio de registo por 100 000 habitantes em cada região foi calculado a partir da população residente em cada região de Portugal continental, em 2012, dividida segundo a Nomenclatura de Unidades Territoriais para fins Estatísticos II (NUTSII) 29.
ANÁLISE ESTATÍSTICA
Foram analisados separadamente os grupos de indivíduos em idade pediátrica (< 18 anos) e adulta (≥ 18 anos). Foi garantida a confidencialidade dos dados pela atribuição de um número aleatório a cada utente. As variáveis foram analisadas utilizando métodos de estatística descritiva: frequência absoluta e relativa para as variáveis qualitativas e média, desvio-padrao (DP) para as variáveis quantitativas. Para comparação dos grupos etários foi utilizado o teste t-student para amostras independentes, na variável idade e o teste de qui-quadrado ou teste exacto de Fisher, nas variáveis categóricas. A análise estatística foi realizada utilizando IBM SPSS Statistics v. 20 (Chicago, Estados Unidos da América) sendo considerado estatisticamente significativo um valor p <0,05.
RESULTADOS
Caracterização geral dos registos do CPARA
Após 10 meses de funcionamento, no CPARA foram registados 20 389 casos de alergias ou outras reacções adversas, correspondendo a 16 253 utentes do Sistema
Nacional de Saúde português. Os registos semanais aumentaram 3,5 vezes desde a implementação do CPARA até Maio 2013 (188 registos/semana aproximadamente), tendo sido feitos, maioritariamente, nos cuidados primários (74%). O ratio médio de registos por 100 000 habitantes foi de 163 em cada região continental NUTSII. A origem da informação proveio principalmente da história clínica transmitida ao médico pelo utente (57%), seguida do médico (28%), imunoalergologista especificamente (11%) e por outros profissionais de saúde (3%).
Caracterização dos registos de anafilaxia
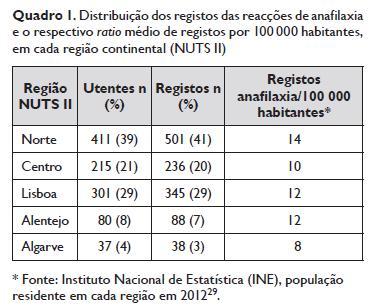
Durante o período referido, foram registados 1209 casos de reacções de anafilaxia, correspondendo a 6% da totalidade das reacções adversas notificadas no CPARA. Aqueles casos são relativos a 1045 utentes residentes em todo o território nacional. De acordo com a região NUTSII, a distribuição das reacções e o respectivo ratio médio de registos de anafilaxia por 100 000 habitantes em cada região continental está descrito no Quadro 1 . Observou-se uma semelhança nos ratios de registos de anafilaxia em todas as regiões, com um ratio médio de registos de 11,2/100 000 habitantes em cada região continental NUTS II.
Nestes registos, também o principal notificador foi o médico, com a informação clínica do utente (54%), seguido pelo médico, imunoalergologista e outros profissionais de saúde (29%, 16% e 2%, respectivamente).
Os utentes apresentavam uma idade média (±DP) de 51,8 (±20,2) anos, com idade mínima de 2 meses e idade máxima de 95 anos, em que 77 (7%) tinham idade inferior a 18 anos. A distribuição por grupos etários, agrupados em 10 anos, e por género está descrita na Figura 1. Em geral, observou-se um predomínio do género feminino (71%), com uma relação feminino/masculino de 2,4/1, acentuada nos casos em idade adulta (2,6/1). Nos casos de idade inferior a 18 anos, pelo contrário, observou-se um discreto predomínio do género masculino (1,1/1), com esta relação acentuada no grupo etário 0 a 10 anos, em que existe uma relação masculino/feminino de 1,6/1.

A frequência relativa das várias etiologias associadas às causas de anafilaxia, de acordo com o grupo etário, está representada no Quadro 2.
Globalmente, observou-se que a principal causa de anafilaxia foi a desencadeada por fármacos (n = 1008; 83%), sendo o grupo dos antibióticos beta‑lactamicos o predominante (46%), seguido dos anti‑inflamatorios não esteróides (AINEs) (22%) (Quadro 2). A segunda causa foi a desencadeada por alimentos (n = 87; 7%), com destaque para o marisco (23%), seguido dos frutos secos (17%) e leite e lacticínios (13%). Os venenos de insectos foram a terceira causa de reacções de anafilaxia (n = 40; 3%) e, por último, com frequência inferior a 1%, os grupos dos alergénios de contacto e dos aeroalergénios. Em apenas cerca de 5% das reacções o alergénio que desencadeou o episódio não foi identificado.
Comparando os grupos etários abaixo e acima dos 18 anos, observamos que há diferenças estatisticamente significativas entre as reacções de anafilaxia causadas por fármacos (p <0,001) e por alimentos (p <0,001).
No grupo de idade pediátrica (< 18 anos), a idade média (±DP) foi de 10,3 (±5,72) anos, com predomínio do género masculino, estatisticamente não significativo (57%; p=0,239) (Quadro 3). A taxa de anafilaxia mais elevada foi a desencadeada por alimentos (43%), com predomínio significativo do género masculino (71%; p=0,019). O grupo leite e lacticínios foi o principal indutor (24%), seguido de frutos secos (21%). A segunda causa foi devida ao alergénio fármacos (41%), sem diferenças significativas entre os sexos e sendo os antibióticos beta‑lactamicos os predominantes (48%).
No grupo dos adultos (≥ 18 anos), a idade média (±DP) foi de 54,8 (±17,0) anos, com predomínio estatisticamente não significativo do género feminino (p=0,461). A causa mais frequente foi a anafilaxia induzida por fármacos (87%), principalmente, e de forma significativa, no género feminino (74%; p=0,002) e devida aos antibióticos beta‑lactâmicos (46%). A segunda causa de anafilaxia neste grupo foi provocada por alimentos (4%), sem diferenças entre os sexos (p=0,672), tendo como principal agente causal o grupo do marisco (31%).
Relativamente à classificação das reacções anafilácticas, a maioria foi considerada Grave/Moderada (83%), não havendo diferenças estatisticamente significativas entre o grau de gravidade da reacção e cada grupo de alergénio.
Cerca de 72% das reacções tinham o estado do registo nao‑confirmado e da totalidade das reacções confirmadas, 26% estavam activas e 2% inactivas.
A maioria das reacções de anafilaxia foi causada por 1 alergénio (89%); enquanto 9% entre 2 a 4 alergénios e os restantes 2% referindo mais de 5 alergénios, com o máximo de 9, sendo neste caso predominante o grupo dos fármacos.
DISCUSSÃO
Este estudo descreve as reacções de anafilaxia registadas nos primeiros 10 meses de disponibilidade do Catálogo Português de Alergias e outras Reacções Adversas em todo o território português. Este está assente numa norma da DGS que obriga a notificação destas reacções a nível dos cuidados de saúde. Do nosso conhecimento, é a primeira análise de registos obrigatórios de episódios de anafilaxia em unidades de cuidados de saúde (primários e secundários, públicos e privados) de um serviço nacional de saúde.
Estes resultados corroboram, de uma maneira geral, os estudos epidemiológicos publicados nacional e internacionalmente relativos à distribuição da amostra e aos 3 grupos de alergénios mais associados às reacções de anafilaxia (fármacos, alimentos e venenos de insectos).
Cerca de 83% da amostra do estudo tinha idade igual ou superior a 18 anos, o que explica a predominância dos fármacos como causa da anafilaxia e a maioria de reacções ocorrer no género feminino7,22,23.
Tal como observado em diversos estudos5,7,8,11,14,21,22, os alergénios mais frequentes foram diferentes consoante o grupo etário e, dentro de cada grupo, também se eram do género feminino ou masculino.
No grupo das crianças (< 18 anos), o género masculino prevaleceu, tal como os alergénios alimentares, em particular o leite e lacticínios e os frutos secos como causas principais da anafilaxia, corroborando os resultados de estudos portugueses15,19,30 e de outros países13,14,17,18,20,31.
Os dados da notificação de anafilaxia da SPAIC identificam também o leite de vaca como a principal causa de anafilaxia alimentar no grupo pediátrico (dados não publicados).
A segunda causa mais frequente da anafilaxia nas crianças foram os fármacos, particularmente devido aos antibióticos beta‑lactamicos, em concordância com os dados da SPAIC, relativos à anafilaxia induzida por fármacos, publicados recentemente9,32.
Nos adultos, os principais alergénios medicamentosos foram os antibióticos beta‑lactamicos e os AINEs, semelhantes aos dados encontrados pela farmacovigilância portuguesa, que em 10 anos de notificação dos casos de anafilaxia causados por fármacos, os antibióticos e os AINEs foram os grupos mais predominantes33, mas contrastando com dados da SPAIC9,32, que reportaram os AINEs como causa principal e em segundo lugar os antibióticos beta‑lactamicos. O segundo grupo de alergénios que mais desencadeou episódios de anafilaxia nos adultos foi o dos alimentos, com o marisco como principal causa, tal como nos estudos de Solé e colaboradores7, de Ben‑Shoshan e colaboradores31 e em Portugal, confirmando o estudo de Morais‑Almeida e colaboradores15, assim como os dados da notificação de anafilaxia promovida pela SPAIC.
A notificação das alergias e outras reacções adversas através do CPARA, por abranger toda a população, tem o potencial para aumentar a segurança dos doentes nos cuidados de saúde, tal como foi documentado em vários estudos7,16,23‑25.
A principal limitação deste estudo foi partir do pressuposto de que os registos das reacções são todos credíveis, visto que a falta de formação sobre o preenchimento de cada uma das variáveis do CPARA pode ter conduzido a erros de categorização dos fármacos e até das próprias reacções alérgicas. De facto, ao fazer uma análise na base de dados do CPARA, de 1017 reacções classificadas como Outros alergénios, 637 (62%) foram reclassificadas (dados não apresentados), importando continuar a divulgar quer o CPARA quer a forma correcta de o utilizar.
Foi abrangido todo o território nacional, de uma forma uniforme, com taxas de notificação semelhantes em todas as regiões de Portugal continental. No entanto, como descrito na literatura34, estima‑se que exista uma sub‑notificação das reacções de anafilaxia, em que somente cerca de 6% das reacções adversas a fármacos são notificadas, atingindo um valor ainda mais baixo no que se refere a outros alergénios.
A identificação da falta de conhecimento e das atitudes relativas à sub‑notificação da anafilaxia no CPARA poderá proporcionar o desenvolvimento de medidas de divulgação e de formação para os profissionais de saúde, contribuindo assim para melhorar a qualidade dos registos no CPARA e, consequentemente, melhorar a prestação dos cuidados de saúde em Portugal.
Em conclusão, o CPARA é uma ferramenta extremamente útil na identificação e referenciação dos casos de anafilaxia na população portuguesa, tendo por isso elevado valor para o estudo desta importante patologia, com potencial para influenciar o seu prognóstico.
REFERÊNCIAS
1. Simons FE. Anaphylaxis. J Allergy Clin Immunol 2010;125(2 Suppl2): S161‑81. [ Links ]
2. Sampson HA, Munoz‑Furlong A, Campbell RL, Adkinson NF Jr, Bock SA, Branum A, et al. Second symposium on the definition and management of anaphylaxis: summary report – Second National Institute of Allergy and Infectious Disease/Food Allergy and Anaphylaxis Network symposium. J Allergy Clin Immunol 2006;117:391‑7. [ Links ]
3. Simons FE, Sampson HA. Anaphylaxis epidemic: fact or fiction? J Allergy Clin Immunol 2008;122:1166‑8. [ Links ]
4. Simons FE, Ardusso LR, Bilo MB, El‑Gamal YM, Ledford DK, Ring J, et al. World allergy organization guidelines for the assessment and management of anaphylaxis. J Allergy Clin Immunol 2011;127:593.e22. [ Links ]
5. Worm M. Epidemiology of anaphylaxis. Chem Immunol Allergy 2010;95:12‑21. [ Links ]
6. Tejedor Alonso MA, Moro Moro M, Mugica Garcia MV, Esteban Hernandez J, Rosado Ingelmo A, Vila Albelda C, et al. Incidence of anaphylaxis in the city of Alcorcon (Spain): a population‑based study. Clin Exp Allergy 2012;42:578‑89. [ Links ]
7. Sole D, Ivancevich JC, Borges MS, Coelho MA, Rosario NA, Ardusso LR, et al. Anaphylaxis in Latin America: a report of the online Latin American survey on anaphylaxis (OLASA). Clinics (Sao Paulo) 2011;66:943‑7. [ Links ]
8. Lieberman P, Camargo CA Jr, Bohlke K, Jick H, Miller RL, Sheikh A, et al. Epidemiology of anaphylaxis: findings of the American College of Allergy, Asthma and Immunology Epidemiology of Anaphylaxis Working Group. Ann Allergy Asthma Immunol 2006;97:596‑602. [ Links ]
9. Faria E, Rodrigues‑Cernadas J, Gaspar A, Botelho C, Castro E, Lopes A, et al. Drug‑induced anaphylaxis survey in Portuguese Allergy Departments. J Investig Allergol Clin Immunol 2014;24:40‑48. [ Links ]
10. Sheikh A, Hippisley‑Cox J, Newton J, Fenty J. Trends in national incidence, lifetime prevalence and adrenaline prescribing for anaphylaxis in England. J R Soc Med 2008;101:139‑43. [ Links ]
11. Peng MM, Jick H. A population‑based study of the incidence, cause, and severity of anaphylaxis in the United Kingdom. Arch Intern Med 2004;164:317‑9. [ Links ]
12. Mullins RJ. Anaphylaxis: risk factors for recurrence. Clin Exp Allergy 2003;33:1033‑40. [ Links ]
13. Ben‑Shoshan M, Clarke AE. Anaphylaxis: past, present and future. Allergy 2011;66:1‑14. [ Links ]
14. Lieberman P. Epidemiology of anaphylaxis. Curr Opin Allergy Clin Immunol 2008;8:316‑20. [ Links ]
15. Morais‑Almeida M, Gaspar A, Santa‑Marta C, Piedade S, Leiria‑Pinto P, Pires G, et al. Anafilaxia – Da notificação e reconhecimento à abordagem terapêutica. Rev Port Imunoalergologia 2007;15:19‑41. [ Links ]
16. Sicherer SH. Advances in anaphylaxis and hypersensitivity reactions to foods, drugs, and insect venom. J Allergy Clin Immunol 2003;111(3 Suppl):S829‑34. [ Links ]
17. Hompes S, Kohli A, Nemat K, Scherer K, Lange L, Rueff F, et al. Provoking allergens and treatment of anaphylaxis in children and adolescents – data from the anaphylaxis registry of German‑speaking countries. Pediatr Allergy Immunol 2011;22:568‑74. [ Links ]
18. Sole D, Ivancevich JC, Borges MS, Coelho MA, Rosario NA, Ardusso L, et al. Anaphylaxis in Latin American children and adolescents: the Online Latin American Survey on Anaphylaxis (OLASA). Allergol Immunopathol (Madr) 2012;40:331‑5. [ Links ]
19. Silva R, Gomes E, Cunha L, Falcao H. Anaphylaxis in children: a nine years retrospective study (2001‑2009). Allergol Immunopathol (Madr) 2012;40:31‑6. [ Links ]
20. Orhan F, Canitez Y, Bakirtas A, Yilmaz O, Boz AB, Can D, et al. Anaphylaxis in Turkish children: a multi‑centre, retrospective, case study. Clin Exp Allergy 2011;41:1767‑76. [ Links ]
21. Bohlke K, Davis RL, DeStefano F, Marcy SM, Braun MM, Thompson RS. Epidemiology of anaphylaxis among children and adolescents enrolled in a health maintenance organization. J Allergy Clin Immunol 2004;113:536‑42. [ Links ]
22. Sheikh A, Alves B. Age, sex, geographical and socio‑economic variations in admissions for anaphylaxis: analysis of four years of English hospital data. Clin Exp Allergy 2001;31:1571‑6. [ Links ]
23. Makinen‑Kiljunen S, Haahtela T. Eight years of severe allergic reactions in Finland: a register‑based report. World Allergy Organ J 2008;1:184‑9. [ Links ]
24. Namork E, Faeste CK, Stensby BA, Egaas E, Lovik M. Severe allergic reactions to food in Norway: a ten year survey of cases reported to the food allergy register. Int J Environ Res Public Health 2011;8:3144‑55. [ Links ]
25. Worm M, Timmermans F, Moneret‑Vautrin A, Muraro A, Malmheden Yman II, Lövik M, et al. Towards a European registry of severe allergic reactions: current status of national registries and future needs. Allergy 2010;65:671‑80. [ Links ]
26. Direção‑Geral Saúde. Anafilaxia: Abordagem Clínica. Norma da Direção‑Geral da Saúde ed: 014/2012; 2012. [ Links ]
27. Direção‑Geral Saúde. Anafilaxia: Registo e Encaminhamento. Norma da Direção‑Geral da Saúde ed: 004/2012; 2012. [ Links ]
28. Direcao‑Geral Saúde. Registo de Alergias e Reações Adversas. Norma da Direção‑Geral da Saúde ed: 002/2012; 2012. [ Links ]
29. INE, PORDATA. População residente. Fundação Manuel dos Santos; 2012 [updated June 2013; cited 2013 August]. [ Links ]
30. Morais‑Almeida M, Prates S, Pargana E, Arede C, Godinho N, Tavares C, et al. Alergia alimentar em crianças numa consulta de imunoalergologia. Rev Port Imunoalergologia 1999;7:167‑71. [ Links ]
31. Ben‑Shoshan M, Harrington DW, Soller L, Fragapane J, Joseph L, Pierre YS, et al. Demographic predictors of peanut, tree nut, fish, shellfish, and sesame allergy in Canada. J Allergy (Cairo) 2012;2012:858306. [ Links ]
32. Faria E, Rodrigues‑Cernadas J, Gaspar A, Botelho C, Castro E, Lopes A, et al. Anafilaxia induzida por fármacos: Registo Nacional2007‑2010. Rev Port Imunoalergologia 2012;20:93‑107. [ Links ]
33. Ribeiro‑Vaz I, Marques J, Demoly P, Polonia J, Gomes ER. Drug‑induced anaphylaxis: a decade review of reporting to the Portuguese Pharmacovigilance Authority. Eur J Clin Pharmacol 2013;69:673‑81. [ Links ]
34. Hazell L, Shakir SA. Under‑reporting of adverse drug reactions: a systematic review. Drug Saf 2006;29:385‑96. [ Links ]
João Almeida Fonseca
CINTESIS – Faculdade de Medicina da
Universidade do Porto
Rua Dr. Plácido da Costa
4200‑450 Porto
E-mail: fonseca.ja@gmail.com
AGRADECIMENTOS
Os autores gostariam de agradecer à equipa dos Serviços Partilhados do Ministério da Saúde, EPE, que implementou o CPARA, pela colaboração na extracção dos dados da base de dados do CPARA.
Financiamento: Nenhum. Declaração de conflitos de interesse: Nenhum.
Data de recepção / Received in: 30/09/2013
Data de aceitação / Accepted for publication in: 01/12/2013
Nota: Prémio da Sociedade Luso‑Brasileira de Alergia e Imunologia Clínica (SLBAIC) 2013