INTRODUÇÃO
Os agentes anestésicos representam uma causa importante de anafilaxia a fármacos, sendo os relaxantes neuromusculares (RNM) dos principais responsáveis pelos casos de anafilaxia perioperatória1. O diagnóstico pode ser desafiante, dado o número elevado de fármacos administrados simultaneamente. Diversos estudos apontam que, dos RNM, os agentes indutores de anafilaxia mais comuns são a succinilcolina, o rocurónio e o atracúrio2,3. Um estudo realizado em França classifica como RNM de alto risco a succinilcolina, o rocurónio e o alcurónio, de médio risco o pancurónio e o vecurónio e de baixo risco o atracúrio e o cisatracúrio4.
O cisatracúrio é o RNM mais recente, sendo um estereoisómero do atracúrio que se acreditava não ter potencial de libertação de histamina e, consequentemente, causar menos reações de hipersensibilidade do que os outros RNM2. No entanto, foram publicados recentemente alguns casos de reação anafilática após a administração de cisatracúrio5. Na Austrália foi realizado um estudo retrospetivo de alergia aos RNM durante um período de dez anos e não foi confirmado nenhum caso de alergia ao cisatracúrio6. Em Portugal não existem relatos conhecidos de reações de hipersensibilidade (HS) ao cisatracúrio. Foi realizado um estudo sobre os agentes causais de anafilaxia a fármacos em serviços de imunoalergologia em Portugal durante um período de quatro anos, que incluiu 313 doentes, não tendo sido reportado nenhum caso de HS ao cisatracúrio7.0 Num outro estudo retrospetivo realizado em Portugal em doentes com suspeita de reações alérgicas/de hipersensibilidade perioperatórias durante um período de dez anos, constatou-se também que não foi confirmado nenhum caso de HS ao cisatracúrio8.
A anafilaxia perioperatória é um fenómeno raro e imprevisível, mas potencialmente fatal se não diagnosticada e tratada rapidamente. A investigação destes casos é essencial para a identificação do fármaco responsável, de forma a evitar nova exposição e encontrar alternativas terapêuticas seguras.
As autoras apresentam dois casos de anafilaxia com sensibilização confirmada ao cisatracúrio em Portugal.
CASO 1
Doente do sexo masculino, 50 anos, proposto para herniorrafia, referenciado a consulta de Imunoalergologia por antecedentes de dois episódios não investigados de reação HS perioperatória, com anafilaxia grave e necessidade de reanimação cardiorrespiratória. Aos 26 anos, em contexto de hérnia discal, foi submetido a intervenção cirúrgica e, durante a fase de indução anestésica, iniciou sensação de mal-estar geral, tonturas e má perfusão periférica com evolução para paragem cardiorrespiratória com necessidade de reanimação. Não foi colhida triptase nem realizada investigação diagnóstica pós-reação, tendo sido informado que seria alérgico a corticosteroides e desde essa altura ficou em evicção dos mesmos. Cerca de 15 anos depois, foi submetido novamente a cirurgia ortopédica, tendo iniciado quadro semelhante durante a fase de indução anestésica, também com necessidade de reanimação. Não são conhecidos os fármacos administrados nessas duas intervenções e, à semelhança da primeira reação, não foi efetuada qualquer investigação. Em 2019 foi submetido a mais duas cirurgias, uma sob anestesia geral e outra sob anestesia local, sem intercorrências.
No âmbito da investigação alergológica realizou testes cutâneos com corticosteroides, que se revelaram negativos. Posteriormente, foi realizada prova de provocação oral com prednisolona que foi negativa, fármaco que o doente tolerou posteriormente. Pela história de intervenção cirúrgica recente sob anestesia geral sem intercorrências, foi solicitada a folha anestésica do procedimento, com os seguintes fármacos tolerados: midazolam, propofol, quetamina, fentanilo, ondansetron, paracetamol, cetorolac, cefuroxime, esomeprazol, morfina e clorexidina. O doente referia tolerância a iodopovidona, utilizada em procedimentos anteriores. Procedeu-se à investigação através da realização de testes cutâneos com fármacos potencialmente utilizados nas cirurgias em que houve reação e de que não há registo posterior de tolerância, com positividade para o cisatracúrio 2mg/ml (intradérmico na diluição de 1:100), negativos para rocurónio, atracúrio e látex (Tabela 1). O doente ficou em evicção estrita de cisatracúrio, com indicação escrita dos fármacos alternativos passíveis de ser utilizados em cirurgias posteriores - atracúrio e rocurónio.
Tabela 1 Testes cutâneos e IgE específica realizados no âmbito da investigação alergológica
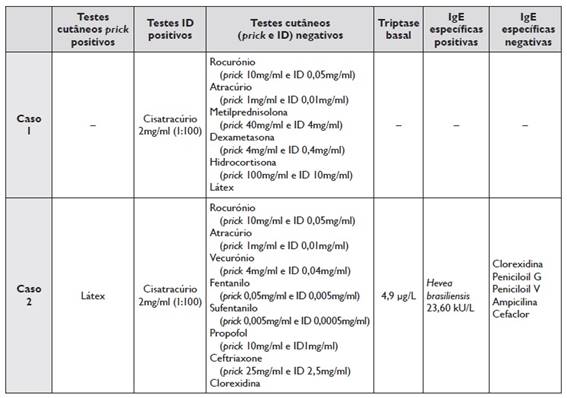
Legenda: ID - intradérmico
CASO 2
Doente do sexo masculino, 47 anos, proposto para encerramento de fístula vesicocutânea em maio de 2017.
A indução anestésica foi realizada com fentanilo, rocurónio, propofol e ceftriaxone. Quarenta minutos após o início da cirurgia iniciou hipotensão, hipoxemia e broncospasmo, tendo sido medicado com adrenalina intramuscular e endovenosa por hipotensão mantida, corticosteroides e anti-histamínicos, com recuperação hemodinâmica em algumas horas, e posteriormente foi internado no serviço de urologia. Analiticamente apresentava uma triptase sérica de 15,4 μg/L, colhida uma hora após o início da reação. A avaliação da triptase basal realizada uma semana depois revelou-se normal.
Tratava-se de um doente com antecedentes de traumatismo vertebromedular consequente de acidente de viação aos 19 anos, submetido a múltiplas cirurgias plásticas (>10) por lesões de queimadura dos membros inferiores e úlceras perineais de repetição e cirurgias urológicas para correção de fístula vesicocutânea. Foi submetido a apendicectomia e correção de úlcera perineal em 2011, cirurgia interrompida por hipotensão, hipoxemia e paragem cardiorrespiratória. Segundo registos do hospital onde foi realizada a cirurgia, terá sido administrado cisatracúrio como RNM. Na consulta de imunoalergologia realizou testes cutâneos com os fármacos que constavam na folha anestésica (Tabela 1), tendo-se observado positividade para o látex (prick) e cisatracúrio 2mg/ml (intradérmico positivo para 1:100). Relativamente ao ceftriaxone, após testes cutâneos negativos o doente foi submetido a prova de provocação, que foi negativa, tendo tolerado posteriormente este fármaco. Destacava-se ainda a presença de IgE específica para Hevea brasiliensis de 23,60 kU/L (Tabela 1). Quando inquirido, o doente referiu prurido e urticária com a exposição a objetos com látex. Considerou-se então o látex como agente causal na segunda reação. No caso descrito, foram identificados dois potenciais alergénios como causadores de anafilaxia perioperatória. Confirmou-se reação de hipersensibilidade imediata ao látex e ao cisatracúrio, com indicação escrita dos fármacos alternativos passíveis de ser utilizados em cirurgias posteriores. Relativamente ao rocurónio, cujos resultados dos testes cutâneos foram negativos, foi fornecida ao doente informação escrita para idealmente se optar por outro RNM e, caso haja necessidade de administrar rocurónio, ser contactada a imunoalergologia de forma a estar presente no bloco operatório. O doente teve ainda indicação para ser submetido a intervenções cirúrgicas em ambiente isento de látex, devendo ser o primeiro doente a ser intervencionado no dia agendado.
DISCUSSÃO
A anafilaxia é uma reação de hipersensibilidade sistémica grave e com risco de vida. É causada pela desgranulação de mastócitos e basófilos, com consequente libertação de mediadores pré-formados, incluindo histamina e triptase. O diagnóstico de reação anafilática habitualmente é clínico, embora o mesmo possa ser suportado pelo estudo analítico. Dos testes in vitro, destacam-se o doseamento da triptase sérica, o doseamento de IgE específica e o teste de ativação de basófilos (TAB)9.
A triptase é um biomarcador armazenado nos grânulos dos mastócitos quiescentes, sendo libertado na corrente sanguínea em consequência da desgranulação dos mastócitos. A triptase atinge picos séricos em 60 a 90 minutos após o início da anafilaxia, podendo permanecer elevada durante algumas horas10. O TAB por citometria de fluxo usando os marcadores CD63 e/ou CD203c é considerado um complemento útil aos testes cutâneos (TC) no diagnóstico de anafilaxia a RNM em doentes com história clínica sugestiva9,10. Segundo um artigo de revisão recente, a sensibilidade e especificidade destes testes para RNM variam entre 38,5% a 92% e 92% a 100%, respetivamente11. Considera-se ainda uma técnica promissora na avaliação da reatividade cruzada entre RNM11.
A identificação dos fármacos responsáveis por reações anafiláticas perioperatórias é desafiante, dado o número elevado de fármacos que são administrados simultaneamente num intervalo de tempo relativamente curto.
O diagnóstico retrospetivo pode depender da rápida referenciação para evitar perda de informação clínica importante, sendo que a folha anestésica é um elemento fulcral para a investigação. A rapidez e eficácia do diagnóstico dependem, ainda, dos TC e/ou resultados analíticos. No segundo caso verificou-se um aumento da triptase sérica na altura da reação, o que vai de encontro ao diagnóstico de anafilaxia. Neste caso foi possível confirmar a alergia ao látex através da clínica e resultados dos TC e presença de IgE específica para a Hevea brasiliensis aumentada. Os TC com RNM foram positivos para o cisatracúrio em ambos os casos e negativos para os restantes RNM testados. A reatividade cruzada (RC) demonstrada para os RNMs dificulta a escolha de um fármaco alternativo, embora os autores não sejam muito consensuais neste tema10. Num estudo realizado em França constatou-se que os doentes alérgicos a um RNM apresentam um risco de alergia de 60-70% a outro RNM. O padrão de reatividade cruzada varia entre os doentes e parece ser mais frequente entre os RNM do grupo aminoesteroides (pancurónio, vecurónio e rocurónio) do que entre os derivados benzilisoquinolinas (D-tubocuramina, cisatracúrio, atracúrio, mivacúrio e alcurónio)12. O cisatracúrio mostrou a mais baixa taxa de reatividade cruzada em doentes alérgicos a outros RNM6,12.
Acreditava-se que o cisatracúrio não tinha potencial evidente de libertação de histamina, causando menos reações alérgicas do que outros RNM, tendo vindo por isso a ser cada vez mais utilizado2. No entanto, foram relatados vários casos de reação anafilática grave após administração de cisatracúrio. Na pesquisa bibliográfica não foram encontrados casos descritos em Portugal de alergia ao cisatracúrio, sendo por isso importante alertar que este RNM não será tão desprovido de potencial alergénico como previamente considerado, e perante reação alérgica durante a indução anestésica esse facto deve ser considerado na investigação imunoalergológica. Recomendações recentes sugerem a utilização de um RNM cujo TC e o TAB sejam negativos10. Apesar da utilidade e complementaridade do TAB, têm vindo a ser verificadas dificuldades na realização deste método diagnóstico no nosso centro hospitalar, pelo que não foi possível incluí-lo na investigação. Tendo em conta o resultado dos testes cutâneos negativos e sabendo que o cisatracúrio apresenta baixa reatividade cruzada, à partida podem ser utilizados como RNMs alternativos, em ambos os nossos casos, o rocurónio e o atracúrio. Seria, no entanto, prudente adicionar o TAB, assim que disponível, para segurança adicional à sua administração.
Os testes cutâneos no Caso 2 mostraram ainda que, mesmo no caso de alergia confirmada ao látex, a investigação alergológica deve prosseguir e incluir todos os fármacos suspeitos.
É imprescindível que os médicos assistentes referenciem os doentes com antecedentes pessoais de anafilaxia perioperatória para consulta de Imunoalergologia. No pedido de consulta deve constar a informação clínica do episódio e toda a medicação administrada no período perioperatório, de modo a permitir uma investigação diagnóstica mais eficiente e uma evicção do(s) fármaco(s) implicado(s), bem como a obtenção de alternativas terapêuticas de um modo relativamente rápido e seguro.
CONCLUSÕES
As autoras apresentam os primeiros casos clínicos de anafilaxia com sensibilização confirmada ao cisatracúrio descritos em Portugal, com restantes RNM negativos. Com estes casos pretendem alertar para o facto de apesar do cisatracúrio ser um RNM considerado “seguro”, deve ser investigado nas anafilaxias perioperatórias.