INTRODUÇÃO
As reações de hipersensibilidade (RH) a antineoplásicos em crianças têm sido documentadas de forma crescente 1,2. A apresentação clínica é variável, podendo ir de manifestações cutâneas ligeiras a formas potencialmente fatais.
As reações imediatas são o tipo mais comum de RH e, teoricamente, podem ocorrer com qualquer fármaco antineoplásico. Geralmente, quando um doente se sensibiliza a um fármaco, o tratamento em curso é interrompido e substituído por um medicamento alternativo, frequentemente menos eficaz ou menos seguro, podendo afetar o prognóstico final.
A dessensibilização a fármacos é um procedimento desconhecido por grande parte dos oncologistas, apesar de permitir que os doentes sejam tratados com agentes de primeira linha através da obtenção de um estado temporário de tolerância ao fármaco ao qual o doente reagiu 3. A dessensibilização consiste na administração de doses sucessivamente crescentes do fármaco em questão até à dose terapêutica pretendida ser atingida, levando a que os mastócitos/basófilos entrem em período refratário 4. No caso de citoestáticos é necessária a dessensibilização ao fármaco a cada novo ciclo, atendendo a que o intervalo entre os tratamentos é habitualmente de 2 a 4 semanas
Este procedimento é realizado principalmente em reações imediatas, contudo casos bem-sucedidos de dessensibilizações em RH não imediatas ligeiras têm sido descritos 5.
Atualmente ainda não existem normas de orientação de dessensibilização a fármacos em idade pediátrica e os princípios gerais adotados para os adultos têm sido aplicados em crianças, diferindo apenas na dose cumulativa administrada.
A carboplatina é um composto de platina de segunda geração que tem sido utilizado como alternativa à cisplatina, o primeiro fármaco desta classe a ser sintetizado. A carboplatina apresenta uma eficácia semelhante à da cisplatina, mas com menor incidência de neurotoxicidade, nefrotoxicidade e sintomas gastrointestinais 6. Em crianças, a carboplatina é utilizada para o tratamento de tumores de células germinativas, hepatoblastoma, retinoblastoma, neuroblastoma e de outros tipos de tumores cerebrais. A combinação de carboplatina e vincristina induz respostas consistentes e duradouras em crianças com glioma de baixo grau (GBG), sendo o esquema farmacológico mais amplamente adotado nestes casos 7.
Os dados da literatura sobre as RH associados à carboplatina em crianças são muito limitados, tendo sido documentada uma incidência de RH à carboplatina em até 47% das crianças afetadas por GBG 8-10. O risco de hipersensibilidade à carboplatina parece estar relacionado com o número cumulativo de infusões e não com a dose cumulativa de cada infusão 1. Em adultos, as reações geralmente ocorrem a partir do sexto ciclo e tendem a ocorrer ligeiramente mais tarde em idade pediátrica 1,3,9,11. Nos últimos anos, foram publicadas várias séries de casos de dessensibilização à carboplatina em idade pediátrica, com diferentes graus de sucesso (20 a 100%) e com as maiores taxas de sucesso observadas em séries que incluíram reações mais ligeiras ou com doses mais baixas de carboplatina 2,9,10,14-17.
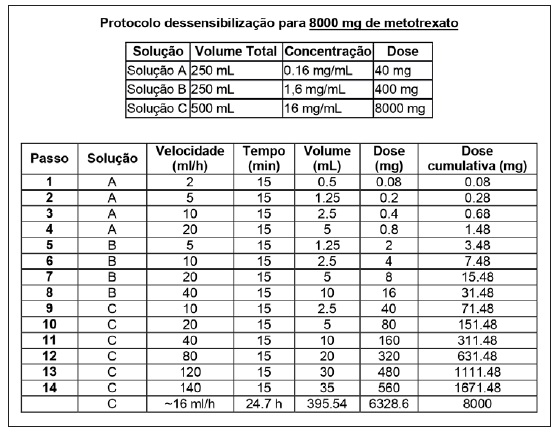
O metotrexato é um potente imunossupressor e antineoplásico que é utilizado em altas doses (5 g/m2) para o tratamento de neoplasias hematológicas pediátricas. Desde meados da década de 1960, a administração intratecal deste fármaco tem sido amplamente utilizada para prevenção ou tratamento de leucemias do sistema nervoso central 12.
Foram documentadas RH ao metotrexato em adultos mas mais raramente em crianças. As RH ao metotrexato ocorrem mais frequentemente com a reexposição e vários mecanismos, para além da mediação pela IgE, podem estar envolvidos 13.
A literatura sobre dessensibilização ao metotrexato em crianças e adultos limita-se à descrição de casos clínicos ou a pequenas séries de casos 13. A segurança da administração de metotrexato intratecal após RH com a administração endovenosa em altas doses não se encontraainda bem estabelecida.
OBJETIVO
Descrever a experiência de um serviço de imunoalergologia de um hospital central na dessensibilização à carboplatina e ao metotrexato em idade pediátrica.
MATERIAL E MÉTODOS
Revisão retrospetiva dos registos clínicos de crianças referenciadas à Área de Alergia a Fármacos do Serviço de Imunoalergologia do Centro Hospitalar Universitário de São João (CHUSJ), entre 2009 e 2021, por reações de hipersensibilidade (RH) à carboplatina e metotrexato que foram submetidos a protocolos de dessensibilização.
O Centro de Referência de Oncologia Pediátrica do Norte agrega o CHUSJ e o Instituto Português de Oncologia (IPO) do Porto na prestação de cuidados de saúde às crianças diagnosticadas com patologia oncológica na região norte do país, sendo que cada um dos centros dirige a sua atividade para um conjunto de patologias oncológicas específicas, nomeadamente tumores sólidos no CHUSJ e líquidos no IPO. Atendendo a esta condição, foram efetuadas dessensibilizações à carboplatina no CHUSJ e ao metotrexato no IPO. No período em análise, não foram realizadas dessensibilizações a outros antineoplásicos em crianças.
O protocolo habitual de administração de carboplatina utilizado pela Oncologia Pediátrica inclui pré-medicação com anti-histamínico e metilprednisolona (1 mg/kg) uma hora antes da infusão, hidratação endovenosa e ondansetron como antiemético.
Habitualmente, nos doentes com RH ligeiras, a pré-medicação é reforçada e a velocidade da infusão reduzida nas administrações subsequentes antes da referenciação à Imunoalergologia pela Oncologia Pediátrica. Os doentes que toleraram a reexposição à carboplatina com estas medidas preventivas não foram incluídos neste estudo.
O protocolo de tratamento das neoplasias hematológicas com metotrexato inclui uma perfusão endovenosa ao longo de 24 horas, composta pela infusão intravenosa de 1/10 da dose durante a primeira hora seguida da perfusão dos 9/10 restantes ao longo das 23 horas subsequentes, terminando com uma dose baixa de metotrexato intratecal. Não está protocolada a realização de pré-medicação. Em todos os casos descritos, a decisão de avançar para a dessensibilização foi baseada numa forte suspeita de RH e na ausência de um fármaco alternativo igualmente eficaz. O benefício de manter o fármaco implicado foi considerado, uma vez que existe o risco de reações mais graves 14. Sempre que possível, os procedimentos foram precedidos por testes cutâneos por picada (10 mg/mL) e intradérmicos (1 e 10 mg/mL) com carboplatina, de acordo com as recomendações internacionais 3. De forma a minimizar a dor associada a este procedimento, um adesivo de prilocaína-lidocaína (EMLA®) foi aplicado com 30 a 60 minutos de antecedência. Não foram realizados testes cutâneos com metotrexato.
A família foi sempre informada dos riscos e benefícios deste procedimento, o consentimento informado assinado e a motivação e capacidade de colaboração foram avaliadas. Salienta-se que em nenhum caso limitações no apoio familiar impossibilitaram o tratamento; a logística hospitalar e o esquema terapêutico (pré-medicação) foram adaptados nestes casos.
Todos os procedimentos de dessensibilização foram efetuados sob supervisão médica rigorosa de oncologistas pediátricos e de imunoalergologistas com experiência na elaboração e aplicação dos protocolos. Nos casos ligeiros ou moderados, os procedimentos de dessensibilização foram realizados no hospital de dia de Oncologia Pediátrica ou na enfermaria de Pediatria. Nos casos de anafilaxia, o primeiro protocolo de dessensibilização foi sempre aplicado na Unidade de Cuidados Intensivos de Pediatria e, nos casos em que não ocorreram reações durante o procedimento, os tratamentos subsequentes foram transferidos para os locais descritos para os casos ligeiros a moderados. Uma vez que as doses dos citostáticos são calculadas por metro quadrado de superfície corporal, as doses terapêuticas foram ajustadas para cada criança e de forma regular a cada tratamento.
Até 2011 foram aplicados protocolos adaptados de Confino-Cohen et al 15 com infusão de 4 soluções de concentrações crescentes do fármaco ao longo de cerca de 90 minutos cada, com uma duração total de 6 horas.
Desde então o protocolo de 12 passos desenvolvido por Castells et al 16 tem sido utilizado e adaptado à dose total pretendida e à gravidade das reações.
Neste último protocolo são utilizadas três ou mais soluções parentéricas com concentrações décuplas crescentes preparadas na farmácia hospitalar de Oncologia, iniciando-se por uma solução diluída a 1/100. Um protocolo de 12 passos com aumentos progressivos da velocidade de perfusão é inicialmente aplicado. Cada passo tem uma duração de 15 minutos, com a exceção do último, que prossegue durante o tempo necessário para que a dose remanescente do fármaco seja administrada.
Quatro crianças foram dessensibilizadas com o um protocolo adaptado de Confino-Cohen et al e as restantes 13 com o protocolo desenvolvido por Castells et al.
RESULTADOS
Um total de 58 crianças receberam carboplatina endovenosa durante o período avaliado. Dezassete desenvolveram uma reação compatível com RH mediada pela IgE com uma incidência estimada de 29%.
Todas apresentavam o diagnóstico de glioma de baixo grau (GBG) e estavam a ser tratadas com um esquema quimioterápico que incluía a administração mensal de carboplatina (550 mg/m2) e vincristina, de acordo com as recomendações da Sociedade Internacional de Oncologia Pediátrica (SIOP) 7.
A mediana de idade aquando da RH à carboplatina foi de 4 anos (entre 18 meses e 9 anos). A maioria era do sexo feminino (53%). Apenas um doente tinha sido exposto previamente a este fármaco cinco anos antes, tendo a RH ocorrido durante um novo ciclo de tratamentos após progressão da doença. Apenas quatro dos 17 doentes eram atópicos.
Um número médio de 8 tratamentos (entre 2 a 10) de carboplatina foi administrado até à ocorrência da reação de hipersensibilidade (RH). A maioria das reações ocorreu menos de 30 minutos após o início da infusão (todos <1 hora). O padrão clínico das reações variou de ligeiro (8 doentes apresentaram sintomas cutâneos isolados) a grave (8 reações foram anafiláticas). Das anafilaxias, duas foram classificadas como graves, segundo os critérios de Brown 17, com sintomas cutâneos generalizados, manifestações gastrointestinais e queixas respiratórias com dessaturação e cianose.
O valor da triptase aquando da reação e basal foi medido em apenas 5 dos 8 doentes com anafilaxia e encontrava-se elevada (triptase basal x 1,2+2 ng/mL) em 3 deles. Apenas um doente recebeu tratamento com adrenalina.
Os testes cutâneos foram negativos em todos os 4 doentes testados. A IgE específica para a carboplatina e cisplatina foi avaliada em 3 doentes e foi positiva em um deles (IgE para carboplatina de 1,6 kU / L e para cisplatina de 4,2 kU / L ,UniCAP; Phadia, Uppsala, Suécia). Não ocorreram atrasos nos tratamentos devido à necessidade de dessensibilização; os tratamentos foram realizados após a data pretendida apenas por indicação da Oncologia Pediátrica.
No total, foram realizados 112 procedimentos de dessensibilização à carboplatina (entre 279 e 706 mg) nas 17 crianças com uma mediana de 6,6 tratamentos por doente (entre 2 e 14). Em 7 doentes, a dessensibilização foi realizada com sucesso na primeira abordagem. Em 10 doentes (59%), devido a reações durante o procedimento, foram realizadas adaptações ao protocolo inicial, incluindo a adição de um ou mais passos intermédios ou de um quarto saco com nova concentração (habitualmente uma diluição inicial de 1/1000) e a pré-medicação (anti- histamínicos, corticosteroides e montelucaste) foi reforçada (Figura 1).
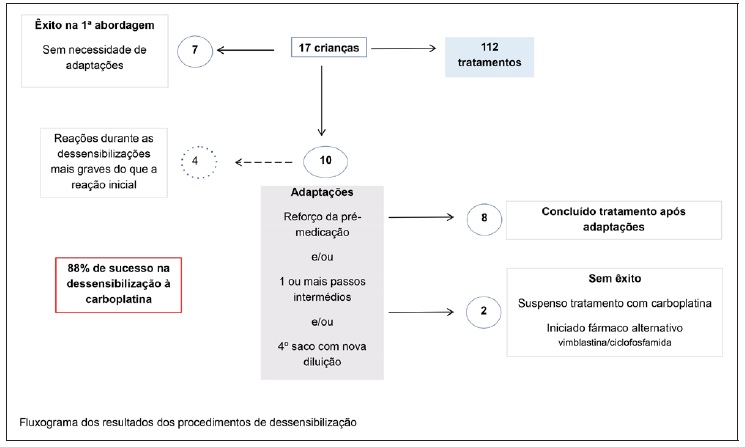
Figura 1 Resultados dos procedimentos de dessensibilização à carboplatina em doentes em idade pediátrica no Centro Hospitalar Universitário de São João entre 2011 e 2021
Habitualmente as reações durante as dessensibilizações ocorreram nos últimos passos do protocolo, correspondendo à administração das doses mais elevadas. Na maioria dos casos as reações resolveram com interrupção da infusão e administração de medicação de acordo com a reação; a infusão só foi reiniciada após a resolução dos sintomas. As reações durante a dessensibilização foram mais graves do que a reação inicial em 4 doentes (24% das crianças).
Em apenas 2 doentes não foi possível concluir os ciclos previstos com a carboplatina devido a reações persistentes durante a dessensibilização, apesar de todas as adaptações realizadas. Estes doentes não corresponderam aos casos com reações iniciais mais graves. Após a suspensão do tratamento com caboplatina, foi prescrita ciclofosfamida a um doente e vimblastina a outro.
Foram dessensibilizadas 4 crianças com metotrexato, 3 com o diagnóstico de leucemia linfoblástica aguda e uma com o diagnóstico de linfoma anaplásico. Todos os doentes tinham sido previamente expostos ao metotrexato e a RH ocorreu no primeiro ciclo de novo tratamento em três doentes e no sexto ciclo em apenas um. Três doentes reagiram durante a primeira hora de infusão e um doente apresentou sintomas cutâneos cerca de 72 horas após a administração endovenosa e intratecal do fármaco. O primeiro doente, um rapaz de 9 anos diagnosticado com leucemia linfoblástica aguda, apresentou urticária generalizada cerca de 30 minutos após o início da infusão. Em tratamento subsequente, efetuou pré-medicação com clemastina e hidrocortisona uma hora antes e realizou um protocolo de dessensibilização endovenosa ao longo de 33 horas, seguido de administração intratecal gradual do fármaco, com tolerância.
Os doentes 2 e 3 eram duas raparigas com 8 e 9 anos que apresentaram urticária generalizada e anafilaxia, respetivamente, imediatamente após o tratamento com metotrexato. O protocolo terapêutico em curso preconizava a perfusão com metotrexato por 24 horas, seguindo-se a administração intratecal. Nestes dois casos foram aplicados protocolos de 12 passos em 6 horas com o objetivo de atingir uma velocidade de perfusão predefinida (e não a dose alvo total) que subsequentemente se manteve cerca de 24 horas, até a dose total ser atingida.
Após o sucesso do primeiro doente, considerou-se que o estado de tolerância atingido durante o procedimento de dessensibilização endovenosa a uma alta dose de metotrexato (>5000 mg) tornaria segura a administração intratecal de 12 mg de metotrexato (estabelecida pelo protocolo de tratamento em curso), pelo que esta foi administrada na dose total imediatamente após o fim da perfusão endovenosa do fármaco. Não ocorreu qualquer reação em ambas as doentes.
Foi utilizado um protocolo semelhante no quarto doente, um rapaz de 12 anos que desenvolveu um exantema maculopapular 72 horas após o tratamento com metotrexato endovenoso e intratecal (Figura 2). Não apresentou sinais de gravidade, como febre, flictenas, áreas de descolamento cutâneo, envolvimento de mucosas ou alterações laboratoriais. O doente recebeu pré-medicação com montelucaste dois dias antes e prednisolona 40 mg um dia antes e durante os quatro dias seguintes ao tratamento. O procedimento foi seguido pela administração intratecal da dose total do fármaco (12 mg), sem qualquer reação imediata ou tardia.
DISCUSSÃO
A taxa de incidência de hipersensibilidade à carboplatina varia de 6% a 47% de crianças diagnosticadas com glioma de baixo grau (GBG) em diferentes estudos 8-10.
A incidência mais elevada foi encontrada na coorte de Dudgshun et al 8 e diferiu de acordo com o protocolo terapêutico utilizado; 8% dos doentes tratados apenas com carboplatina e 68% daqueles tratados com carboplatina e vincristina apresentaram RH, respetivamente, postulando-se a existência de um efeito imunológico potenciador causado pela combinação destes fármacos. No presente estudo, apesar de todos os doentes terem sido tratados com carboplatina e vincristina, a incidência de RH foi significativamente menor (29%). Não foram incluídos doentes que toleraram infusões subsequentes com medidas preventivas, o que pode explicar a diferença nos resultados, já que apenas 1/3 dos doentes da série de Dodgshun foram dessensibilizados à carboplatina. A anafilaxia representou 47% das RH à carboplatina, em conformidade com a literatura que relata que uma importante proporção das RH aos sais de platina são graves18.
Valores elevados de triptase em fase aguda apoiam o diagnóstico de anafilaxia, favorecendo a realização de dessensibilização, apesar de um resultado normal não permitir a exclusão desta hipótese. A triptase não foi colhida de forma sistemática durante as RH, uma vez que este parâmetro ainda é subvalorizado por outras especialidades durante a abordagem de uma RH e nem sempre se encontra disponível. Consistentemente em estudos prévios as reações ocorreram em média ao oitavo ciclo1,3,6,9,11,14.
Vários autores têm recomendado testes cutâneos profiláticos aos sais de platina entre o quinto e o oitavo ciclo para prever o risco futuro de RH (valor preditivo negativo e positivo em adultos de 99 e 86%, respetivamente)19. No entanto, as implicações de um teste positivo ainda não são claras, especialmente em crianças.
Os testes cutâneos diagnósticos apresentam uma sensibilidade de 100% para a carboplatina e um valor preditivo negativo de 94% 20; contudo, não foi possível a sua realização em todos os doentes, já que o momento ideal implicaria atrasar o ciclo de tratamento e a sua realização precoce aumentaria o risco de resultados falsos-negativos.
Dos 4 doentes testados, nenhum apresentou testes cutâneos positivos, inclusivamente a criança com IgE específica positiva. As concentrações não irritativas para a carboplatina encontram-se validadas apenas em adultos e as crianças podem comportar-se de forma diferente e apresentar resultados positivos com menor frequência ou com concentrações distintas 21. Na realização dos testes cutâneos com EMLA® com outros fármacos não foram encontradas diferenças nos resultados, mas as platinas não foram avaliadas neste estudo 22.
Os doentes incluídos nesta revisão apresentaram alta incidência de reações anafiláticas e/ou persistência de sintomas, apesar das medidas preventivas (pré-medicação e redução da velocidade de administração), o que, aliado à sua fragilidade inerente, não justificou a realização de provas de provocação diagnósticas após uma ponderação benefício/riscos. Embora nenhuma das suspeitas de RH à carboplatina tenha sido confirmada por testes cutâneos, a elevada incidência de reações durante as dessensibilizações (em 76% dos doentes) corroborou a suspeita inicial. As reações durante as dessensibilizações foram mais graves do que a reação inicial em 24% doentes; uma caracterização mais precisa das reações pelos imunoalergologistas pode ser uma explicação, embora seja conhecido o risco de reações mais graves durante as dessensibilizações.
As reações graves durante as dessensibilizações, mesmo em casos de reação inicial ligeira-moderada, comprovam a necessidade de estes procedimentos serem realizados por imunoalergologistas experientes, sob vigilância rigorosa e num centro de referência em Oncologia Pediátrica.
Duas mortes ocorreram após a conclusão do tratamento devido à progressão da doença. Em apenas 2 dos 17 doentes (12%) não foi possível completar o tratamento com carboplatina, devido à persistência de sintomas mucocutâneos desconfortáveis, apesar de várias adaptações ao protocolo inicial. Em doentes com hipersensibilidade à carboplatina, as opções terapêuticas disponíveis são a dessensibilização ou a sua substituição por um fármaco alternativo igualmente eficaz. A substituição da carboplatina por outro composto de platina, como a cisplatina, pode ser limitada pela reatividade cruzada, apesar de a verdadeira prevalência de reatividade cruzada entre os dois fármacos ainda não se encontrar totalmente definida23,24. A maior toxicidade da cisplatina também foi responsável pela opção da dessensibilização à carboplatina.
Nos casos em que não foi possível concluir o tratamento com a carboplatina, os fármacos alternativos selecionados foram a ciclofosfamida e a vimblastina e não a cisplatina, por decisão da Oncologia. De referir que estes 2 casos ocorreram em 2011 e 2014, altura em que não existiam ainda dados sobre a segurança e eficácia da utilização de anti-IgE como pré-medicação em dessensibilizações a sais de platina. Recentemente foram publicados casos com a utilização de omalizumab em doentes que não toleraram os protocolos de dessensibilização, podendo ser uma estratégia a considerar no futuro em crianças. 25
A taxa de sucesso nas dessensibilizações à carboplatina neste estudo foi de 88%, comparável às taxas descritas em outras séries de adultos, mas significativamente diferente de outras séries pediátricas com taxas de sucesso entre 8 e 100% 7,8,10,11,21. Foram utilizados vários protocolos e as taxas de sucesso mais elevadas ocorreram em séries em que fora aplicados protocolos de 12 passos de Castells 21.
Em relação às RH ao metotrexato, estas ocorreram sempre durante a reexposição e a maioria (75%) apresentou sintomas sugestivos de reação IgE mediada, de acordo com as raras descrições na literatura 13. Apesar de os testes cutâneos serem uma ferramenta útil na avaliação destes doentes, como na carboplatina, não foram realizados de forma a não atrasar o esquema terapêutico.
Adicionalmente as concentrações não irritativas para o metotrexato ainda não se encontram validadas; as concentrações utilizadas em alguns estudos foram de 10 mg/ml nos testes cutâneos por picada e de 0,1; 1 e 10 mg/ml nos intradérmicos 13. Nestes doentes não foi colhida de forma sistemática triptase durante a reação. Contudo, as características das reações e a fragilidade destes doentes favoreceram a dessensibilização em relação à prova de provocação diagnóstica.
Foi administrada medicação previamente às dessensibilizações com o objetivo de minimizar o risco de reações durante os procedimentos. Esta foi selecionada de acordo com a reação inicial do doente. Os protocolos de 12 passos aplicados para o metotrexato foram semelhantes aos utilizados para a carboplatina, diferindo principalmente no maior tempo total de infusão, resultante das elevadas doses necessárias deste fármaco.
Está descrita uma reação anafilática após a administração intratecal de metotrexato 12, podendo assim deduzir-se que a barreira hematoencefálica é permeável ao fármaco e que a administração intratecal resulta em exposição sistémica. De facto, na abordagem do primeiro doente foi realizada dessensibilização intratecal do fármaco, apesar de ter realizado previamente dessensibilização à dose total do fármaco por via endovenosa.
Essa experiência positiva permitiu, nos doentes subsequentes, a administração intratecal em dose única, com maior segurança após dessensibilização endovenosa com metotrexato em alta dose, sugerindo que o procedimento de indução de tolerância sistémica funciona na prevenção de reações no decurso de administrações intratecais que se seguem ao tratamento endovenoso.
As reações de hipersensibilidade tardia a fármacos podem ser fatais e, classicamente, constituem uma contraindicação à dessensibilização. Contudo, em casos selecionados de exantemas não complicados, quando o fármaco implicado é insubstituível, esta opção pode ser considerada.
As limitações do estudo incluem a reduzida amostra de doentes e a ausência de todos os dados em alguns doentes devido ao seu caráter retrospetivo.
CONCLUSÃO
O risco de reações de hipersensibilidade (RH) a antineoplásicos em idade pediátrica não deve ser subestimado. A carboplatina foi o fármaco mais frequentemente implicado na população estudada, devido ao nosso centro se encontrar integrado num hospital em que a Oncologia Pediátrica se dedica maioritariamente ao diagnóstico e tratamento de tumores sólidos e por ser o fármaco de primeira linha no tratamento dos gliomas de baixo grau. Apesar da dessensibilização ser um procedimento não isento de riscos, quando realizada em condições adequadas pode ser uma opção, mesmo em lactentes, apresentando um importante impacto no prognóstico oncológico. Tanto quanto é do conhecimento das autoras esta é a maior série europeia de casos de dessensibilização a quimioterápicos em idade pediátrica, com uma taxa de sucesso de 88% para a carboplatina e de 100% para o metotrexato. São necessários mais estudos para conhecer a verdadeira incidência de RH a antineoplásicos em idade pediátrica bem como estratégia terapêutica mais adequada para esta faixa etária.