Serviços Personalizados
Journal
Artigo
Indicadores
Links relacionados
Compartilhar
Nascer e Crescer
versão impressa ISSN 0872-0754
Nascer e Crescer vol.25 no.2 Porto jun. 2016
ARTIGOS DE REVISÃO / REVIEW ARTICLES
Hemangioma da Infância
Infantile Haemangioma
Maria Armanda PassasI; Marta TeixeiraII
I S. de Pediatria, Hospital Pediátrico Integrado, Centro Hospitalar São João. 4202-139 Porto, Portugal. armanda_passas@hotmail.com
II S. de Dermatologia e Venereologia, Hospital Pedro Hispano, Unidade de Saúde Local de Matosinhos. 4464-513 Senhora da Hora, Portugal. martateixeira.derma@gmail.com
RESUMO
Os hemangiomas infantis são os tumores mais comuns da infância, ocorrendo em cerca de 3 a 10% das crianças com idade inferior a um ano de idade, com predomínio no sexo feminino. Apesar da frequência destes tumores, a sua patogénese permanece pouco compreendida e a melhor abordagem terapêutica é controversa. Têm uma história natural de crescimento rápido durante a primeira infância, seguida de involução gradual, muitas vezes levando à regressão completa. Devido à sua involução espontânea, a maioria dos hemangiomas infantis não requerem qualquer intervenção. No entanto, em 10 a 15% dos casos é necessário tratamento devido às possíveis complicações locais, compromisso fisiológico ou estético a longo prazo elevado ou risco de vida.
Palavras-chave: Hemangioma; Malformações vasculares; Tratamento.
ABSTRACT
Infantile hemangiomas are the most common softtissue tumors of infancy, occurring in approximately 3 to 10 percent of one-year-old children, with predominance in females. Despite the frequency of these tumors, their pathogenesis is not completely understood, and the best approach to their management remains controversial. They have a well-described natural history of rapid growth during early infancy followed by gradual involution, often leading to complete regression. Because of their spontaneous involution, most infantile hemangiomas do not require therapeutic intervention. However, in 10 to 15 % of cases, treatment is necessary because of local complications, life or physiological functioning is threatened or the long-term esthetic risk is too high.
Keywords: Hemangioma; Vascular Malformations; Treatment.
INTRODUÇÃO
Devido à nomenclatura confusa e ausência de uma classificação adequada, o termo hemangioma foi utilizado durante anos de forma indiscriminada, para designar anomalias vasculares distintas quanto à sua etiologia, características clínicas, histopatológicas e prognóstico. Em 1982, Mulliken e Glowacki propuseram uma classificação das lesões vasculares, entretanto revista em 1996 pela International Society for the Study of Vas- cular Anomalies (ISSVA), que pela sua simplicidade e relevância clínica contribuiu para um avanço importante na compreensão das anomalias vasculares.1,2,6 Esta classificação é baseada nas manifestações clínicas, quadro histopatológico e história natural dividindo assim as lesões vasculares em dois grupos: tumores e malformações vasculares.2
Os tumores vasculares são neoplasias dos vasos (proliferação celular) enquanto as malformações vasculares consistem em erros da morfogénese e são classificadas de acordo com o vaso predominante (Quadro 1 e 2).
EPIDEMIOLOGIA
Os hemangiomas são o tumor mais comum na infância, ocorrendo em 3 a 10% das crianças no primeiro ano de vida, no en- tanto, a verdadeira incidência é desconhecida.8,13,15 Existe uma predileção pela raça branca e pelo sexo feminino, com uma razão que varia de 3 a 5:1 até 9:1 no síndrome PHACES.5,8,15 Outros fatores de risco identificados são a prematuridade, muito baixo peso ao nascimento (< 1500g), filhos de mães submetidas a biópsia das vilosidades coriónicas, história familiar de de hemangioma infantil (HI).8,11,16-18 Embora possam ter qualquer localização, os locais mais frequentemente afetados são a cabeça e o pescoço (60%), seguido do tronco (25%) e extremidades (15%).3,5,15
Os hemangiomas podem ser classificados quanto à profundidade da lesão em superficiais (50-60%), profundos (15%) ou mistos (25-35%) e de acordo com a extensão anatómica em focais (67%), segmentares (13%) ou indeterminados. 2,8-11
Os HI segmentares apresentam maior correlação com anomalias estruturais, complicações e necessidade de tratamento.12
ETIOPATOGENIA
Vários estudos têm sido desenvolvidos na tentativa de iden- tificar os fatores causais. No entanto, nenhuma hipótese é suficiente para descrever todas as características dos HI. Estes parecem ser o resultado de uma combinação entre a predisposição genética e a influência do meio ambiente (hipóxia fetal, trauma da pele).11, 19-21
HISTOPATOLOGIA
Atualmente, considera-se que os HI são o resultado de um desequilíbrio na angiogénese que permite a proliferação descontrolada de elementos vasculares.
O aspecto histológico do HI e as alterações identificadas por imunohistoquímica variam em função das diferentes fases evolutiva do tumor. Durante a fase proliferativa, ocorre expansão clonal de células endoteliais, com formação de massas sem uma arquitetura vascular definida, que se organizam progressivamente em capilares. Durante a fase de involução, os capilares regridem e são substituídos por um estroma fibroadiposo.22
O HI é formado por uma mistura complexa de células endoteliais imaturas (CD31+), pericitos (SMA+), células dendríticas (factor XIIIa+), células mesenquimatosas com potencial adipogénico e uma pequena proporção de células germinativas multipotentes (stem cells).23 Adicionalmente podem ser recrutados para o tumor mastócitos e células mielóides.24-26
Durante a fase proliferativa ocorre elevação dos níveis de VEGF e bFGF e as células endoteliais e intersticiais expressam um marcador de proliferação denominado MIB 1.8 As células endoteliais expressam um fenótipo particular: indolamina 2,3 dioxigenase (IDO), LYVE-1, CCR6 e GLUT 1, antigénio Lewis Y (LeY), antigénio FcRγII, CD15. O GLUT 1 proteína transportadora de glicose é também expresso na placenta, tecidos embrionários e fetais e é negativo nas outras patologias vasculares sendo considerado um marcador específico para diagnóstico do hemangioma infantil.27, 28
Durante a fase involutiva ocorre elevação dos marcadores de maturação e ativação de células endoteliais como HLA-DR e ICAM – 1 (CD54), as células endoteliais expressam marcadores de apoptose (caspases) e ocorre infiltração dos tecidos por linfócitos T CD8+ com atividade citotóxica.29 A diferenciação das células mesenquimatosas em adipócitos ocorre nesta fase com a expressão do marcador PPAR (peroxisome proliferator – activated receptor gamma 2).
HISTÓRIA NATURAL
A história natural dos HI compreende três fases: proliferativa, involutiva e involuída.5
Habitualmente, a lesão encontra-se ausente ao nascimen- to, podendo existir uma lesão precursora em 50% dos casos, que se manifesta clinicamente sob a forma de telangiectasias, uma mácula hipopigmentada, eritematosa e/ou equimótica circundada ou não por um halo anémico.5,6,31 Cerca de 90% dos hemangiomas vão tornar-se evidentes no final do primeiro mês de vida.5,15
A fase de crescimento rápido é habitualmente mais pronunciada nos primeiros 3 a 6 meses de vida prolongando-se habitualmente até aos 9 – 12 meses. Nos hemangiomas profundos esta fase pode ser um pouco mais prolongada.32
Após um período quiescente, involui então lentamente, manifestando-se por alteração da coloração na região central da lesão.33
Estima-se uma taxa de regressão aproximadamente 10% por ano. Assim, cerca de 50% das lesões regridem total ou parcialmente aos 5 anos e 90% até aos 9 anos.4,5,34 Em cerca de metade dos casos a involução é praticamente completa; no entanto podem permanecer lesões residuais, como telangiectasias, atrofia, pele redundante ou hipopigmentada, entre outras.5,35
QUADRO CLÍNICO
A apresentação clínica varia de acordo com o tamanho da lesão, localização, profundidade e estadio de evolução. Os he- mangiomas superficiais normalmente estão restritos à derme papilar e reticular, podem ser nodulares ou em placas, de cor vermelho-vivo, são pouco compressíveis e bem delimitados. Os hemangiomas profundos envolvem a derme profunda e o tecido subcutâneo, são lesões nodulares, da cor da pele ou com tonalidade azulada, algumas vezes com telangiectasias na superfície.
COMPLICAÇÕES
A complicação mais frequente é a ulceração, ocorrendo em cerca de 16% dos casos.11,36 Ocorre mais frequentemente nos HI segmentares da face, nos HI com crescimento rápido na fase de proliferação e em localizações mais expostas a traumatismo e fricção, como a região perioral e perineal.36 Esta pode ser bastante dolorosa e complicar-se com hemorragia, sobreinfeção e cicatrização desfigurante.
Determinadas localizações apresentam maior risco de de- senvolver complicações ou podem estar associadas a outras anomalias (Quadro 3).3
Insuficiência cardíaca congestiva é uma complicação rara e pode estar associada a hemangiomas de grandes dimensões ou múltiplos.5,9 É fundamental a pesquisa de lesões em outros órgãos, principalmente no fígado. Pode apresentar ICC por alto débito e hepatomegalia nas primeiras semanas de vida, podendo coexistir anemia e trombocitopenia. É fundamental o tratamento, de modo a reduzir o volume sanguíneo, promovendo assim a regressão do hemangioma.
Hipotiroidismo pode estar associado a hemangiomas grandes.5,9 A enzima 3-iodotironina deiodinase, normalmente pre- sente no cérebro e placenta, pode também ser encontrada nos tecidos do HI. Esta enzima catalisa a conversão da tiroxina em triiodotironina reversa e a conversão da triiodotironina em 3,3-diodotironina, ambas biologicamente inativas. Acredita-se que num hemangioma gigante, devido à sua vascularização e tamanho, ocorra inativação excessiva da hormona tiroideia. Apesar de esta associação ainda não se encontrar totalmente estabelecida, recomenda-se a pesquisa da função tiróideia em todas as crianças com hemangiomas volumosos e/ou hepáticos e o controlo periódico durante a fase proliferativa.
DIAGNÓSTICO DIFERENCIAL
Cerca de 90% das anomalias vasculares podem ser clas- sificadas como hemangiomas ou malformações vasculares apenas com base na história clínica e exame objetivo.5 Dentro dos tumores vasculares o HI deve ser diferenciado de outros tumores mais raros como, o hemangioma congénito, que se apresenta totalmente desenvolvido ao nascimento e pode regredir completamente no primeiro ano de vida denominado de hemangioma congénito rapidamente involutivo (RICH) ou pode apresentar-se como uma mácula telangiectásica persistente denominado hemangioma congénito não involutivo (NICH). Pode ser distinguido do HI pela ausência de reatividade aos antígenos GLUT1 e LeY. O angioma em tufos e o hemangioendotelioma kaposiforme pertencem ao mesmo espectro de lesões, estão presentes ao nascimento e podem ser responsáveis pelo fenó- meno de Kasabach-Merritt (trombocitopenia, anemia hemolítica microangiopática, coagulopatia de consumo). Outras massas e neoplasias podem simular um hemangioma nomeadamente, o angiossarcoma, fibrossarcoma, rabdomiossarcoma, neurofibroma, teratoma, glioma nasal e cisto dermóide.
EXAMES COMPLEMENTARES DE DIAGNÓSTICO
Estudos imagiológicos não invasivos como ecografia com doppler, tomografia computorizada (TC) e ressonância magnética (RMN) são úteis na diferenciação das malformações vasculares. A RMN é o exame de eleição para avaliar a extensão da lesão e a presença de anomalias associadas. Os exames invasivos como a arteriografia devem ser reservados para os casos que requerem embolização.4,5,8
TRATAMENTO
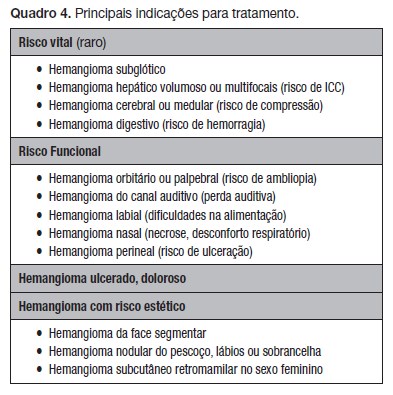
A maioria dos HI tem evolução favorável com regressão espontânea, sendo recomendada uma atitude expectante, com acompanhamento periódico preferencialmente com documen- tação fotográfica e discussão com os cuidadores das vantagens e eventuais desvantagens das opções terapêuticas disponíveis, procurando minimizar o stress psicossocial do doente e família. No entanto, 10 a 15% dos casos, incluindo os HI segmentares, com complicações locais ou em localizações com risco vital, funcional ou estético significativo, necessitam de tratamento (Quadro 4).11,45,46
Propranolol: Desde a primeira publicação em 2008, sobre os efeitos do propranolol nos HI foram publicadas várias séries de casos e estudos que demonstram a eficácia do propranolol, levando ao seu uso generalizado.51,52 O mecanismo de ação permanece ainda pouco conhecido; no entanto, pensa-se que estimula a vasoconstrição dos capilares, diminui a angiogénese das células endoteliais, reduzindo a expressão dos genes VEGF e FGFb e induz a apoptose das células endoteliais. A sua atividade parece ser eficaz, tanto na fase proliferativa como na involutiva. A dose habitualmente utilizada é 2 – 3 mg/Kg/dia, 8/8h por via oral. Dependendo dos centros, a sua administração inicial pode ser efetuada em internamento ou em ambulatório, com dose inicial e avaliação laboratorial e cardíaca variável. Os principais efeitos adversos reportados são bradicardia, hipotensão, hipoglicemia, broncoespasmo (particularmente, nos pacientes com hiperreatividade brônquica) e distúrbios do sono.52-54 Apesar de terem sido publicados estudos que demonstram que a utilização de propranolol nos pacientes com síndrome PHACE é segura, recomenda-se precaução na sua utilização nestes doentes, pois pensa-se que a diminuição da pressão arterial pode diminuir o fluxo sanguíneo nos vasos estenóticos ou displásicos, resultando em hipoperfusão dos territórios envolvidos.55
Recentemente têm surgido estudos sobre a utilização de outros bloqueadores beta com melhor perfil de segurança que o propranolol e a aplicação de formulações tópicas (ex. Timolol) no tratamento de hemangiomas superficiais.
Corticoterapia: A corticoterapia sistémica foi considerada durante anos a terapêutica de eleição no tratamento de HI.46,47 O seu mecanismo de ação permanece pouco esclarecido. Hansan et al. demonstraram que estes estimulam a apoptose por aumento do citocromo b e ao mesmo tempo aumentam a libertação de factores antiangiogénicos por aumento do número de mastócitos.48 A dose preconizada é 2 a 5 mg/kg/dia de prednisolona por via oral, em toma única, durante 6 a 8 semanas. Esta redução deve ser lenta e progressiva.46 A duração total do tratamento deve, se possível, cobrir a fase proliferativa da lesão; no entanto, depende da resposta ao tratamento, idade da criança e complicações da terapêutica. A resposta habitualmente é observada entre a 2ª e 3ª semanas de tratamento e a taxa de resposta varia entre 30 e 60% dos casos.49 Os efeitos colaterais mais comuns são fácies cushingóide, atraso de crescimento, irritabilidade, refluxo gastro esofágico. Outras complicações mais graves (HTA, cardiomiopatia hipertrófica, insuficiência adrenal, etc) são raras. A indicação dos corticóides tópicos e intralesionais é controversa; no entanto, a tentativa de reduzir os efeitos colaterais dos corticóides sistémicos justifica a sua utilização. Habitualmente utiliza-se a triamcinolona (10-20 mg/mL, dose máxima 3-5mg/kg/dose) associada ou não à betametasona (0,5-1mg/kg/dose) no tratamento dos HI perioculares e em lesões focais de pequenas dimensões. Os efeitos laterais variam desde a atrofia cutânea no local tratado, à cegueira por oclusão da artéria da retina.50
Interferão alfa 2a e 2b (IFNα 2a e 2b): devido à acção inibidora da angiogénese, tem sido utilizado na fase proliferativa nos HI resistentes aos corticoides e propranolol. O tratamento deve ser suspenso se não houver resposta ao fim de 1 mês. Os efeitos colaterais mais comuns são febre, irritabilidade e sintomas semelhantes a um quadro gripal. Pode ainda ocorrer neutropenia, anemia e elevação das enzimas hepáticas, habitualmente ligeiras e transitórias. A reacção adversa mais temida, apesar de reversível na maioria dos casos, é a diplegia espástica, relatada em até 20% dos casos e de risco aparentemente proporcional à dose e duração do tratamento.9,46
Vincristina: é um agente com acção inibidora da angiogénese ao interferir com os microtúbulos durante a fase mitótica e in- duzir a apoptose das células tumorais in vitro. Está indicada nos HI complicados que não respondem à terapêutica de primeira linha. Os efeitos adversos incluem fadiga, alopécia, obstipação, dor abdominal, neuropatia periférica, toxicidade hematológica e SIADH.46,56
Laser: Os lasers de CO2 ou Erbium podem ser utilizados nas cicatrizes residuais.46
O laser PDL (pulsed dye laser) tem sido utilizado no tratamento de HI ulcerados e em telangiectasias residuais. Contudo, a sua utilização no tratamento de HI na fase proliferativa permanece controversa. A sua utilização é limitada pela profundidade de penetração do laser e por se tratar de um tratamento doloroso, habitualmente com necessidade de sedação.
Cirurgia: Embora a necessidade de intervenção cirúrgica seja rara durante fase proliferativa, pode ser necessária para reparação de sequelas como presença de tecido residual redundante, atrofia cutânea ou lesões estruturais.46
A embolização é particularmente útil nos hemangiomas hepáticos com ICC.
Radioterapia: muito utilizada no passado, está praticamente abandonada nos dias de hoje devido às sequelas a longo prazo. Tratamento da ulceração: a maioria apenas necessita de cuidados básicos como: limpeza, desinfecção e antibiótico tópico, para prevenir ou tratar infeções. No entanto, pode ser necessário a utilização de antibióticos sistémicos (cefalosporina de primeira geração ou amoxicilina/ ácido clavulânico) nos casos de infeção mais extensa ou resistente às medidas instituídas. A oclusão com vaselina ou aplicação de gel hidrocelular e/ou hidrocolóides tem sido utilizadas com sucesso. Na zona da fral- da é fundamental a utilização de cremes barreira para evitar a maceração e ulceração.5,46
CONCLUSÕES
Hemangiomas são os tumores benignos mais comuns da infância.
Algumas formas de apresentação embora raras podem estar associadas a complicações graves, sendo recomendada a referenciação a um especialista.
80% casos não necessitam de tratamento.
O prognóstico é bom com involução completa até aos 9 anos em 90% dos casos.
REFERÊNCIAS BIBLIOGRÁFICAS
1. Mulliken JB, Glowacki J. Hemangiomas and vascular malformations in infants and children: a classification based on endothelial characteristics. Plast Reconstr Surg. 1982; 69:412-22. [ Links ]
2. ISSVA Classification of vascular anomalies international society for the study of vascular anomalies. [ Links ]
3. Vascular tumors and malformations. Habif. Clinical Dermatology. 5th ed : Mosby, Elsevier, 2009, 23. [ Links ]
4. Morelli G.M. Vascular Disorders. Kliegman. Nelson Textbook of Pediatrics. 19th ed. : Saunders, 2011. [ Links ]
5. Bruckner AL, Frieden IJ. Hemangiomas of infancy. J Am Acad Dermatol. 2003; 48:477-93. [ Links ]
6. Finn MC, Glowacki J, Mulliken JB. Congenital vascular lesions: clinical application of a new classification. J Pediatr Surg 1983; 18: 894-9. [ Links ]
7. Hand JL, Frieden IJ. Vascular birthmarks of infancy: resolving nosologic confusion. Am J Med Genet 2002; 108: 257-64. [ Links ]
8. C. Léauté-Labrèze, S. Prey, K. Ezzedine. Infantile haemangioma: Part I. Pathophysiology, epidemiology, clinical features, life cycle and associated structural abnormalities. 2011, JEADV, Vols. 25, 1245–53. [ Links ]
9. Goldsmith L A, Katz S I, Gilchrest B A, Paller A S, Leffell D J Wolff K. Vascular tumors. Fitzpatricks Dermatology in General Medicine. 7th. ed : MC Graw Hill, 2008, Vol.1. [ Links ]
10. Chiller KG, Passaro D, Fieden IJ. Hemangiomas of infancy. Clinical characteristics, morphologic subtypes and their relationship to race, ethnicity and sex. Arch Dermatol 2002; 138: 1567–76. [ Links ]
11. Haggstrom AN, Drolet BA, Baselga E et al. Prospective study of infantile hemangiomas: clinical characteristics predicting complications and treatment. Pediatrics 2006; 118: 882–7. [ Links ]
12. Drolet BA, Esterly NB, Frieden IJ. Hemangiomas in children. N Engl J Med. 1999; 341:173-81. [ Links ]
13. Kilcline C, Frieden IJ. Infantile hemangiomas: how common are they? A systematic review of the medical literature. Pediatr Dermatol. 2008; 25: 168-73. [ Links ]
14. Hoornweg MJ, Smeulders MJ, van der Horst CM. Prevalence and characteristics of haemangiomas in young children. Ned Tijdschr Geneeskd 2005; 149: 2455–8. [ Links ]
15. Fishman SJ, Mulliken JB. Vascular anomalies: a primer for pediatricians. Pediatr Clin North Am 1998; 45: 1455-77. [ Links ]
16. Garzon MC, Drolet BA, Baselga E, Chamlin SL, Haggstrom AN, Horii K, et al. Hemangioma Investigator Group. Comparison of infantile hemangiomas in preterm and term infants: a prospective study. Arch Dermatol. 2008 Sep;144(9):1231-2. [ Links ]
17. Burton BK, Schulz CJ, Angle B, Burd L. An increased incidence of haemangiomas in infants born following chorionic villus sampling (CVS). Prenat Diagn 1995; 15: 209-14. [ Links ]
18. Drolet BA, Swanson EA, Frieden IJ; Hemangioma Investigator Group. Infantile hemangiomas: an emerging health issue linked to an increased rate of low birth weight infants. J Pediatr. 2008; 153: 712-5. [ Links ]
19. Drolet BA, Frieden IJ. Characteristics of infantile hemangiomas as clues to pathogenesis: does hypoxia connect the dots? Arch Dermatol 2010;146: 1295–9. [ Links ]
20. Lopez Gutierrez JC, Avila LF, Sosa G, Patron M. Placental anomalies in children with infantile hemangiomas. Pediatr Dermatol 2007; 24: 353–5. [ Links ]
21. Chang EI, Thangarajah H, Hamou C, Gurtner GC. Hypoxia, hormones, and endothelial progenitor cells in hemangioma. Lymphat Res Biol 2007; 5: 237–43. [ Links ]
22. Boye E, Yu Y, Paranya G et al. Clonality and altered behaviour of endothelial cells from hemangiomas. J Clin Invest 2001; 107: 745–52. [ Links ]
23. Yu Y, Fuhr J, Boye E et al. Mesenchymal stem cells and adipogenesis in hemangioma involution. Stem Cells 2006; 24: 1605–12. [ Links ]
24. Ritter MR, Butschek RA, Friedlander M, Friedlander SF. Pathogenesis of infantile haemangioma: new molecular and cellular insights. Expert Rev Mol Med 2007; 9: 1–19. [ Links ]
25. Jinnin M, Ishihara T, Boye E, Olsen BR. Recent progress in studies of infantile hemangioma. J Dermatol 2010; 37: 283–98. [ Links ]
26. Khan ZA, Boscolo E, Picard A et al. Multipotential stem cells recapitulate human infantile hemangioma in immunodeficient mice. J Clin Invest 2008; 118: 2592–9. [ Links ]
27. Yu Y, Flint AF, Mulliken JB et al. Endothelial progenitor cells in infantile hemangiomas. Blood 2004; 103: 1373–5. [ Links ]
28. Boye E, Jinnin M, Olsen BR. Infantile hemangioma: challenges, new insights, and therapeutic promise. J Craniofac Surg. 2009; 20: 678-84. [ Links ]
29. Razon MJ, Kraling BM, Mulliken JB, Bischoff J. Increased apoptosis coincides with onset of involution in infantile hemangioma. Microcirculation 1998; 5: 189–95. [ Links ]
30. Mulliken JB, Fishman SJ, Burrows PE. Vascular anomalies. Curr Probl Surg 2000;37:519-84. [ Links ]
31. Esterly NB. Haemangiomas. In: Harper J, Oranje A, Prose N, eds. Textbook of pediatric dermatology. Oxford: Blackwell Science, 2000:997-1016. [ Links ]
32. Brandling-Bennett HA, Metry DW, Baselga E et al. Infantile hemangiomas with unusually prolonged growth phase: a case series. Arch Dermatol 2008; 144: 1632–7. [ Links ]
33. Chang LC, Haggstrom AN, Drolet BA, Baselga E, Chamlin SL, Garzon MC, Horii KA, Lucky AW, Mancini AJ, Metry DW, Nopper AJ, Frieden IJ; Hemangioma Investigator Group. Growth characteristics of infantile hemangiomas: implications for management. Pediatrics. 2008 Aug;122: 360-7. [ Links ]
34. Garzon MC, Frieden IJ. Hemangiomas: when to worry. Pediatric Annals 2000; 29: 58-67. [ Links ]
35. Gampper TJ, Morgan RF. Vascular anomalies: hemangiomas. Plast Reconstr Surg 2002; 110: 572-85. [ Links ]
36. Chamlin SL, Haggstrom AN, Drolet BA, Baselga E, Frieden IJ, Garzon MC, Horii KA, Lucky AW, Metry DW, Newell B, Nopper AJ, Mancini AJ. Multicenter prospective study of ulcerated hemangiomas. J Pediatr. 2007 Dec;151: 684-9, 689-1. [ Links ]
37. Yap EY, Bartley GB, Hohberger GG. Periocular capillary hemangioma: a review for pediatricians and family physicians. Mayo Clin Proc 1998;73: 753-9. [ Links ]
38. Metry D, Heyer G, Hess C, Garzon M, Haggstrom A, Frommelt P, et al. PHACE Syndrome Research Conference. Consensus Statement on diagnostic criteria for PHACE Syndrome. Pediatrics. 2009; 124: 1447-56. [ Links ]
39. Metry DW, Garzon MC, Drolet BA, Frommelt P, Haggstrom A, Hall J, et al. PHACE syndrome: current knowledge, future directions. Pediatr Dermatol. 2009;26: 381-98. [ Links ]
40. Metry DW, Haggstrom AN, Drolet BA, Baselga E, Chamlin S, Garzon M, et al. A prospective study of PHACE syndrome in infantile hemangiomas: demographic features, clinical findings, and complications. Am J Med Genet A. 2006:1;140: 975-86. [ Links ]
41. Orlow SJ, Isakoff MS, Blei F. Increased risk of symptomatic hemangiomas of the airway in association with cutaneous hemangiomas in a beard distribution. J Pediatr 1997;131: 643-6. [ Links ]
42. Girard C, Bigorre M, Guillot B, Bessis D. PELVIS syndrome. Arch Dermatol 2006; 142: 884–8. [ Links ]
43. Stockman A, Boralevi F, Taı¨eb A, Leaute´-Labre`ze C. SACRAL syndrome: spinal dysraphism, anogenital, cutaneous, renal and urologic anomalies, associated with an angioma of lumbosacral localization. Dermatology 2007; 214: 40–5. [ Links ]
44. Horii KA, Drolet BA, Frieden IJ, Baselga E, Chamlin SL, Haggstrom AN, et al. Hemangioma Investigator Group. Prospective study of the frequency of hepatic hemangiomas in infants with multiple cutaneous infantile hemangiomas. Pediatr Dermatol. 2011;28: 245-53. [ Links ]
45. Frieden IJ, Haggstrom AN, Drolet BA, Mancini AJ, Friedlander, SF, Boon L, et al. 2005. Infantile hemangiomas: Current knowledge, future directions. In Proceedings of a research workshop on infantile hemangiomas;7–9, 2005, Bethesda, Maryland. Pediatr Dermatol 22: 383–406. [ Links ]
46. C. Léauté-Labrèze,S. Prey, K. Ezzedine Infantile haemangioma: Part II. Risks, complications and treatment. JEADV 2011, 25, 1254–60. [ Links ]
47. Kristen E. Holland, Beth A. Drolet, Infantile Hemangioma. Pediatr Clin N Am. 2010; 57: 1069–83. [ Links ]
48. Hasan Q, Tan ST, Gush J et al. Steroid therapy of a proliferating hemangioma: histochemical and molecular changes. Pediatrics 2000;105: 117-20. [ Links ]
49. Bennet ML, Fleischer AB, Chamlin SL, Frieden IJ. Oral corticosteroid use is effective for cutaneous hemangiomas. An evidence based evaluation. Arch Dermatol 2001;137: 1208-13. [ Links ]
50. Shorr N, Seiff SR. Central retinal artery occlusion associated with periocular corticosteroid injection for juvenile hemangioma. Ophtalmic Surg 1986; 17: 229–31. [ Links ]
51. Léauté-Labrèze C, Dumas de la Roque E, Hubiche T, Boralevi F, Thambo JB, Taïeb A. Propanolol for severe hemangiomas of infancy. N Engl J Med. 2008;358: 2649-51. [ Links ]
52. Price CJ, Lattouf C, Baum B, McLeod M, Schachner LA, Duarte AM, Connelly EA. Propranolol vs corticosteroids for infantile hemangiomas: a multicenter retrospective analysis. Arch Dermatol. 2011;147(12):1371-6. [ Links ]
53. Léauté-Labrèze C, Taïeb A. Effecacité des bêtabloquants dans les hémangiomes capillaires infantiles: signification physiopathologique et conséquences thérapeutiques. Ann Dermatol Venereol. 2008;135: 860-2. [ Links ]
54. Sans V, Dumas de la Roque E,Berge J, et al. Propranolol for Severe Infantile Hemangiomas: Follow-Up Report. Pediatrics 2009; 124: 423. [ Links ]
55. Brain perfusion SPECT in Patients with PHACES Syndrome under propranolol treatment Eur J Pediat Surg 2012; 22 :54-9. [ Links ]
56. Enjolras O, Breviere GM, Roger G, Tovi M,Pellegrino B, Varotti E et al. Traitement par vincristine des hemangiomes graves du nourrisson. Arch Pediatr 2004;11: 99-107. [ Links ]
Endereço para correspondência
Maria Armanda Passas
Serviço de Pediatria
Hospital Pediátrico Integrado, Centro Hospitalar São João
Alameda Professor Hernâni Monteiro, 4202-139 Porto
Email: armanda_passas@hotmail.com
Recebido a 12.08.2015 | Aceite a 11.01.2016














