Introdução
O acidente vascular cerebral (AVC) e caracterizado por um defice neurologico decorrente de uma lesao aguda, de causa vascular, do sistema nervoso central (SNC).1
A dor e uma sequela frequentemente subvalorizada, existindo em aproximadamente 38% dos doentes no momento do AVC, mas em 46% dos casos surge seis meses depois do evento agudo.2 A dor pós-AVC pode ser categorizada em dois tipos: i) dor desencadeada por mecanismos periféricos, como a dor secundária a espasticidade, a omalgia e outros quadros de dor musculoesquelética; e ii) dor central (DC), sobre a qual se debruça esta revisão.3-5
Processo de revisão da literatura
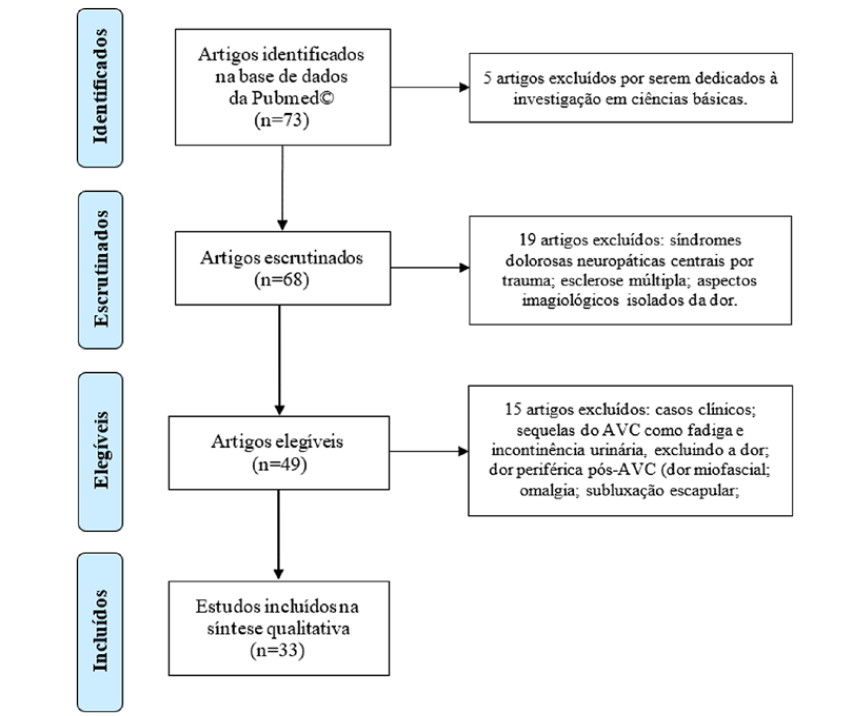
Foram pesquisados artigos na PubMedc publicados de dezembro 2009 a dezembro 2019, em Português ou Inglês, com texto completo, relatando investigação humana em adultos, utilizando os termos “central AND pain AND post stroke”. Foram identificados 73 artigos, sendo excluídos cinco. Dos 68 escrutinados, foram excluidos 19. Dos 49 elegíveis, foram excluídos 15. Foram incluidos 33 artigos nesta revisão narrativa (Fig. 1).
Definição de Dor Central após Acidente Vascular Cerebral
A DC pós-AVC e uma síndrome dolorosa neuropática que ocorre como consequência direta de uma lesão isquemica do SNC, afetando a área corporal correspondente a lesão cerebrovascular.1,6A DC e caracterizada por dor e alterações sensitivas como alodinia e hiperalgesia. Como se pode verificar adiante, tratando-se de um diagnóstico de exclusão, outras causas de dor neuropática periférica, nocicetiva ou psicogénica devem ser excluídas.7
Prevalência da Dor Central após Acidente Vascular Cerebral
O maior estudo de prevalência de DC pós-AVC, o PRo-FESS (Prevention Regimen for Effectively avoiding Second Stroke)- um estudo aleatorizado e controlado que incluiu 695 centros, 35 países e 20 332 doentes, dos quais 15 754 elegíveis, - mostrou que 10,6% doentes desenvolveu DC pós-AVC.6 Outras investigações revelaram que a DC ocorre em aproximadamente 5%-11% dos doentes que sofreram um AVC, aumentando esta prevalência para 18% nos casos com deficiencia sensitiva, ate 50% nos doentes com AVC talamico.2,8Não existem diferenças de prevalência em doentes que sofreram AVC isquémicos ou hemorrágicos (associados a hemorragia intracerebral ou subaracnoideia).3 Outros estudos encontraram prevalências de DC pós-AVC mais elevadas, variando entre 25% a 42%.9 Em Portugal existem poucos estudos sobre a prevalência da DC pós-AVC.
Os doentes mais jovens (idade media de 60 anos), do sexo feminino (62% dos casos de DC pós-AVC), fumadores, com antecedentes de depressão e com AVC de maior gravidade, parecem ter uma maior predisposição para o desenvolvimento de DC.2,6,10,11
Apresentação Clínica da Dor Central após Acidente Vascular Cerebral
É consensual que a DC pós-AVC e uma sindrome que pode passar desapercebida, a menos que os sintomas sejam ativamente questionados pelo médico assistente.12 Note-se que as alterações neurológicas concomitantes (como afasia, síndrome de negligência ou demência) podem dificultar a identificação e caracterização da DC pós-AVC.4
A DC pós-AVC não tem sinais ou sintomas patognomónicos.7 A dor tem características semelhantes as que costumam existir nas síndromes dolorosas neuropáticas periféricas, sendo geralmente descrita como uma sensação de queimadura, facada, picada, aperto ou, menos comummente, como um choque elétrico, frio doloroso ou prurido (considerado equivalente a dor).1,2,13A DC distribui-se mais frequentemente nas extremidades superiores, podendo atingir ainda as extremidades inferiores, a face, ou o hemicorpo completo; localizando-se sempre no lado afetado pelo AVC.2,13
Além das características acima descritas, a DC acompanha-se, em aproximadamente 85% dos doentes, de alodinia (sensacao de dor em resposta a um estímulo não doloroso) e/ou hiperalgesia (sensação de dor exagerada em resposta a
um estímulo doloroso de reduzida intensidade).14
A intensidade da dor e variável, agravando com estímulos externos ou internos, como movimento, toque, frio ou stress emocional, aliviando com o repouso e as atividades distrativas.1 A DC pode apresentar-se como:
A DC pós-AVC, sobretudo se subtratada ou refrataria ao tratamento, está ainda associada a um maior declinio cognitivo e funcional11; a alterações de humor (em 87% dos doentes), ao aumento do risco de depressão grave e suicídio4; e a perturbações do sono (em 50% dos doentes).3 Tem, portanto, um impacto negativo na qualidade de vida destes doentes, prejudicando ainda a sua adesão e o seu desempenho nos programas de reabilitação.15
Diagnóstico da Dor Central após Acidente Vascular Cerebral
A historia clinica e exame objetivo, com especial enfoque na completa avaliação da sensibilidade dolorosa, revelam-se essenciais para o diagnóstico de DC. Os exames complementares, como a ressonância magnética nuclear, auxiliam na confirmação e localização da lesão do SNC. Outros exames, como a eletroneuromiografia, podem ajudar no diagnóstico diferencial com a dor neuropática de origem periférica.7
Recentemente, o grupo de estudo de taxonomia da dor da “American Pain Society” descreveu seis critérios cumulativos que devem estar presentes para estabelecer o diagnostico de DC pos-AVC, a saber:16
1) historia clinica fortemente sugestiva de AVC (com presenca de défice neurológico de causa cerebrovascular que persistiu >24 horas) ou existência de exames complementares documentando um AVC;
2) dor contínua ou recorrente após um AVC, com início da dor após o evento agudo ou no periodo ate aos 12 meses pos-AVC;
3) duração da dor de três meses, pelo menos;
4) a dor e descrita na área do corpo afetada pela lesão do AVC;
5) a dor esta associada a alterações sensoriais, com uma distribuição plausível do ponto de vista neuroanatómico, com presença de, pelo menos, um sinal sensorial positivo (por exemplo, alodinia dinâmica mecânica ou evocada pelo frio) ou um sinal sensorial negativo (por exemplo, limiares aumentados perante o frio ou o calor, ou sensação diminuida ao toque, picada ou estimulo térmico);
6) não há outro diagnóstico que possa explicar melhor a presença de dor.
Fisiopatologia da Dor Central após Acidente Vascular Cerebral
A DC pós-AVC foi inicialmente designada como sindrome de Dejerine-Roussy, em honra dos neurologistas franceses que descreveram, inicialmente, o quadro de DC decorrente de AVC talâmicos. Por este motivo, esta DC é também denominada de dor talâmica.3 O talâmo desempenha um papel substancial em alguns doentes com DC, seja como gerador de dor, seja pelo processamento anormal da via de dor ascendente.7 A excitabilidade aumentada dos núcleos talâmicos pode significar uma adaptação inadequada da plasticidade homeostática devido a perda de aferências ascendentes do feixe espinhotalâmico.7 A desaferenciacao, a perda de neurónios inibidores gabaergicos e a ativação microglial foram sugeridas como contribuintes das mudanças talâmicas ocorridas após uma lesao do SNC.7 Contudo, e hoje aceite que uma lesão em qualquer componente do feixe espinhotalamocortical pode causar DC pós-AVC, sendo o enfarte talâmico responsavel por apenas 25%-33% dos casos.3,4Esta via e responsável pela transmissão dos estímulos de dor e temperatura, pelo que a ausência de alterações na sensação algica e/ou termica praticamente exclui a DC.3,4A perda sensitiva associada a lesões do feixe espinhotalamocortical não é suficiente para o surgimento de DC.3,4Diversas teorias procuram explicar esta síndrome.
No SNC existe um equilíbrio entre os sistemas de facilitação e de inibiçao da dor, incluíndo interações entre os núcleos do tronco cerebral (o núcleo ventromedial da medula e a substância cinzenta periaquedutal) e a medula espinhal e os
circuitos supraspinhais talamocorticais.7 A “teoria da desinibição” defende que uma lesão ao nível do feixe espinhotalâmico lateral pode causar uma desinibição do espinhotalamico medial, ao interromper a sinalização inibitória entre estas duas vias, dependente do ácido gama-aminobutirico, com consequente dor.3,10Após um AVC, as alterações plásticas das vias somatossensoriais e de dor ocorrem possivelmente no sistema lateral “discriminatório” da dor.7
A “teoria da hipersensibilidade” defende que a desenervação dos axónios do feixe espinhotalâmico, na sequência de um AVC, resulta na facilitacao da ativação neuronal, causando dor.3 Uma lesão do SNC origina alteracoes anatómicas, neuroquímicas, excitotoxicas e inflamatórias que podem desencadear um aumento da excitabilidade neuronal.7 Combinada com uma perda de inibição e maior facilitação, esta excitabilidade aumentada pode implicar uma sensibilização central que pode explicar a cronicidade da dor.7 Este mecanismo e apoiado pelo fato de muitos farmacos disponiveis para o tratamento da DC, em parte, diminuam a hiperexcitabilidade neuronal.12,17A dor espontanea que ocorre na dor pós-AVC
pode estar associada a hiperexcitabilidade ou a descargas espontâneas em neurónios desaferenciados localizados no talâmo ou no cortéx.7
Outra hipótese aventada para a dor pós-AVC reside nas alterações funcionais do feixe espinhotalâmico. As perturbações das sensações dolorosa e térmica são habituais em doentes com DC pos-AVC, estando normalmente associadas a uma lesao do feixe espinhotalamico.7 As hipersensibilidades a picada e aos estímulos térmicos (o frio, particularmente) são comuns em doentes com dor pós-AVC, o que pode indicar uma hiperexcitabilidade e uma atividade contínua do feixe espinhotalâmico.7
Em suma, um desequilibrio entre os mecanismos facilitadores e inibidores das vias espinhotalamicas e talamocorticais pode culminar no surgimento de DC.10 Porem, mais estudos são necessários para fortalecer a evidência dos fenómenos fisiopatológicos que sustentam a dor pós-AVC.1
Tratamento da Dor Central após Acidente Vascular Cerebral
A DC pós-AVC e dificil de tratar. Estima-se que menos de 25% dos doentes recebe um tratamento adequado.9
Na prática clínica, o tratamento implica frequentemente um processo de tentativa-erro ate que o alívio sintomático seja atingido, com recurso a combinações de diferentes fármacos e a medidas nao farmacológicas.
O controlo completo da dor e, contudo, raramente obtido.7
Torna-se, portanto, de elevada importância informar o doente que o alívio sintomático poderá ser alcancado gradualmente, consoante o ajuste posológico dos fármacos. É também fundamental alertar o doente que o intuito do tratamento é reduzir a dor e o seu impacto na qualidade de vida, podendo não ser possível erradicar completamente os sintomas.17 Efetivamente, uma ligeira redução na intensidade da dor (dois pontos ou 30% numa escala de autoavaliação numérica de 0-10) está relacionada com uma melhoria clinicamente significativa, independentemente da intensidade inicial da dor.18
A abordagem destes doentes deve incluir o tratamento dos sintomas e comorbilidades associados à DC, como as perturbações do humor e do sono.17 Uma intervenção psicossocial pode ser considerada junto destes doentes, estando associada ao desenvolvimento de competências para lidar com a dor, a reversão de comportamentos perniciosos (como a inatividade) e a uma melhor adesão ao tratamento analgésico.3
Farmacoterapia
1. ANTIDEPRESSIVOS
A amitriptilina, um antidepressivo triciclico, e considerada um fármaco de primeira linha no tratamento da DC, com a necessidade de uma titulação lenta até, pelo menos, 75 mg/dia. Os efeitos adversos anticolinérgicos são frequentemente pouco tolerados pelos doentes mais idosos.18,19Entre os efeitos adversos destacam-se a xerostomia, a retenção urinária e a obstipação; mas devem ser considerados outros efeitos potencialmente mais graves, tais como a hipotensão
ortostática e as alterações do ritmo cardíaco.19,20
Uma possível alternativa reside nos inibidores da recaptação de serotonina e noradrenalina, tais como a duloxetina, que apesar de nao terem ainda a sua eficácia estabelecida na DC, poderao ser uma opção mais segura no contexto de doença cardíaca associada.7
Os inibidores seletivos de recaptação da serotonina, de uma forma geral, não parecem ser eficazes no alivio da DC.3
Excecionalmente, um estudo revela uma eficacia moderada associada a fluvoxamina (125 mg/dia), caso seja iniciada no ano procedente ao AVC.21~
2. ANTICONVULSIVANTES
Nesta classe farmacolgica incluem-se diferentes fármacos que são adjuvantes do tratamento da dor e que atuam através de vários mecanismos, mormente a redução da hiperexcitabilidade neuronal.22
O papel da pregabalina não é consensual, sendo os resultados escassos ou conflituosos.18,21,23Num estudo multicêntrico, aleatorizado, duplamente cego, controlado com placebo e paralelo, de 13 semanas, com doentes com DC pós-AVC, foram administradas doses de 150-600 mg/dia de pregabalina e constatou-se que as reduções da dor não diferiram significativamente entre os grupos.24 A pregabalina estava associada a uma melhoria do sono e da ansiedade, existindo uma impressão clínica global de melhoria com este anticonvulsivante.24
O uso de lamotrigina é controverso. Por um lado, há estudos que associam a lamotrigina a uma melhoria clinicamente significativa da DC, em doses de 200-400 mg/dia, sendo geralmente bem tolerada pelos doentes.18 Por outro lado, numa revisao Cochrane da literatura que incluiu 11 estudos e 1511 participantes, mas apenas com um estudo sobre DC pós-AVC, o papel da lamotrigina foi considerado pouco significativo no tratamento da dor neuropática.25
O papel do levetiracetam tambem nao e unanime.17,26Numa revisão Cochrane que incluiu seis estudos, com 344 doentes com diferentes tipos de dor neuropática, incluindo a DC pos-AVC, o levetiracetam (2000-3000 mg/dia) não foi superior ao placebo no tratamento da dor, durante 4-14 semanas de seguimento. O levetiracetam esteve associado a um aumento dos efeitos adversos e a suspensão do fármaco devido a efeitos intoleráveis.27
A carbamazepina não é eficaz na DC pos-AVC quando comparada com a amitriptilina ou o placebo.17,26Da mesma forma, o topiramato não revelou ser eficaz no alívio sintomatico da DC.17,26A gabapentina, que é amplamente utilizada com eficácia noutras síndromes neuropáticas, carece de mais investigação no ambito da DC.19,21O mesmo se aplica a outros anticonvulsivantes, como a fenitoina ou a zonisamida, para os quais a evidencia e escassa ou conflituosa.18,21
3. OUTROS FÁRMACOS
Os anti-inflamatórios não-esteróides e os analgésicos não opióides não parecem ser eficazes no alívio da DC.3,7,17
Apesar de os opióides também serem considerados ineficazes no tratamento da DC, os estudos revelam que a morfina poderá ser útil no alivio da alodinia e das alterações de perceção térmica associadas a DC; todavia, nem sempre o
tratamento com morfina e bem tolerado pelos doentes.3,7,17
Relativamente a corticoterapia, apenas um pequeno estudo retrospetivo relatou uma reducao da DC com um curso de metilprednisolona (24 mg no primeiro dia, decrescendo 4mg/dia subsequentemente); contudo, não existem estudos prospetivos que apoiem este dado.11,21
A lidocaína intravenosa e a cetamina poderão também ser eficazes no alívio agudo da DC; todavia, apenas alguns casos pontuais suportam esta evidência, sendo necessários mais estudos para concluir a sua eficácia na DC.11
Adicionalmente, note-se que não existe atualmente evidência que favoreca a profilaxia farmacológica da DC pós-AVC.11
Tratamento Não Farmacológico
1. CIRURGIA
Dada a refratariedade da DC, vários procedimentos cirúrgicos ou radiocirúrgicos foram propostos na tentativa de interromper a sinalização nocicetiva patológica, nomeadamente:
rizotomia, simpatectomia, talamotomia, lobotomia frontal, cingulotomia, entre outros.17,18A eficácia destes procedimentos na DC pós-AVC não foi demonstrada, estando associados quer a uma recidiva da dor ao fim de meses a anos, quer a uma morbimortalidade significativa, pelo que a sua utilização não é atualmente recomendada.17,18
2. NEUROESTIMULAÇÃO
Várias terapias de neuroestimulação foram avaliadas para o tratamento de casos resistentes de DC pós-AVC.
A estimulação cerebral profunda e um método de neuromodulação invasivo que, com a implantação de elétrodos no talâmo ventral posterior (sensorial), na cápsula interna ou na substância cinzenta periventricular, permite aliviar a DC em 25% a 70% dos doentes.3,7,17Os resultados sao, contudo, bastante variáveis entre os doentes e menos satisfatórios do que na dor de origem periférica.3,7,17,28
A estimulação da medula espinhal e um método de neuromodulação invasivo que pode reduzir a DC, sobretudo em doentes jovens e em casos de AVC nao-talâmico, sendo que o alívio da dor pode permanecer por mais de 12 meses.29
A estimulação do cortéx motor e também um método invasivo, com eficacia reportada de cerca de 50% na DC, aumentando para 77% se os potenciais evocados somatossensoriais forem utilizados para confirmar a correta colocação
dos elétrodos.11 Noutros estudos, com seguimentos variando de doze meses a seis anos, mais de metade dos doentes (54%) teve uma redução da dor de 50%-80%, sendo os resultados superiores nas sndromes talâmicas.30
A estimulação do cortex somatossensitivo (giro pós-central) não está associada a um alívio da DC.14
A estimulação supraespinhal, apesar da sua indicação para a DC e para a nevralgia do trigemeo em quadros refratários, carece de mais estudos para documentar a sua utilização.28 Os mecanismos subjacentes a este efeito benéfico não estão totalmente esclarecidos, podendo estar relacionados com um aumento do fluxo sanguíneo e/ou um aumento da libertação de opióides endógenos em várias áreas cerebrais, incluindo o talâmo, a insula, o sistema limbico, entre outros.1,7,31Estes são responsáveis pela perceção da dor e pelos aspetos emocionais associados.
Considerando o benefício e os riscos, todos os metodos invasivos atrás mencionados não estão atualmente recomendados, devendo ser reservados para a última linha de tratamento, em casos selecionados e efetuados em centros especializados.17
Em alternativa, sao propostos os metodos nao invasivos e mais seguros, tais como a estimulacao transcraniana por corrente continua e a estimulação transcraniana magnética.
Estas, quando dirigidas ao cortéx motor primario, estão associadas a uma melhoria clinicamente significativa da DC, por curto a médio prazo.32,33Adicionalmente, alguns autores sugerem que o resultado da terapia com estimulação transcraniana magnética do cortéx motor pode ser usado como preditor da eficácia da estimulação (invasiva) do cortéx motor.7,31Note-se que mais estudos são necessários para determinar a viabilidade clínica destas técnicas e para estabelecer os seus modos de execução, que são muito variáveis entre os estudos publicados, nomeadamente o local exato de estimulação, a frequência e a duração do estímulo, a frequencia das sessoes, entre outros.33
Conclusão
A DC é uma possível sequela do AVC e tem um impacto importante na qualidade de vida dos doentes. A DC pós-AVC é frequentemente subdiagnosticada e de difícil tratamento, implicando uma abordagem flexível e individualizada, combinando metodos farmacologicos e nao farmacológicos. É necessária mais evidência científica de modo a clarificar a fisiopatologia subjacente, melhor definir os critérios de diagnóstico, e permitir um adequado controlo sintomático e tratamento da DC pós-AVC.