Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Revista Portuguesa de Pneumologia
versão impressa ISSN 0873-2159
Rev Port Pneumol v.16 n.3 Lisboa jun. 2010
Reacções adversas aos antibacilares em doentes internados: Gravidade e factores de risco
Ana Sofia Vilariça1, Nelson Diogo2, Mota André2, Jaime Pina3
1 Interna do Internato Complementar de Pneumologia/Resident, Pulmonology
2 Assistente Hospitalar Graduado de Pneumologia/Specialist, Consultant, Pulmonology
3 Chefe de Serviço Hospitalar de Pneumologia e Director do Serviço de Pneumologia III do Hospital de Pulido Valente, Lisboa/Head, Hospital Pulmonology Unit and Director, Pulmonolgy Unit III, Hospital de Pulido Valente, Lisbon
Serviço de Pneumologia III
Hospital de Pulido Valente, Centro Hospitalar Lisboa Norte, Lisboa
Resumo
Introdução: Atendendo às características do Mycobacterium tuberculosis (MT), o tratamento da tuberculose (TB) é feito com uma associação de vários fármacos, por um período de tempo alargado (≥ a 6 meses), cada um com potencial para provocar reacções adversas (RA). Estas podem acompanhar-se de significativa morbilidade e comprometer o tratamento da TB.
Objectivos: Determinar a incidência, a gravidade e os factores de risco das principais RA induzidas pelos antibacilares, em doentes internados com TB em tratamento.
Material e métodos: Análise retrospectiva dos registos clínicos dos doentes internados no Serviço de Pneumologia III do Hospital de Pulido Valente com tuberculose activa, medicados com antibacilares, durante o período de Abril de 1999 a Julho de 2007. Foram registadas as RA que resultaram em modificação ou descontinuação do tratamento ou que foram a causa de internamento. As características demográficas e os dados clínicos dos doentes foram usados como variáveis independentes. A relação entre variáveis independentes e a frequência e gravidade das RA foi feita através de uma análise multivariada, utilizando um modelo de regressão logística. Os dados foram analisados pelo teste t de Student, one-way ANOVA e regressão logística. A aplicação utilizada para a análise estatística foi o programa SPSS (Statistical Package for the Social Sciences), versão 15.0.
Resultados: Dos 1400 doentes internados e tratados por TB activa entre 1999 e 2007, 175 doentes (12,5%), 118 homens e 57 mulheres, apresentaram pelo menos uma RA induzida pelos antibacilares, num total de 192 eventos. A hepatotoxicidade foi a RA mais prevalente (83/47,4%), seguindo-se a reacção cutânea (55/31,4%) e a intolerância gastrintestinal (24/13,7%). Em 76 doentes (43,4%) as RA causaram o prolongamento do internamento. Constatou-se que a demora média do grupo de doentes com RA foi de 58,4 dias. Esta demora média apresentou diferenças estatisticamente significativas (p< 0,001) em relação à demora média dos doentes sem RA, que foi de 26 dias. Os fármacos mais implicados foram a isoniazida (62,2%) e a rifampicina (51,9%). Dos 134 casos em que foi possível caracterizar a gravidade das RA, em 106 casos (79%) houve necessidade de suspensão do fármaco. A relação causal fármaco-RA foi definitiva em 23 casos (17%). Dos 13 doentes (9,6%) que faleceram, em 6 (4,4%) a RA esteve directamente implicada na causa de morte. A ocorrência de qualquer RA foi associada ao alcoolismo (risco relativo [RR] de 3,0; 95% de intervalo confiança [IC], 1,1-7,9) e aos níveis de CD4 < 350 células/ mm3 ([RR] de 2,6 ; [IC], 1,4-5). No modelo preditivo, as reacções hepáticas foram associadas à ocorrência de hepatites virais B e/ou C ([RR] de 2,5; [IC], 1,2-5,1) e aos níveis de CD4 < 350 células/mm3 ([RR] de 5,5; [IC], 1,6-18,6).
Conclusões: Os antibacilares estão associados a um número significativo de RA que podem condicionar grande morbilidade, prolongamento do internamento e mesmo alguma mortalidade. Os nossos resultados mostram que o alcoolismo e os níveis de CD4 <350 células/mm3 foram significativamente associados a um elevado risco de ocorrência de qualquer RA e que as hepatites B e C e os níveis de CD4 < 350 células/mm3 foram associados, também de forma significativa, ao risco de RA hepáticas.
Palavras-chave: Tuberculose, reacção adversa (RA), antibacilares, infecção VIH.
Adverse reactions to antituberculosis drugs in in-hospital patients: Severity and risk factors
Abstract
Introduction: Given Mycobacterium tuberculosis’s characteristics, the treatment of tuberculosis (TB) infection is administered over a long period of time (for six months or more) with a combination of several drugs which could cause adverse reactions (AR). These can cause significant morbidity and compromise tuberculosis treatment regimens.
Aim: To determine the incidence and severity of and risk factors for major adverse reactions to antituberculosis drugs in in-hospital patients treated for active tuberculosis.
Methods: Retrospective analysis of clinical records of patients admitted to Pulido Valente Hospital (Pulmonology Unit III) with active TB treated with anti-tuberculosis agents April 1999 to July 2007. Adverse reactions resulting in modification or discontinuation of treatment or hospital admission were recorded. Patients’ demographic characteristics and clinical data were used as independent variables. The relationship between independent variables and the frequency and severity of AR was studied using multivariate analysis using a logistic regression model. The data were analysed using the Student t test, one-way ANOVA and logistic regression. Statistical analysis was performed using the SPSS (Statistical Package for the Social Sciences) version 15.0.
Results: We recorded 1400 in-hospital patients treated for active TB 1999 to 2007, of which 175 patients (12.5%), 118 male and 57 female, had at least one AR induced by antituberculosis agents, to a total of 192 events. Hepatotoxicity was the most prevalent AR (83/47.4%), followed by skin reactions (55/31.4%) and gastrointestinal intolerance (24/13.7%). In 76 patients (43.4%) AR caused prolonged hospital stay. Statistically significant differences (p<0.001) were observed in the average hospital stay (58.4 days for patients with AR and 26 days for patients without AR). Isoniazid (62.2%) and rifampicin (51.9%) were the most frequently implicated drugs. It was possible to characterise the AR severity in 134 cases. In 106 cases (79%) AR resulted in discontinuation of the drug. The relationship between drug and AR was definitive in 23 cases (17%). Of the 13 patients (9.6%) who died, AR was directly implicated in the cause of death in six (4.4%). AR were associated with alcoholism (relative risk [RR] 3.0; 95% confidence interval [CI] 1.1-7.9) and CD4 levels <350 cells/mm3 (RR 2.6; CI 1.4-5). In the predictive model, hepatic reactions were associated with viral hepatitis B and/or C (RR 2.5, CI; 1.2-5.1) and that CD4 levels <350 cells/mm3 (RR 5.5; CI 1.6-18.6).
Conclusions: Antituberculosis drugs are associated with a significant number of AR that can cause significant morbidity, prolonged hospital stay and even death. Our results show that alcoholism and levels of CD4 <350 cells/mm3 were significantly associated with a high risk of AR and hepatitis B and C and levels of CD4 <350 cells/mm3 were also significantly associated with hepatotoxicity.
Key-words: Tuberculosis, adverse reaction (AR), antituberculosis drug, HIV infection.
Introdução
A tuberculose continua a ser a doença infecciosa de mortalidade e morbilidade no mundo em vias de desenvolvimento. Os esquemas com antibacilares utilizados no tratamento da tuberculose são eficazes e curativos, mas podem causar reacções adversas (RA), que não são desprezíveis.
Vários factores favorecem o aparecimento de RA aos antibacilares.
A prioridade nos programas de prevenção e controlo da tuberculose é a identificação e o tratamento dos doentes com tuberculose activa1. O aumento de casos tratados conduz, inevitavelmente, a um aumento das reacções aos fármacos utilizados.
As características do Mycobacterium tuberculosis têm implicações terapêuticas, fazendo com que as regras para o tratamento da tuberculose sejam diferentes das indicadas para as infecções habituais. É necessário recorrer a um esquema de tratamento com associações de múltiplos fármacos, de forma a evitar falências de tratamento, recaídas, e a prevenir o desenvolvimento de resistências. Na poliquimioterapia é necessário ter em conta três aspectos fundamentais: 1) o potencial de cada fármaco individualmente para provocar RA; 2) a farmacocinética de alguns fármacos, que facilita o aparecimento de reacções a outros, administrados concomitantemente; 3) a dificuldade em determinar o fármaco implicado na RA.
A necessidade de tratamento prolongado, com duração igual ou superior a 6 meses, é outro factor que favorece o desenvolvimento de RA. Por outro lado, a infecção pelo VIH, reconhecida como o principal factor de risco para a aquisição de tuberculose activa, aumenta a incidência de RA2. Além disso, um dos fármacos de primeira linha para o tratamento da TB – rifampicina – tem sido implicado no aparecimento de RA nos doentes infectados pelo VIH, independentemente do grau de imunossupressão, da apresentação clínica da tuberculose e da presença, ou não, de patologia oportunista associada3.
As RA mais frequentemente observadas com os principais antibacilares são as seguintes: a neuropatia periférica e a hepatotoxicidade associadas à isoniazida; as reacções gastrintestinais e a hepatite tóxica desencadeadas pela rifampicina, potenciadas pela associação com a isoniazida; a hiperuricemia e a toxicidade hepática (que é rara mas pode ser fatal) provocadas pela pirazinamida; a nevrite óptica associada ao etambutol e a ototoxicidade à estreptomicina4. Na prática clínica, a RA mais frequente com que nos deparamos é a intolerância gástrica. No entanto, as RA mais problemáticas e que obrigam à suspensão dos esquemas terapêuticos são as reacções cutâneas de hipersensibilidade e as hepáticas.
As RA aos fármacos antituberculosos podem causar morbilidade significativa e comprometer os regimes terapêuticos, conduzindo à sua modificação ou interrupção, ou ao internamento dos casos complicados. Por isso, é fundamental o conhecimento das principais RA e o seu reconhecimento precoce, para diminuir a morbilidade e mortalidade associadas5.
A amplitude e as características das RA não são bem conhecidas devido à escassez de registo e notificação das mesmas. Assim, este trabalho teve como objectivos: 1) determinar a incidência e caracterizar as principais RA aos antibacilares em doentes internados com tuberculose activa em tratamento; 2) determinar os principais factores de risco; 3) contribuir para o conhecimento mais aprofundado das principais RA, a fim de se efectuar uma correcta abordagem, monitorização e controlo das mesmas.
Material e métodos
Os autores efectuaram um estudo retrospectivo dos doentes admitidos no Serviço de Pneumologia III do Hospital de Pulido Valente, entre Abril de 1999 e Julho de 2007, com o diagnóstico de tuberculose activa em tratamento. Procedeu-se à revisão dos registos clínicos dos doentes, através da consulta de uma base de dados em Microsoft Office Access 2003, desenvolvida pelo Serviço.
Da totalidade dos doentes com RA aos antibacilares foram avaliados os seguintes parâmetros epidemiológicos: sexo, distribuição etária, raça, estatuto de imigrante, país de origem, classificação da Organização Mundial de Saúde (OMS), coinfecção pelo VIH e seus factores de risco, hábitos etílicos, localização da doença e comorbilidades significativas para reacções de hepatotoxicidade. Os registos existentes permitiram caracterizar os tipos de RA e a sua gravidade, a demora média, o fármaco suspeito implicado, a relação causal fármaco-RA, as consequências terapêuticas (suspensão definitiva/reintrodução do fármaco) e a evolução durante o internamento dos doentes com RA aos fármacos antibacilares.
De acordo com a classificação de registo e notificação da TB, proposta pela OMS, distinguem-se os seguintes grupos: casos novos e retratamentos (por recidiva, por insucesso terapêutico, após interrupção do tratamento e por tuberculose crónica). Relativamente às categorias de risco para infecção VIH, consideraram-se relevantes os seguintes grupos: toxicodependência, homossexualidade e heterossexualidade promíscua.
Uma RA foi definida como uma reacção da qual resultou a interrupção de um ou mais fármacos e/ou que directamente resultou no internamento ou no seu prolongamento. No que concerne aos tipos de RA, consideraram-se os seguintes: hepática, cutânea, digestiva, renal, auditiva, ocular, hematológica, reumatológica, endócrina, neurológica e psíquica.
A hepatotoxicidade foi definida de acordo com a elevação das transaminases, três vezes mais do que o limite superior do normal, na presença de sintomas como anorexia, náuseas, vómitos ou dor abdominal, ou uma elevação das transaminases cinco vezes mais do que o limite normal, mesmo na ausência de sintomas. A hepatite tóxica foi considerada induzida por fármacos se as transaminases eram normais antes do início do tratamento, se aumentaram durante o tratamento e se normalizaram após a descontinuação do fármaco responsável. As comorbilidades consideradas significativas para a RA de hepatotoxicidade foram: hepatite C, hepatite B, alcoolismo crónico e doença hepática crónica. Um fármaco foi definido como responsável pela RA se os sinais ou sintomas regrediram após a sua suspensão e reapareceram após a sua reintrodução.
Quanto à gravidade da RA, foi classificada nos seguintes grupos: não grave, motivou internamento, prolongou o internamento, com risco de morte e provocou a morte do doente. As RA tiveram como implicação terapêutica a suspensão do fármaco, sendo estes casos divididos naqueles em que houve ou não a reintrodução do fármaco suspeito. Os que fizeram reintrodução foram classificados em dois grupos: aqueles em que houve recorrência ou não, de RA idêntica. Uma RA grave, que resolveu após a suspensão de determinado fármaco, foi atribuída a esse fármaco mesmo sem a sua reintrodução. Se a RA resolveu após a suspensão de dois ou mais fármacos, o cálculo do evento foi dividido igualmente entre os potenciais fármacos responsáveis. No que respeita à relação causal fármaco-RA, esta foi classificada em definitiva, provável, possível e improvável. Em relação à evolução no internamento, distinguiram-se dois grupos: doentes com melhoria clínica e falecidos com relação à RA.
As características demográficas e os dados clínicos dos doentes foram usados como variáveis independentes. A relação entre variáveis independentes e a frequência e a gravidade das RA foi feita através de uma análise multivariada.
Os dados foram analisados pelo teste t de Student, one-way ANOVA e regressão logística. A aplicação utilizada para a análise estatística foi o programa SPSS (Statistical Package for the Social Sciences), versão 15.0.
Resultados
Dos 1400 doentes internados com tuberculose activa e tratados entre Abril de 1999 e Julho de 2007, 175 (12,5%) apresentaram, pelo menos, uma RA induzida pelos antibacilares, num total de 192 eventos.
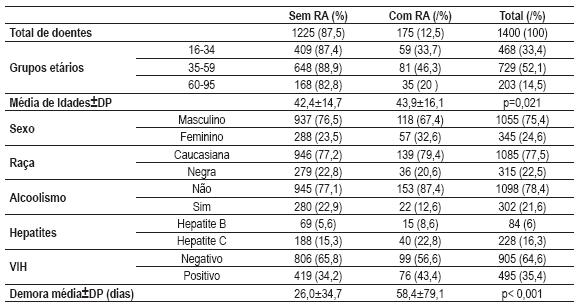
No Quadro I estão assinaladas algumas características da população estudada. A maioria dos doentes com RA pertencia ao sexo masculino (118/67,4%) e encontrava-se no grupo etário entre os 35-59 anos (81/46,3%), com média etária de 43,9 ± 16,1 anos; as idades variaram entre os 19 e os 88 anos. Relativamente à raça, verificou-se que 139 doentes (79,4%) eram caucasianos e 36 (20,6%) pertenciam à raça negra.
Quadro I – Características dos doentes internados com TB (1999-2007)
Em relação ao país de origem, constatou-se que 32 doentes (18,3%) eram imigrantes, a maioria dos quais oriundos dos países africanos de língua oficial portuguesa (PALOP) – Angola, Cabo Verde e Guiné-Bissau (Fig. 1).
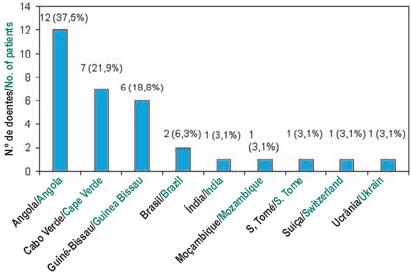
Fig. 1 – Origem dos doentes imigrantes
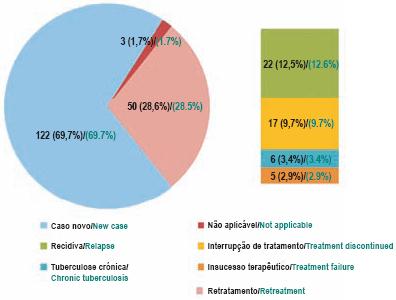
Fig. 2 – Classificação OMS
No que concerne à classificação da OMS (Fig. 2), a maior parte (122/69,7%) eram casos novos e 50 (28,6%) retratamentos. Destes, 22 (12,6%) foram atribuídos a recidiva, 17 (9,7%) a interrupção do tratamento, 6 (3,4%) a tuberculose crónica e 5 (2,9%) a insucesso terapêutico. Em 3 doentes não foi possível a sua classificação.
Em relação à localização da doença (Fig. 3), verificou-se um predomínio da tuberculose pulmonar (144/82,3%), estando a forma miliar presente em 22 casos (12,6%). As restantes localizações foram extrapulmonares (52/29,7%), das quais se destacaram: ganglionar torácica (16/9,1%), ganglionar periférica (11/6,3%) e pleural (10/5,7%). Com menor frequência salientam-se ainda as seguintes localizações extrapulmonares: meninges, córtex cerebral, intestino/retroperitoneu, baço, aparelho urogenital, peritoneu e laringe.
A presença de coinfecção VIH, nos doentes com RA, registou-se em 76 casos (43,4%). A dependência de drogas (consumidas por via endovenosa ou por outra via) constituiu o factor de risco predominante para a infecção pelo VIH (57/75%).
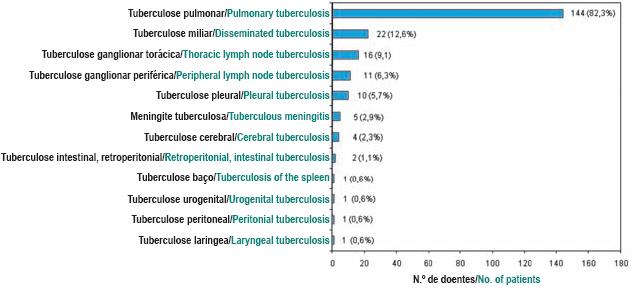
Fig. 3 – Principais localizações da tuberculose nos doentes com RA
Os níveis de linfócitos CD4 (Quadro II) foram determinados em 464 (33%) do total de doentes. A média de CD4 em cada um dos grupos, com e sem RA, foi respectivamente de 214 e 362,9 células/mm3.
Quadro II – Determinação de CD4 (média de células/mm3)
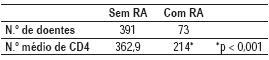
Esta diferença foi estatisticamente significativa (p< 0,001). Registaram-se diferenças estatisticamente significativas entre os dois grupos de doentes, com e sem RA, no que diz respeito à média de idades (43,9 versus 42,4 anos; p= 0,021), aos níveis médios de CD4 (214 versus 362,9 células/mm3; p< 0,001) e à demora média de internamento (58,4 versus 26 dias; p<0,001), como se mostra respectivamente nas Figs. 4, 5 e 6.
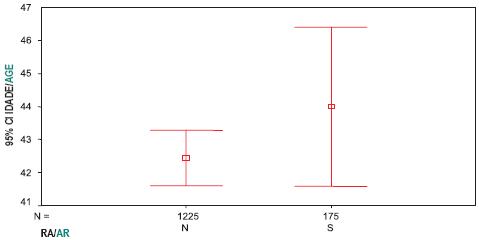
Fig. 4 – Média de idades em doentes sem RA versus com RA (p=0,021)
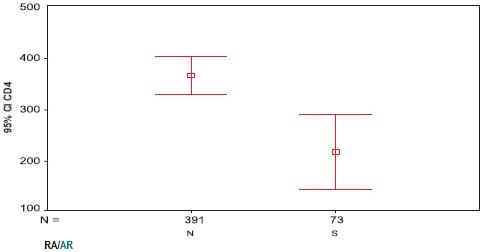
Fig. 5 – Níveis médios de CD4 em doentes sem RA versus com RA (p< 0,001)
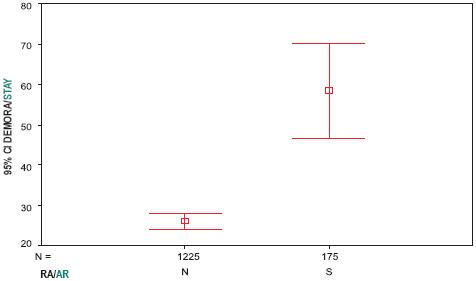
Fig. 6 – Demora média de internamento de doentes sem RA versus com RA (p<0,001)
Do total de 192 eventos, a hepatotoxicidade foi a RA mais prevalente (83/43,2%), seguindo-se a reacção cutânea (55/28,7%) e a intolerância gastrintestinal (25/13%). Para além das três principais RA já descritas, registaram-se ainda as seguintes: renais (6/3,1%), auditivas (6/3,1%), reumatológicas (6/3,1%), neurológicas (4/2,1%), hematológicas (3/1,6%), endócrinas (3/1,6%) e neuropsíquicas (1/0,5%) (Fig. 7).
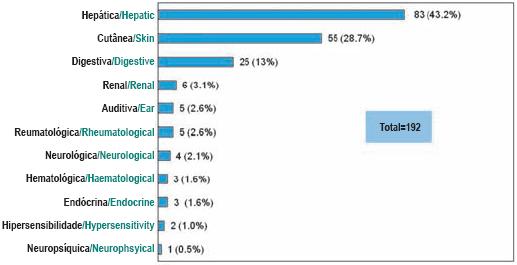
Fig. 7 – Tipo de reacções adversas
A hepatite C (40 / 48,2%) foi a comorbilidade mais significativa associada às RA de hepatoxicidade, seguindo-se o alcoolismo crónico (23/27,7%) e a hepatite B (15/18,1%) (Fig. 8).
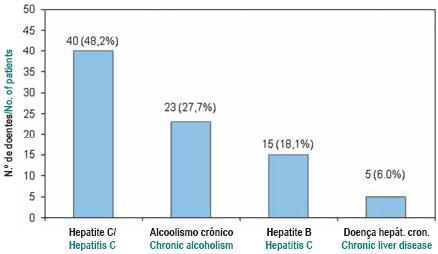
Fig. 8 – Comorbilidades para reacções de hepatotoxicidade
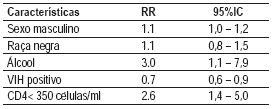
O risco de ocorrência de qualquer RA não foi associado ao sexo, à raça ou à infecção VIH. Contudo, esse risco foi associado significativamente ao alcoolismo ([RR] de 3,0 ; [IC], 1,1-7,9) e aos níveis de CD4 < 350 células/mm3 ([RR] de 2,6 ; [IC], 1,4-5) (Quadro III).
Quadro III – Risco relativo para as RA em geral
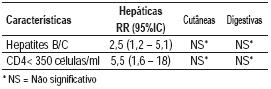
No modelo preditivo, as reacções hepáticas foram associadas de forma significativa à ocorrência de hepatites virais B e/ou C ([RR] de 2,5; [IC], 1,2-5,1) e, ainda de forma mais significativa, aos níveis de CD4 <350 células/mm3 ([RR] de 5,5; [IC], 1,6-18,6) (Quadro IV). No que diz respeito às reacções cutâneas e digestivas, este modelo não detectou qualquer variável que estivesse a elas associado.
Quadro IV – Risco relativo para as RA específicas
A determinação da relação causal (definitiva, possível, provável) não registou diferenças significativas relativamente à duração da RA, à idade, aos níveis de CD4 e à demora média de internamento.
Dos 134 casos em que foi possível caracterizar a gravidade das RA, 16 casos (11,9%) motivaram o internamento, 74 (55,2%) prolongaram o internamento, 5 (3,7%) constituíram risco de morte e 6 doentes (4,5%) faleceram; em 30 doentes (22,4%) a RA foi considerada não grave.
O fármaco mais implicado foi a isoniazida (84/62,7%), seguida da rifampicina (70/52,2%) e da pirazinamida (29/21,6%) (Fig. 9). Na maioria dos casos (63/47%), a relação causal fármaco-RA foi considerada provável. Foi possível estabelecer uma associação definitiva entre o fármaco e a RA em 24 doentes (17,9%) e em 48 (35,8%) esta relação foi considerada possível. A RA conduziu à suspensão do antibacilar em 106 doentes (79%), sendo possível a sua reintrodução em 60 casos (56,6%). Destes, 23 (38,3%) voltaram a apresentar reacção idêntica, com necessidade de suspensão definitiva (Fig. 10). Dos doentes em que foi possível caracterizar a gravidade da RA, 13 (9,6%) faleceram, sendo que apenas em 6 (4,4%) houve relação com a RA (5 doentes com hepatotoxicidade e um com toxicidade renal) (Fig. 11). Verificou-se que os 5 doentes cuja causa de morte esteve directamente relacionada com RA de hepatotoxicidade apresentavam comorbilidades importantes: coinfecção VIH (3 doentes), hepatite viral C (2) e doença hepática crónica etanólica (1). Destes, 2 doentes tinham formas graves de tuberculose: miliar com envolvimento do sistema nervoso central e disseminada. O doente em que a nefrotoxicidade foi a RA implicada na causa de morte apresentava, como patologias associadas, diabetes mellitus e nefropatia diabética.
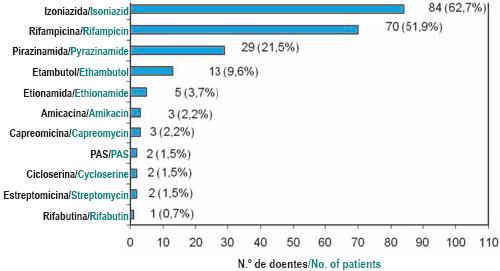
Fig. 9 – Fármacos implicados nas reacções adversas
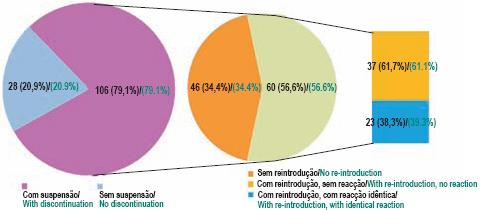
Fig. 10 – Reintrodução do fármaco
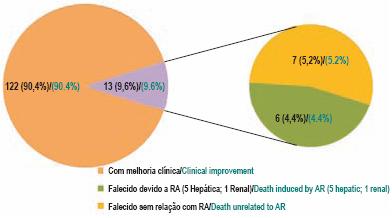
Fig. 11 – Evolução dos doentes com reacções adversas
Discussão e considerações finais
A tuberculose, independentemente da sua localização, é uma doença infecciosa que pode ser totalmente curada pela utilização de associações padronizadas de fármacos antibacilares. No entanto, os regimes terapêuticos correntes podem causar RA, as quais podem condicionar elevada morbilidade, prolongar o internamento hospitalar e obrigar a interrupção dos esquemas de tratamento, conduzindo à falência terapêutica e, consequentemente, dificultando a erradicação da tuberculose6.
No presente estudo, a incidência de RA aos antibacilares foi significativa, sendo mais elevada do que em alguns estudos anteriormente publicados7. Nesta amostra de doentes, o predomínio do sexo masculino, o número de imigrantes e os respectivos países de origem, bem como a localização maioritariamente pulmonar da doença, estão de acordo com a situação epidemiológica da tuberculose em Portugal8. A tuberculose miliar aparece logo em segundo lugar, justificando o facto de as formas graves de tuberculose e da coinfecção VIH/tuberculose estarem, em alguns estudos, associadas ao aumento da incidência de RA4,6,9. Na presente análise, a presença por si só da infecção VIH não constituiu um factor de risco para o desenvolvimento de RA aos antibacilares. No entanto, naqueles em que os valores de CD4 eram inferiores a 350 células/mm3, esse risco foi significativo, tanto para as RA em geral, como para as RA de hepatotoxicidade em particular.
Em relação à distribuição etária dos doentes desta série, os resultados são coincidentes com os de outros estudos, que concluem que a incidência e a gravidade das RA aumentam com a idade9,10. Outros autores11 são da opinião que a idade não é um factor de risco para o aparecimento de RA, nomeadamente as reacções de hepatoxicidade. De salientar que, na presente revisão, no que diz respeito à média de idades, registaram-se diferenças estatisticamente significativas entre os dois grupos de doentes, com e sem RA. Vários estudos retrospectivos sugerem que a gravidade das RA em geral6 e da hepatotoxicidade12 induzida por antibacilares em particular pode ser maior em mulheres. Na nossa casuística, o risco de ocorrência de qualquer RA, e particularmente da hepatotoxicidade, não foi associado ao sexo, e dos 5 doentes que faleceram, na sequência desta reacção, apenas um pertencia ao sexo feminino.
O alcoolismo, de acordo com alguns autores13, é um factor de risco bem estabelecido para o aparecimento da hepatotoxicidade induzida por fármacos. Contudo, no presente estudo, o risco de RA de hepatoxicidade não foi associado de forma significativa ao alcoolismo. Apesar deste facto, o alcoolismo constituiu uma das comorbilidades mais frequentes nos doentes que tiveram este tipo de reacção. No entanto, quando se fez a análise de risco de ocorrência de qualquer RA, o alcoolismo já foi associado de forma significativa.
As RA mais frequentes na presente análise foram as de hepatotoxicidade, que para a maioria dos autores são as que assumem maior gravidade. Segundo a literatura14,15, a elevação transitória, moderada e assintomática das transaminases séricas, não requerendo a alteração do regime terapêutico, é comum; as formas graves de hepatoxicidade que implicam a suspensão do esquema antibacilar são pouco frequentes e predominam nos doentes com factores de risco para hepatite. Os nossos resultados demonstraram que as reacções hepáticas tinham uma importante relação com as hepatites virais B e/ou C, o que está de acordo com a literatura. No entanto, para outros autores16, não foi encontrada qualquer associação entre as hepatites virais e as RA.
Relativamente ao estado imunitário dos doentes com infecção VIH, num trabalho recente publicado em 2008, os autores17 concluem que existe uma associação estatisticamente significativa entre a diminuição de CD4 e o aparecimento de hepatotoxicidade. Esta conclusão coincide com os nossos resultados, em que se encontrou uma associação significativa entre a ocorrência de reacções de hepatotoxicidade e os níveis de CD4 inferiores a 350 células/ /mm3. Este fenómeno não é referido noutros estudos anteriores e pode sugerir a presença de um mecanismo imunológico para o aparecimento da hepatite tóxica induzida pelos antibacilares, embora o mecanismo exacto não tenha ainda sido claramente estabelecido18. Uma outra explicação para este fenómeno pode consistir no facto destes doentes, que estão profundamente imunodeprimidos e com maior susceptibilidade a infecções oportunistas, terem necessidade de outras terapêuticas também com potencial hepatotóxico19,20.
Um dos efeitos das RA nos doentes internados com TB sob tratamento antibacilar é o aumento da demora média21, facto que na nossa casuística se verificou de forma significativa.
De salientar que os doentes em que a RA foi directamente implicada na causa de morte apresentavam comorbilidades significativas que potenciaram a gravidade da evolução clínica.
Nos doentes que desenvolvem RA aos antibacilares é de extrema importância a monitorização clínica para analisar a sua evolução7,22,23. Atendendo a que, no presente estudo, as reacções de hepatotoxicidade foram as mais frequentes, é útil, para reduzir o risco destas reacções, reforçar os seguintes aspectos:
Avaliar a função hepática antes de iniciar a terapêutica antibacilar;
Monitorizar os níveis séricos das enzimas hepáticas, pelo menos duas vezes por semana, nas duas primeiras semanas, e uma vez por semana nos dois meses seguintes;
Suspender de imediato a terapêutica antibacilar, caso se verifique um aumento das enzimas hepáticas três vezes superior ao valor de base;
Evitar associar outros fármacos indutores do citocromo P450.
Bibliografia
1. Tratamento da tuberculose latente, revisão das normas, Sociedade Portuguesa de Pneumologia.
2. Program Abstr 4th Conf Retrovir Oppor Infect Conf Retrovir Oppor Infect 4th 1997 Wash DC 1997; 4(186): abstract no. 659ª.
3. Mota A. Reacções adversas aos antibacilares. 3th Virtual Congress HIV-AIDS, 2002.
4. Sharma SK, Mohan A, Kadhiravan T. HIV-TB coinfection : epidemiology, diagnosis & management. Indian J Med Res 2005; 121(4):550-567.
5. Forget EJ, Menzies D. Adverse reactions to first–line antituberculosis drugs, Expert Opin Drug Saf 2006; 5(2):231-249.
6. Yee D, Valiquette C, Pelletier M, Parisiene I, Rocher I, Menzies D. Incidence of serious effects from first –line antituberculosis drugs among patients treated for active tuberculosis. Am J Respir Crit Care Med 2003; 167(11):1472-1477.
7. Gulbay BE, Gurkan OU, Yildiz AO, Onen ZP, Erkekol FO, Baççioglu A, Acican T. Side effects due to primary antituberculosis drugs during the initial phase of therapy in 1149 hospitalized patients for tuberculosis. Respir Med 2006; 100(10):1834-1842.
8. Ana Maria Correia, Luís Castro. Epidemiologia da Tuberculose em Portugal-Perspectiva epidemiológica. Actualização em tuberculose. II Curso de Pós –Graduação da Escola de Pneumologia da SPP, 2006.
9. Lanternier F, Dalban C, Perez L, Bricaire F, Costagliola D, Caumes E. Tolerability of antituberculosis treatment and HIV serostatus. Int J Tuberc Lung Dis 2007; 11(11);1203-1209.
10. Cantalice JP, Bóia MN, Sant Anna CC. Analysis of the treatment of pulmonary tuberculosis in elderly patients at university Hospital in Rio de Janeiro, Brazil. J Bras Pneumol 2007; 33(6):691-698.
11. Yimer G, Aderaye G, Amogne W, Makonnen E, Aklillu E, et al. Anti-tuberculosis therapy-induced hepatotoxicity among Ethiopian HIV-positive and negative patients. 2008; PLoS ONE 3(3): e1809. doi:10.1371/ journal.pone.0001809.
12. Saukkonen JJ, Cohn DL, Jasmer RM, Schenker S, Jereb JA, Nolan CM, Peloquin CA, Gordin FM, Nunes D, Strader DB, Bernardo J, Venkataramanan R, Sterling TR, on behalf of the ATS Hepatotoxicity of Antituberculosis Therapy Subcommittee. Am J Respir Cril Care Med 2006; 174:935-952.
13. Sharma SK, Balamurugan A, Saha PK, Pandey RM, Mehra NK. Evaluation of clinical and immunogenetic risk factors for the development of hepatotoxicity during antituberculosis treatment. Am J Respir Crit Care Med 2002; 166:916-919/Yee D, Valiquette C, Pelletier M, Parisien I, Rocher I, et al. Incidence of serious side effects from first-line antituberculosis drugs among patients treated for active tuberculosis. Am J Respir Crit Care Med 2003; 167:1472-1477.
14. Vidal Pla R, de Garcia X, Gallego B, Algueró C, Bravo C. The hepatotoxicity of tuberculosis treatment. Med Clin (Barc) 1991; 97(13):481-485.
15. Yew WW, Leung CC. Antituberculosis drugs and hepatotoxicity. Respirology 2006; 11(6):699-707. [ Links ]
16. Int J Tuberc Lung Dis 2007; 11(8):868-875.
17. Yimer G, Aderaye G, Amogne W, Makonnen E, Aklillu E, et al. Anti-tuberculosis therapy-induced hepatotoxicity among Ethiopian HIV-positive and negative patients. 2008; PLoS ONE 3(3): e1809. doi: 10.1371/ journal.pone.0001809.
18. Pol S, Lebray P, Vallet-Pichard A. HIV Infection and hepatic enzyme abnormalities: Intricacies of the pathogenic mechanisms. Clinical Infectious Diseases 2004; 38:65-72.
19. Hoffmann C, Rockstroh JK, Kamps BS. HIV Medicine 2006; 395-480.
20.Mehta U, Durrheim DN, Blockman M, Kredo T, Gounden R, Barnes KI. Adverse drug reactions in adult medical inpatients in a South African hospital serving a community with a high HIV/AIDS prevalence: prospective observational study. Br J Clin Pharmacol 2008; 65(3):396:406. Epub 2007 Dec 7.
21. Gholami K, Kamali E, et al. Evaluation of antituberculosis induced adverse reactions in hospitalized patients, Pharmacy Practice 2006; 4(3):134-138.
22.Yamada H, Yasuoka A, Sasayama K, et al. Adverse reactions of antituberculous agents, especially about its onset and duration. Kekkaku, 1990; 65(9):563-568.
23. Kobashi Y, Niki Y, et al. Adverse reactions of antituberculous agents. Kekkaku 1998; 73(7):485-490.
Hospital de Pulido Valente, Centro Hospitalar Lisboa Norte, Lisboa
Alameda das Linhas de Torres, 117
1769-001 Lisboa
e-mail: anasofia.vilarica@gmail.com
Recebido para publicação/received for publication: 09.07.31
Aceite para publicação/accepted for publication: 09.11.05













