Introdução
A infeção e a resistência dos microrganismos aos antimicrobianos são problemas atuais e interdependentes. As instituições não podem ficar indiferentes às suas implicações e impacto nos utentes, nas unidades de saúde e comunidade (Programa de Prevenção e Controlo da Infeção e Resistência aos Antimicrobianos, 2017).
A Infeção Associada aos Cuidados de Saúde (IACS) é hoje um conceito alargado de infeção que ocorre num doente durante o processo de prestação de cuidados num hospital ou noutra instituição de cuidados de saúde, que não estava presente e nem em incubação no momento de admissão, (World Health Organization, 2011).
Mais de 4 milhões de utentes, na Europa, são afetados por IACS todos os anos e nos Estados Unidos da América (EUA) correspondem a 1.7 milhões (WHO, 2011). Cerca de 5-10% dos doentes admitidos nos hospitais dos países desenvolvidos adquirem uma ou mais IACS e estas percentagens podem exceder os 25% nos países de baixo desenvolvimento, (Damani, 2012).
Estudos, nacionais e internacionais, definem as Unidades de Cuidados Intensivos (UCI) como os serviços de maior risco para os doentes adquirirem esta entidade nosológica. A WHO (2011) aponta uma taxa de 30% de doentes admitidos em UCI afetados por um episódio de IACS, estando associadas a taxas de morbilidade e mortalidade significativas. Nas UCI nos EUA, a pneumonia associada à ventilação (PAV) é a segunda IACS mais comum, com taxas de 25%. (Sedwick, Lance-Smith, Reeder & Nardi, 2012. Recentemente, os dados da Vigilância Epidemiológica na rede europeia, coordenada pelo European Centre For Disease Prevention and Control (ECDC), na qual Portugal também participa, verificam que no ano de 2017, 8,3% (11787) dos pacientes internados mais de dois dias em UCI adquiriram pelo menos uma IACS (PAV, bacteriemia associada ao Cateter Venoso Central (CVC) ou Infeção Trato Urinário-ITU associada ao cateter vesical-CV). Destas IACS a PAV surge como a mais prevalente, em 6% dos casos, em que 97% destas infeções estão associados à intubação traqueal, sendo a Pseudomonas aeruginosa o microrganismo mais isolado, (ECDC, 2019).
O Programa de Prevenção e Controlo de Infeções e de Resistências aos Antimicrobianos (PPCIRA), no seu Relatório Anual do Programa Prioritário, refere que globalmente em Portugal, no período de 2013 a 2017, os resultados melhoraram face ao controlo de IACS e resistência aos antimicrobianos. A Vigilância Epidemiológica (VE) das UCI revela um decréscimo de 10,81% na densidade de incidência de PAV por 1000 dias de entubação no ano de 2017 em relação a 2013, bem como uma redução de 30,77% na densidade de incidência de bacteriemia por 1000 dias de CVC relativamente ao mesmo período.
A presença de dispositivos invasivos e os procedimentos cirúrgicos são descritos com os principais fatores de risco, bem como as infeções por microrganismos multirresistentes, que na atualidade, representam uma ameaça significativa devido ao impasse terapêutico que originam, (Pina, E., Ferreira, E.,Marques, A. & Matos, B., 2010). Nos anos 60 a 80 ficou conhecido o fenómeno da multirresistência relacionado com enterobactérias e Pseudomonas. No dias de hoje e em particular nas UCI passou a ser problemática a emergência de determinados Microrganismos Multirresistentes (MMR) como causadores de infeção hospitalar/IACS, tomando especial importância bactérias como Staphylococcus aureus meticilina-resistente (MRSA), Enterococos vancomicina-resistentes (VRE) e Gram negativos produtores de beta-lactamase de espectro alargado (ESBL), para os quais se vão tornando escassas as armas eficazes. Os MMR são microrganismos, maioritariamente bactérias, que são resistentes a uma ou mais classes de agentes antimicrobianos, (Centre for Disease Control, 2017). Estes microrganismos estão associados às infeções hospitalares da corrente sanguínea, infeção respiratória/pneumonia nosocomial, infeção do trato urinário e infeção do local cirúrgico e de pele e tecidos moles, tendo um potencial epidémico significativo, (Pina et al, 2010). Este tipo de infeções manifestam-se de forma semelhante àquelas provocadas por microrganismos sensíveis, no entanto a escassez das opções terapêuticas complica a abordagem no tratamento das mesmas. Constatando-se um aumento nos tempos de internamento e custos, bem como taxas de morbi-mortalidade significativas, (CDC, 2017).
1. Enquadramento teórico
As Infeções Associadas aos Cuidados de Saúde são uma problemática transversal às diversas instituições prestadoras de cuidados de saúde, quer a nível nacional, bem como mundial. É essencial a união de esforços dirigidos à sua prevenção e controlo, envolvendo não só profissionais de saúde, mas também órgãos de gestão e políticos na fomentação de uma cultura de segurança e qualidade dos cuidados prestados.
O ECDC no seu estudo de Prevalência das IACS e Resistência aos Antimicrobianos, de 2016-2017, envolvendo 28 países da União Europeia/Zona Económica Europeia, incluindo Portugal, reporta que 5,9% dos doentes desenvolveram uma IACS (Suetens, C.,Latour, K.,Karki,T.,Ricchizzi, E. & Kinross, P. et al, 2018). A prevalência e tipologia das IACS são variáveis, denotando-se diferenças a nível mundial, o mesmo se verificando no nosso país. Nos EUA as infeções mais comuns são a do trato urinário (36% e 27% respetivamente). Na Europa a IACS mais prevalente é a infeção do trato respiratório (21,45% pneumonia e 4,3% outras infeções do trato respiratório inferior), seguida da ITU (18,9%) e as Infeções da Corrente Sanguínea surgem em 10,8% dos casos (Suetens et al, 2018).
Estudos, nacionais e internacionais, definem as UCI como os serviços de maior risco para os doentes adquirirem esta entidade nosológica. A WHO (2011) aponta uma taxa de 30% de doentes admitidos em UCI afetados por um episódio de IACS, estando associadas a taxas de morbilidade e mortalidade significativas. Nas UCI nos EUA, a pneumonia associada à ventilação (PAV) é a segunda IACS mais comum, com taxas de 25%. (Sedwick, Lance-Smith, Reeder & Nardi, 2012). Recentemente, os dados da Vigilância Epidemiológica na rede europeia, coordenada pelo ECDC, na qual Portugal também participa, verificam que no ano de 2017, 8,3% (11787) dos pacientes internados mais de dois dias em UCI adquiriram pelo menos uma IACS (PAV, bacteriemia associada ao CVC ou infeção trato urinário associada ao cateter vesical). Destas IACS a PAV surge como a mais prevalente, em 6% dos casos, em que 97% destas infeções estão associados à intubação traqueal, sendo a Pseudomonas aeruginosa o microrganismo mais isolado, (ECDC, 2019). Em Portugal, em 2017, as UCI tiveram uma densidade de incidência de PAV/1000 dias de intubação de 7.2, sendo inferior à média Europeia (9,5/1000 dias de intubação), no mesmo período. Dos microrganismos isolados os mais frequentes foram as Pseudomonas Aeruginosas (29,2%), Klebsiella spp. (19,7%) e Staphylococcus aureus com 13,8%.
A Infeção Respiratória Associada à Ventilação (IRAV) define-se como uma infeção do parênquima pulmonar, estando associada ao uso do tubo endotraqueal (TET) em doentes submetidos a ventilação mecânica num período superior ou igual a 48 horas, (Lawrence & Fulbrook, 2011). É uma das complicações mais preocupantes no contexto dos cuidados intensivos, porque para além de aumentar as taxas de mortalidade em cerca de 20-50%, é responsável pelo aumento do tempo de internamento, sensivelmente em 6 dias, (Rello, Lode, Cornaglia & Masterton, 2010). Por outro lado, Caserta et al (2012) complementam, afirmando que este tipo de infeção aumenta o tempo de ventilação mecânica, como também potencia e acentua a utilização excessiva de antibióticos, refletindo-se em custos hospitalares acrescidos.
O mecanismo etiológico descrito como o maior responsável pela IRAV, consiste na colonização do trato orofaríngeo e digestivo com microrganismos potencialmente patogénicos e a aspiração subsequente de secreções contaminadas para a via aérea inferior, (Lawrence & Fulbrook, 2011). Os mesmos autores descrevem que os doentes com TET estão mais expostos ao risco de desenvolver IRAV, porque este dispositivo invasivo quebra as barreiras de defesa naturais da via aérea do organismo (reflexo de tosse diminuído, encerramento da epiglote alterado, ação mucociliar diminuída). Por outro lado, o TET funciona como uma porta de entrada de microrganismos para a via aérea inferior. Para além disto, a existência de co-morbilidades, tais como a desnutrição, doença pulmonar obstrutiva crónica, sinusite crónica e higiene oral pobre são descritos como fatores de risco adicionais, (Lawrence & Fulbrook, 2011).
Ainda existe muita controvérsia quanto às melhores estratégias a utilizar para diagnosticar este tipo de infeção, que consistem em técnicas não-invasivas e técnicas invasivas. A maior dificuldade para a comparação da efetividade e valor de cada uma destas técnicas, consiste no fato de não existir uma estratégia padrão de diagnóstico de IRAV, (Vicente et al, 2010). No âmbito desta dificuldade de diagnóstico, Lawrence e Fulbrook (2011) fazem referência às normas do Centres for Disease Control (CDC) de 2008, que recomendam a combinação de dados clínicos, radiológicos e laboratoriais para diagnosticar a PAV. Em Portugal, estas recomendações servem de referência para o Programa Nacional de Controlo de Infeção (PNCI).
Outro tipo de IACS são as Infeções Nosocomiais da Corrente Sanguínea (INCS), normalmente associadas ao uso de Catéteres Venosos Centrais (CVC). Os cateteres centrais temporários, os cateteres centrais de inserção periférica, os cateteres de alto fluxo utilizados na diálise e os cateteres tunelizados constituem o grupo designado de CVC, (Hsu, 2014). Estes dispositivos intravasculares são indispensáveis para a prática clinica e tratamento do doente crítico, em particular nas UCI. Apesar de permitirem um acesso vascular importante para administração de drogas, monitorização hemodinâmica invasiva e outras terapias, como a Hemodiafiltração Veno-Venosa continua, o seu uso implica riscos para o doente. Podem incluir complicações locais a sistémicas, englobando as infeções do local de inserção do catéter, as infeções da corrente sanguínea associada a CVC e também, as tromboflebites e endocardites, entre outras. Ruiz-Giardin et al (2019) referem que 15 a 30% de todas as bacteriemias nosocomiais estão associadas a dispositivos intravasculares, é estimado que cerca de 70% de todos os pacientes admitidos em contexto hospitalar, são submetidos a cateterização venosa. As UCI são descritas como as unidades com maior prevalência deste tipo de infeção, seguidas pelas unidades de hematologia e oncologia, (Ruiz-Giardin et al, 2019).
Diversos autores descrevem as infeções da corrente sanguínea associada a CVC como responsáveis por taxas de mortalidade e morbilidade significativas, resultando também num impacto económico importante. O custo de uma só infeção nosocomial da corrente sanguínea (INCS) associada ao CVC é aproximadamente 16500 US dólares, em que a taxa de mortalidade é 2-4 vezes superior relativamente aos doentes que não adquirem este tipo de infeção, (Wichman et al 2018). No relatório epidemiológico para o ano de 2017 do ECDC, foram reportados 5298 casos de INCS, em UCI, em que cerca de 36.5% estavam associadas ao CVC, (Suetens el al, 2019).
A nível nacional, com base no Relatório Anual do PPCIRA de 2018, verifica-se um aumento na participação dos hospitais que monitorizam as INCS, observando-se uma diminuição na Densidade de incidência desta infeção do ano de 2013 a 2017 de 2,5%, correspondendo a 1,18/1000 dias de internamento. Quanto à densidade de incidência de INCS associada ao CVC nas UCI portuguesas, que participam na Vigilância Epidemiológica (VE) na rede europeia do ECDC, também constatam uma maior participação das instituições nesta monitorização e também uma redução de 30,77% no ano de 2017 face a 2013, (PPCIRA, 2018).
São diversas as propostas de critérios para o diagnóstico deste tipo de infeção, incluindo a temperatura corporal, e análises laboratoriais básicas, como contagem celular e níveis de Proteina-C-reativa no sangue, juntamente com hemoculturas e análise microbiológica da ponta do CVC, (Frykholm et al 2014). Em Portugal, com base nas normas da Direção Geral da Saúde (DGS), para diagnóstico deste tipo de IACS são utilizados critérios clínicos e laboratoriais, definindo Infeção da Corrente Sanguínea Associada a Cateter quando existe pelo menos uma hemocultura positiva obtida através de veia periférica, ponta de CVC colonizada com o mesmo microrganismo encontrado na(s) hemoculturas e manifestações clínicas de infeção (febre, arrepios e/ou hipotensão) e sem a presença aparente de outras fontes de infeção (PNCI, 2006).
A dimensão do hospital, os serviços/unidades e tipo de cateter podem influenciar consideravelmente as taxas de INCS relacionada com cateter, bem como fatores de risco intrínseco dos doentes, tais como tipo e gravidade da doença (grande queimado, cirurgia cardíaca), assim como os parâmetros relacionados com o catéter, nomeadamente as condições em que foram colocados (i.e; electiva versus urgente) e o tipo de catéter (i.e; tunelizáveis versus percutâneos) ou o local de colocação (i.e; veia subclávia versus veia jugular), (PNCI, 2006). A colonização do CVC por microrganismos pode ter origem na microflora da pele do doente, levando à contaminação deste dipositivo no momento da inserção, ou através das mãos dos profissionais de saúde, que durante as manipulações do cateter contribuem para a sua contaminação. Outras causas, menos comuns, são a administração de infusões endovenosas contaminadas ou a via hematogénea, (Loveday et al, 2014). De acordo com Hentrich et al (2014) quando o uso do CVC é inferior a 14 dias, o mecanismo da infeção está relacionado com a contaminação da zona extraluminal do CVC, com a subsequente proliferação de microrganismos ao longo do trajeto exterior do cateter, enquanto, nos casos em que o doente está exposto ao CVC mais do que 14 dias, a porta de entrada dos microrganismos será a via intraluminal. Estes autores descrevem que em menos de 24horas, após a inserção do CVC, forma-se um biofilme na parede interior, composto por substâncias como polissacarídeos e fibrina, que conferem um meio óptimo para a proliferação de bactérias, servindo, ao mesmo tempo, como cápsula de proteção destas contra a ação de mecanismos de defesa ou da antibioterapia, (Hentrich et al, 2014). Os depósitos de microcristais, provenientes dos “flushs” de solução salina ou o microtrauma, resultante do momento de inserção do CVC, que promovem a formação de pequenos trombos na ponta intravascular do cateter, são designados como possíveis habitats de proliferação bacteriana, (Hentrich et al, 2014).
A Infeção do Trato Urinário (ITU), outro tipo de IACS, também está fortemente associada ao uso de dispositivo invasivo -o cateter vesical (CV). Laan et al (2017) afirmam que na generalidade dos hospitais cerca de 15-25% dos doentes são submetidos à cateterização vesical durante o internamento e que, no contexto hospitalar Ocidental, 40% de todas as infeções nosocomiais correspondem a ITU. O estudo de Prevalência das IACS e Uso de Antimicrobianos desenvolvido pelo ECDC, no período 2016-2017 (no qual Portugal é participante), descreve a ITU como a segunda IACS mais prevalente, correspondendo a 18,9% dos casos de IACS em hospitais de agudos, (Suetens et al, 2019). Halm (2014) descreve que nas UCI a prevalência no uso de cateter vesical é significativamente mais elevada (67%-76%) em relação a outras unidades (16%-33%). O Relatório Epidemiológico Anual do ECDC, referente às IACS adquiridas nas UCI (43 UCI Portuguesas participaram nesta VE), no ano de 2017, reporta um total de 1274 casos de ITU, correspondendo, em média a cerca de 2% dos doentes admitidos em UCI, num período superior a dois dias e 97,9% dos casos foram associados ao uso de cateter urinário, (Suetens et al, 2019).
Os cateteres vesicais aumentam o risco para a infeção, na medida em que os mecanismos de defesa do doente, como a mucosa uretral e micção vão ser anulados, permitindo aos microrganismos deslocarem-se até à bexiga sem barreiras, (Loveday et al, 2014). A via intra-luminal e extra-luminal funcionam como vias de acesso dos microrganismos até ao trato urinário, no primeiro caso a contaminação acontece devido ao refluxo de urina de um reservatório de drenagem contaminado, enquanto no segundo caso a colonização acontece no momento da inserção do cateter através das mãos do profissional de saúde ou a partir da flora perineal do hospedeiro, (Loveday et al,2014). Com base em vários estudos, é evidente que o risco de infeção depende do método e duração da cateterização, da qualidade dos cuidados prestados, e a susceptibilidade do individuo. Pina et al (2010) referem que por cada dia de algaliação, o risco de infeção aumenta em 3 a 10%, e ao fim de 30 dias aproxima-se dos 100%.
As UCI são reconhecidas pelo maior risco dos doentes adquirirem uma IACS, associada à gravidade da sua situação clínica, mas também à exposição a diversos dispositivos/procedimentos invasivos. Ao longo das últimas décadas foram desenvolvidas várias iniciativas, com o objetivo de definirem as melhores estratégias para a prevenção das IACS, mais especificamente aquelas associadas ao uso de dispositivos invasivos, como o TET, o CVC e o CV. Pina et al (2010) salientam que o fato deste tipo de infeções, serem exógenas, ou seja, originam-se na introdução/implantação de microrganismos provenientes das mãos dos profissionais, material ou equipamento contaminado,”serão por definição, evitáveis”.
Na comunidade científica, a nível internacional, constata-se que a aplicação de normas/medidas preventivas como um conjunto, ou seja, como uma “Bundle” é mais efetiva e com melhores resultados na prevenção das IACS, em vez da aplicação das mesmas medidas de forma isolada. Rello et al (2010) definem “Bundle” como um conjunto de intervenções chave com fundamentação na evidência científica, que quando aplicadas na prática conduzem a uma melhoria dos resultados. Os mesmos autores explicam que os principais objetivos da “Bundle” consistem na mudança do processo do cuidar do doente crítico e na melhoria da adesão às respetivas medidas preventivas, (Rello et al, 2010).
Um dos exemplos de “Bundle” mais referenciados em diversos estudos que abordam esta temática e mais aplicados nas UCI a nível internacional e nacional, é aquela desenvolvida em 2005 e atualizada em 2010 pelo Institute Healthcare Improvement (IHI) no âmbito da “5 Million Lives Campaign”. Esta “Bundle” consiste na aplicação de medidas preventivas, baseadas em evidência científica (revisões sistemáticas de estudos randomizados controlados), aplicadas em conjunto, a todos os doentes submetidos a dispositivos invasivos, com o objetivo de diminuir as taxas de incidência de infeções associadas aos mesmos, nas UCI norte-americanas, (IHI, 2007). Por outro lado, a sua aplicação tem maior sucesso quando todas as suas medidas são executadas em conjunto, baseadas na estratégia “all-or-none”, (IHI, 2007). A dinâmica de trabalho das equipas tem que sofrer mudanças, no sentido da melhoria da comunicação entre os seus elementos, tornando-se mais efetiva, sendo essencial uma discussão e revisão multidisciplinar, diária dos objetivos e das estratégias do plano terapêutico definido, (Pina et al 2010). Estes autores também descrevem que esta metodologia de trabalho está fortemente associada à educação, formação de equipas de qualidade, monitorização do cumprimento das intervenções e a informação de retorno sobre o desempenho dos profissionais, (Pina et al 2010).
A nível Europeu, também foram desenvolvidas estratégias de prevenção das IACS, com base na metodologia de “Care Bundles”, um dos exemplos é a “Bundle” desenvolvida pelo National Services Scotland (NHS) em 2008. Foi com base nestes trabalhos científicos que, por sua vez, foram escolhidas as medidas integrantes da “Bundle” de prevenção da infeção respiratória associada à ventilação da UCIP do Centro Hospitalar objeto do presente estudo. Este conjunto de medidas engloba: a verificação regular da pressão do Cuff, mantendo entre os 20-30mmHg, a elevação da cabeceira da cama superior ou igual a 30˚, a realização da higiene oral três vezes ao dia com aplicação de Clorhexidina, o desmame da sedação e da ventilação precoce. Este projeto teve início na sua aplicação no ano de 2012.
Entretanto no ano 2015, em Portugal foram desenvolvidos pela DGS os “Feixe de intervenções”, que correspondem a um conjunto de medidas (“Bundle”) para a prevenção de IACS associadas a dispositivos/procedimentos invasivos. Dos quais salientam-se os “Feixes de intervenções” de Prevenção de: Pneumonia Associada à Intubação (Norma Nº21/2015), Infeção Relacionada com Cateter Venoso Central (Norma Nº22/2015) e Infeção Urinária Associada a Cateter Vesical (Norma Nº19/2015). O objetivo dos “Feixes ”consiste em assegurar que os doentes sejam submetidos aos melhores cuidados, baseados na evidência cientifica, de uma forma consistente, (DGS, 2015). Este conjunto de intervenções, deve ser implementado de forma integrada e em grupo, promovendo melhores resultados, com maior impacto do que a aplicação de cada uma destas intervenções individualmente, (DGS,2015). Outro aspeto importante do “Feixe de Intervenções” consiste na realização da Vigilância Epidemiológica relativa às IACS associadas à intubação, ao CVC e ao CV, e também a auditoria da adesão dos profissionais ao conjunto destas medidas, (DGS, 2015).
Apesar dos objetivos das recomendações de prevenção das IACS serem claros e baseados na evidência científica, a sua implementação na prática clínica diária demonstra uma certa heterogeneidade, o que influencia a sua execução e impossibilita os melhores resultados (Park, S.,Ko, S., Na, H., Bang, J, & Chung, W., 2017). Estes autores constatam que é importante existir uma coordenação consistente de diversos fatores, como: adequar as estratégias de implementação das recomendações à realidade de cada instituição/localidade/país, existirem sistemas de apoio financeiro, sensibilizar os órgãos de gestão para a promoção de uma cultura de segurança e qualidade nos cuidados no seio da instituição e, fomentar a formação adequada e contínua dos profissionais de saúde, (Park et al 2017).
Perante uma IACS, para além da implementação de critérios de diagnóstico objetivos e claros, também são essenciais algumas intervenções para o tratamento dessa infeção. Pina et al (2010) descrevem que a estratégia adequada de tratamento das IACS deve basear-se na identificação do foco infeccioso, na colheita de produtos biológicos para exame microbiológico (no caso da INCS associada ao CVC, é importante a análise da ponta do cateter), no controlo do foco (pode envolver a necessidade de procedimentos cirúrgicos) e início precoce de antibioterapia, em doses adequadas e com espectro de cobertura amplo, com posterior descalação, direcionada para as sensibilidades do agente causal.
O uso de antimicrobianos constitui nos dias de hoje uma questão central junto da comunidade científica e das instituições de saúde, na medida em que o uso excessivo e, por vezes desnecessário destes fármacos está diretamente relacionado com o aumento das resistências aos antimicrobianos (O’Neil, 2016). Este autor refere que quanto maior o uso de antimicrobianos, maior será a resistência desenvolvida pelos microrganismos, sendo importante a redução no seu consumo, salvaguardando a eficácia dos fármacos já existentes e diminuindo a necessidade da produção de novos antimicrobianos, com maior poder de ação, (O’Neil,2016). O PPCIRA (2017), explica que o aumento das taxas de resistência significa que, na presença de uma infeção, é maior a probabilidade do microrganismo responsável ser resistente aos antibióticos normalmente utilizados, obrigando à utilização de fármacos de espectro mais alargado, que por sua vez é potenciador de novas resistências. Este autor refere também que inverter esta tendência deve ser uma prioridade, não só na área da saúde humana, mas em todos os contextos que recorrem ao uso de antibióticos, como no caso da pecuária e saúde animal, (PPCIRA, 2017).
De acordo com Pina et al (2010) a questão da multirresistência aos antimicrobianos surgiu na década de 60 a 80 do Séc. XX, com as enterobactérias e a Pseudomonas. Nos dias de hoje a investigação cientifica reconhece microrganismos como Staphylococcus aureus Meticilino-Resistente (MRSA), enterococus vancomicina-resistentes (VRE) e os Gram-negativos produtores de beta-lactamases de largo espectro (ESBL) como os protagonistas desta problemática, que assume grande importância na medicina intensiva, pois estes estão associados a IACS da corrente sanguínea, respiratórias, do trato urinário, local cirúrgico, pele e tecidos moles, tendo um potencial epidémico significativo, (Pina et al 2010). Estes autores explicam que o fenómeno da resistência das bactérias aos antimicrobianos surge no decorrer do processo da luta pela sobrevivência das espécies e que se manifesta de duas formas: pela capacidade de sofrer mutações (pressão seletiva afetada pelas práticas na prescrição de antibióticos) e pela troca de informação genética entre espécies bacterianas (transmissão cruzada), (Pina et al, 2010). Różańska. et al (2017) referem que o rápido aumento da resistência de bactérias como o Staphylococcus e bacilos Gram-negativos é um problema central no seio das instituições de saúde, afeta significativamente a eficácia dos tratamentos disponíveis para as IACS, especialmente nos doentes com infeções severas admitidos nas UCI.
Os MMR são microrganismos, maioritariamente bactérias, que são resistentes a uma ou mais classes de agentes antimicrobianos, (CDC, 2017). As infeções por MMR manifestam-se de forma semelhante àquelas provocadas por microrganismos sensíveis, no entanto a escassez das opções terapêuticas complica a abordagem no tratamento das mesmas. Constatando-se um aumento nos tempos de internamento e custos, bem como taxas de morbi-mortalidade significativas, (CDC, 2017).
O CDC (2017) explica que, a partir do momento que este tipo de MMR, integram o ambiente de uma instituição de saúde, a transmissão e a persistência no nível de resistência irá depender: da vulnerabilidade dos doentes, da pressão seletiva exercida pelo uso de antimicrobianos, da probabilidade da transmissão (que depende do número de doentes colonizados ou infetados) e do impacto da implementação e adesão às medidas de prevenção. Nesta medida, é essencial a identificação daqueles doentes que correm maior risco para a colonização ou infeção por MMR. Pina et al (2010) descrevem alguns critérios que permitem a avaliação do risco/suscetibilidade para este tipo de infeções: antibioterapia prévia, imunossupressão, internamento recente/ou prolongado (superior a 2 dias nos 90 dias precedentes), permanência em lares ou doentes sujeitos a plano de hemodiálise não domiciliária.
Em Portugal, no ano de 2013 foi criado o Programa de Prevenção e Controlo de Infeções e de Resistência aos Antimicrobianos, surge como uma extensão da DGS às Unidades de saúde, com o intuito de dar uma resposta integrada na abordagem de ambos problemas, (PPCIRA, 2018). Este Programa tem como base de ação três grandes pilares: a prevenção e controlo da Infeção com base na implementação de boas práticas através das Precauções Básicas Controlo da Infeção e as Precauções Baseadas nas Vias de Transmissão dos Microrganismos; a redução da emergência de resistências aos antimicrobianos (RAM), reduzindo e monitorizando o seu consumo; a Vigilância Epidemiológica, que possibilita a monitorização das boas práticas, as IACS e as RAM, planeando intervenções de melhoria, (PPCIRA, 2018).
A evidência cientifica sugere que as mãos dos profissionais de saúde são o fator determinante para a transmissão destes MMR de uma pessoa para a outra, durante o processo da prestação de cuidados ou pelo contacto com superfícies contaminadas inerentes ao ambiente onde está alocado o doente, (CDC, 2017).
As principais medidas de prevenção das IACS devem fundamentar-se num conjunto de estratégias que englobam intervenções simples como a higiene das mãos, a limpeza e desinfeção das superfícies/equipamentos, a utilização adequada de Equipamentos de Proteção Individual. Mas também devem incidir na contenção dos microrganismos epidemiologicamente importantes através de medidas baseadas nas vias de transmissão, acautelando o isolamento dos doentes colonizados/infetados com este tipo de microrganismos. Różańska et al (2017) referem que a limpeza e a desinfeção ambiental têm influência significativa no controlo das IACS por MRSA. Compreender os mecanismos de resistência destes microrganismos, permite não só a criação de novos fármacos para o tratamento deste tipo de infeções, mas também a identificação de novas substâncias utilizadas no desenvolvimento de desinfetantes ou de materiais utilizados durante os cuidados de saúde, (Różańska et al, 2017). Estes autores, no seu estudo concluíram que um terço das amostras de Staphylococcus colhidas das superfícies das diversas unidades hospitalares, revelaram a presença da capacidade de produzir biofilme, o que sugere ser a causa da contaminação do ambiente hospitalar por esta bactéria, e por outro lado, concluíram que as superfícies de contacto compostas por liga de cobre podem ter um papel importante na redução da proliferação de bactérias no ambiente hospitalar (Różańska et al, 2017).
Um programa global de controlo de IACS deve abranger não só as áreas de prestação direta de cuidados, mas também as áreas de apoio e orientado por três vertentes: vigilância epidemiológica de estruturas, procedimentos e resultados (é importante cada instituição conhecer os riscos para a infeção, e quais os MMR mais prevalentes), recomendações de boas práticas (uso adequados de antimicrobianos, limpeza/desinfeção ambiental e de equipamentos, serviços hoteleiros,….) e formação contínua dos profissionais em função das necessidades identificadas, (Pina et al 2010).
Decorrente do exposto o estudo procura responder à seguinte questão de investigação:
Em articulação definiram-se os seguintes objetivos:
Identificar as IACS associadas ao uso de dispositivos invasivos (TET, CVC e CV) adquiridas na UCIP;
Calcular as Taxas de Incidência e a Densidade de Incidência das IACS relacionadas com o uso de TET, do CVC e do CV, na UCIP;
Calcular as Taxas de Exposição aos dispositivos invasivos TET, CVC e CV, na UCIP;
Descrever a tipologia de microrganismos existentes na UCIP;
Identificar os antimicrobianos mais prescritos na UCIP.
2. Métodos
O estudo equacionado para esta investigação engloba os métodos de análise quantitativa, garantindo a precisão dos resultados; insere-se no tipo de investigação não experimental, pois não se manipularam as variáveis em estudo; é um estudo, descritivo e analítico porque, visa descrever a amostra alvo deste estudo quanto ao padrão de Infeção no momento da admissão na UCIP e uso de antimicrobianos prévio a esse momento. Carateriza também as IACS diagnosticadas durante o internamento na UCIP, a exposição aos dispositivos invasivos (TET, CVC, Catéter urinário), os microrganismos identificados e a antibioterapia utilizada. É transversal, pois a colheita de dados decorreu num curto período de tempo.
Este artigo visa descrever diversos aspetos intrínsecos ao doente crítico, submetido a ventilação mecânica, em contexto de cuidados intensivos, abordando essencialmente uma das complicações mais graves consequente desta condição que são as IACS, bem como os microrganismos envolvidos e antimicrobianos utilizados.
2.1 Amostra
A população alvo incidiu sobre os doentes internados em UCI de um Centro Hospitalar, submetidos a ventilação mecânica e de forma retrospectiva foram analisados os registos clínicos correspondentes a um período de 6 meses situado entre, 1 de Julho a 31 de Dezembro, dos anos 2010, 2011 e 2012. A escolha deste período residiu na tentativa de procurar amostras similares, suportada na semelhança do tipo de doentes admitidos nas épocas dos anos em estudo.
O estudo teve por base, uma amostra não probabilísta, acidental, constituída por 162 adultos de ambos os géneros, internados numa Unidade de Cuidados Intensivos Polivalente de um Centro Hospitalar Central da zona Centro de Portugal, no período descrito anteriormente.
A UCIP é uma unidade mista, admite doentes do foro médico e cirúrgico, com uma ocupação total de 8 camas. Dos doentes admitidos a percentagem dos que são submetidos a ventilação mecânica é superior a 80%. Integra 40 profissionais de saúde (médicos, enfremeiros e assistentes operacionais). O “ratio” enfermeiro/doente é 1:2, sem alterações nos três trunos de 8 horas (manhã 8-16h; tarde 16-24h e noite 0-8h), nas 24 horas existe sempre um médico em presença física. Durante o desenrolar deste estudo a UCIP não sofreu alterações na sua estrutura física ou organizacional.
A amostra constituída por 162 doentes críticos internados em cuidados intensivos com idades compreendidas entre os 18 e os 88 anos, com uma média de idades de 64.34 anos (DP=15.151) e com uma distribuição moderada em torno da média (CV=23.55%).
O sexo feminino apresenta uma ordenação média sugestiva de uma idade superior, comparativamente com o sexo masculino, (OM=87.09 vs OM=79.61), no entanto sem significância estatística (U=2251.5; Z=-0.883; p=0.377).
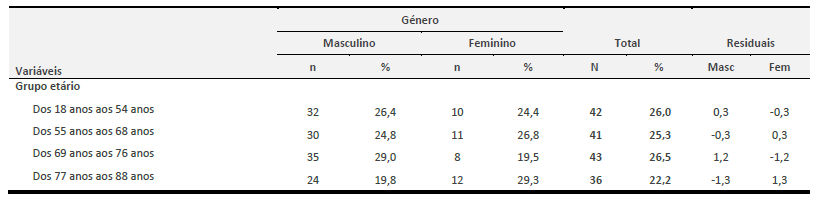
A idade foi recodificada em quatro grupos homogéneos, verificando-se que é no grupo etário dos 69 aos 76 anos que os homens estão mais representados face as mulheres (29.0% vs 19.5%), por sua vez nas mulheres o grupo etário mais representativo é o dos 77 aos 88 anos com 29.3%, (χ2=2.349; p=0.503), (cf. Tabela 1)
2.2 Instrumentos de recolha de dados
A colheita de dados foi efetuada no período de Julho de 2012 a Julho de 2013, tendo por base os processos clínicos dos doentes internados na UCIP nos períodos de 1 de Julho a 31 de Dezembro de 2010, 2011 e 2012.
A colheita de dados foi suportada numa Grelha Clínica de Cunha e Coelho (2012), construída para o efeito, na qual foram registados os dados relativos aos doentes internados na UCIP, nos períodos descritos anteriormente, e que respeitavam os critérios de inclusão no estudo.
Esta grelha divide-se em 2 partes:
1.Caracterização Geral: Refere-se à caracterização dos doentes internados na UCIP, nomeadamente em termos de género, idade, tempo de internamento hospitalar antes da admissão nos cuidados intensivos e tempo de internamento na UCIP, proveniência, motivo admissão, encaminhamento e alta clínica.
2.Caracterização do padrão da infeção e antibioterapia, corresponde ao levantamento de dados acerca da exposição a dispositivos invasivos como TET e ventilador, o CVC, o cateter urinário, a presença de infeção na admissão na UCIP, a existência de antibioterapia prévia ao internamento nesta unidade, diagnóstico de IACS, antibioterapia instituída para o tratamento dessas infeções e o microrganismo responsável.
2.3 Critérios de Inclusão
Como critérios de inclusão dos participantes no estudo definiu-se estar internado na UCIP, submetido a ventilação mecânica num período superior ou igual a 48 horas, com internamento no serviço superior ou igual a 72 horas. De um total de 361 doentes admitidos na UCIP nos últimos semestres de 2010, 2011 e 2012, foram excluídos do estudo 199 doentes por não apresentarem estes critérios.
2.4 Procedimentos
O estudo obteve parecer favorável da Comissão de Ética da ESSV, e o procedimento de recolha de dados foi autorizado pelo Concelho de Administração da Instituição selecionada.
Para a caracterização e descrição da amostra utilizou-se o programa Statiscal Package Social Science 19 para o Windows, o Excel e Word Microsoft.
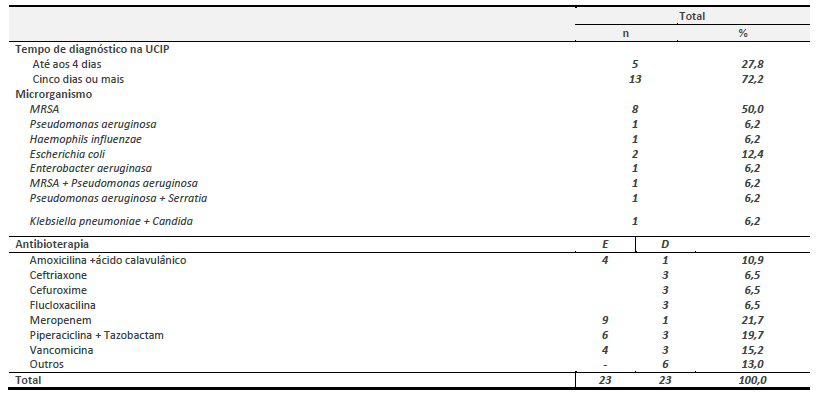
Com o intuito de descrever as principais características dos participantes e examinar a distribuição dos valores das principais variáveis, a análise descritiva dos dados utiliza as seguintes medidas: Frequências absolutas (n) e percentuais (%); Medidas de tendência central: Médias (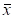 ) e Medidas de dispersão ou variabilidade: Desvio padrão (DP) e Coeficiente de variação (CV).
) e Medidas de dispersão ou variabilidade: Desvio padrão (DP) e Coeficiente de variação (CV).
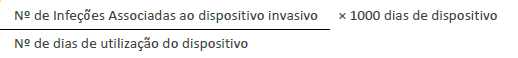
Foram calculados indicadores importantes no contexto das infeções associadas a dispositivos invasivos, nomeadamente a Densidade da IACS (correlacionando o número de IACS-pneumonia associada à ventilação/entubação ou infeção da corrente sanguínea associada ao CVC ou infeção do trato urinário associada ao cateter vesical) com o número de dias de utilização do dispositivo invasivo) e a Taxa de Exposição ao fator de risco (ventilador e TET; CVC e cateter vesical).Estes indicadores foram calculados com base nas seguintes fórmulas a) e b),:
3. Resultados
As variáveis referentes às condições de admissão e alta na UCIP correspondem ao tempo de internamento hospitalar no Centro Hospitalar antes da admissão na UCIP, tempo de internamento na UCIP, proveniência, o motivo de admissão e o encaminhamento e alta.
A análise do tempo de internamento hospitalar no Centro Hospitalar antes da admissão na UCIP, mostra que o tempo médio foi de 4,47 dias (DP = 7.290), variou entre 0 dias e um máximo de 50 dias.
Quanto ao tempo total de internamento na UCIP, ao longo dos últimos semestres dos três anos em estudo verificou-se que em 2010 foi de 896 dias, no ano de 2011 foi de 766 e em 2012 correspondeu a total de 571 dias, correspondendo a um total de 2233 dias de internamento. O tempo médio de internamento na UCIP foi de aproximadamente 14 dias (DP=12.080), variando entre mínimo de 3 dias e um máximo de 71 dias, apresentando uma dispersão elevada em torno da média (CV=87.66%), (cf. Tabela 2).
No período em estudo não existe diferença significativa no tempo médio de internamento prévio à UCIP, bem como no tempo de internamento nesta unidade, entre homens e mulheres (p>0.05), (cf. Tabela 2).
Tabela 2 Estatísticas relativas ao tempo de internamento no Centro Hospitalar, antes da admissão na UCIP, e do tempo de internamento na UCIP em função do género
Nota. O tempo de internamento corresponde à contabilização em dias. UCIP-Unidade de Cuidados Intensivos Polivalente
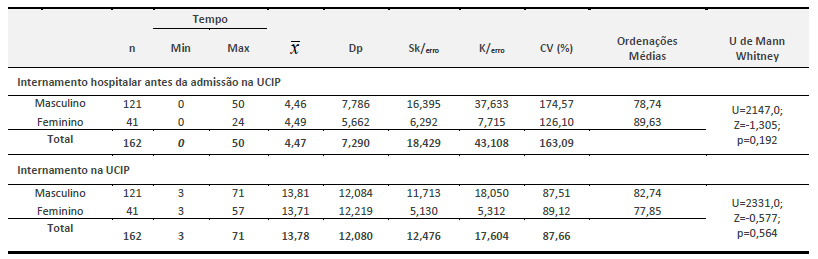
Relativamente à Proveniência dos doentes, a maioria é admitida na UCIP através de outro serviço do hospital (35.8.0%), com patologia médica (53,1%). O Bloco operatório (35.2%) e o serviço de urgência (26.5%) são outros serviços de proveniência dos doentes críticos, em que 42,6% dos doentes são admitidos com patologia cirúrgica, e somente 4,3% são doentes vítimas de Trauma/Intoxicação. Quanto ao encaminhamento e alta dos doentes, 75.9% tem alta clinica dos cuidados intensivos para outro serviço do Centro Hospitalar, 6.2% tem alta clinica para outro hospital e 17.9% acabam por falecer nos cuidados intensivos, (cf. Tabela 3).
O valor residual revela que as diferenças entre homens e mulheres não são significativas em relação às variáveis analisadas, (cf.Tabela 3).
Tabela 3 Caracterização quanto às condições de admissão e alta em função do género
Nota. CH=Centro Hospitalar
Padrão das Infeções e antibioterapia
A avaliação da situação dos doentes face à problemática da infeção prévia à admissão na UCIP e às IACS adquiridas durante o internamento nesta unidade corresponde por isso ao estudo de variáveis como infeção antes do internamento na UCIP e à antibioterapia prévia à admissão nesta unidade, às IACS adquiridas na UCIP, incluindo o estudo da IRAV, os microrganismos responsáveis e a antibioterapia instituída. E também inclui o estudo sobre a exposição dos doentes internados na UCIP a dispositivos invasivos, como o TET e ventilador, CVC e cateter urinário.
Infeção e Antibioterapia prévia à admissão na UCIP
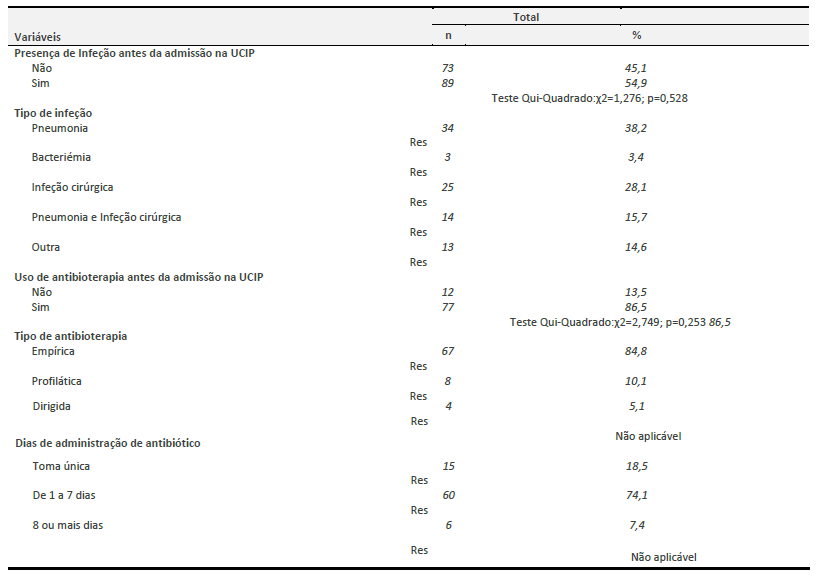
A análise de dados clínicos relacionados com a presença ou não de infeção dos doentes antes de serem admitidos na UCIP revelou que a maioria já apresentava infeção (54.9%), sendo mais frequentes a infeção respiratória (pneumonia) (38.2%) e a infeção cirúrgica (28.1%).
Observou-se que 86.5% dos doentes admitidos na UCIP foram submetidos previamente a antibioterapia, de forma empírica (84.8%) e durante 1 a 7 dias (74.1%), (Tabela 4).
IACS adquiridas durante o internamento na UCIP
Os dados presentes na Tabela 5 são relativos à caracterização das IACS adquiridas durante o internamento na UCIP. Desta forma observou-se que apenas 26 doentes adquiriram infeção associada a dispositivos invasivos (16.0%). A maioria das infeções é do sistema respiratório (69.2%), as restantes correspondem à INCS associada ao CVC e à ITU associada ao CV, que surgiram em igual número, 15,4% cada, com Densidade de Infeção de 2.25/1000 dias de CVC e 1,82/1000 dias de CV, respectivamente. Os microrganismos mais frequentes identificados foram o Staphilococus aureus meticilino-resistente (MRSA) (45.8%) e a Escherichia coli (12.4%). A antibioterapia foi aplicada em 96.2% dos doentes, na sua maioria entre 1 e 7 dias (69.2%) e foi usada de forma dirigida ao tipo de microrganismo responsável pela infeção (65.2%). Não se observaram diferenças significativas em relação ao ano de internamento, sendo os valores semelhantes entre os três anos, (cf. Tabela 5).
Infeção Respiratória Associada à Ventilação, tempo de diagnóstico, microrganismo causal, antibioterapia e densidades da infeção
Ao analisar os dados das IACS adquiridas na UCIP, verificou-se que a Infeção Respiratória Associada à Ventilação é a mais incidente e por essa razão considerou-se pertinente fazer uma análise mais aprofundada de alguns dados.
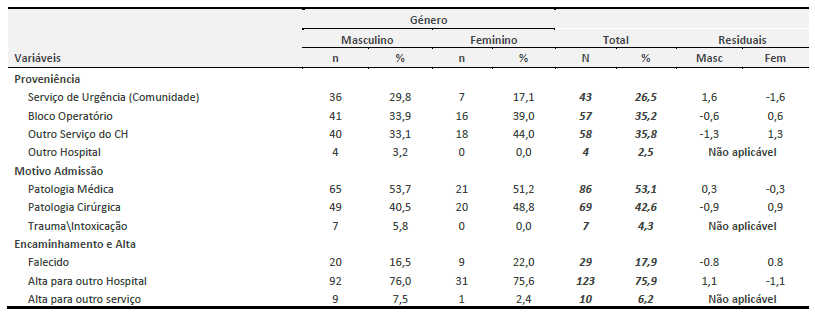
Analisou-se o tempo (em dias) decorrido desde a exposição do doente ao TET e ventilação mecânica invasiva até ao diagnóstico da IRAV. Verificou-se que o diagnóstico da infeção respiratória foi na sua maioria superior a cinco dias (72.2%), (cf. Tabela 6). Ao calcular a Densidade da IRAV verificou-se que na amostra global esse valor foi 10,5/1000 dias de ventilação. Em metade dos doentes com infeção respiratória o agente causal foi o microrganismo MRSA e em 12.4% foi a Escherichia coli, observando-se uma distribuição semelhante em relação aos microrganismos responsáveis pela IRAV nos três anos em estudo, (cf. Tabela 6).
Quanto à antibioterapia instituída para o tratamento da IRAV, verificou-se que o meropenem foi o antimicrobiano mais utilizado (21,7%), seguido pela piperaciclina + tazobactam (19,7%) e pela vancomicina (15,2%). Adicionalmente o antimicrobiano mais utilizado como terapia empírica é o meropenem, (cf. Tabela 6).
Tabela 6 Caracterização do tempo de diagnóstico da infeção Respiratória Associada à Ventilação na UCIP, microrganismo responsável e antibioterapia
Nota, MRSA =Staphilococus aureus meticilino-resistente, E=antibioterapia empírica, D=antibioterapia dirigida, outros corresponde aos antimicrobianos como a ampicilina, amicacina, ciprofloxacina, linezolide e tigeciclina.
Dispositivos invasivos e tempo de exposição
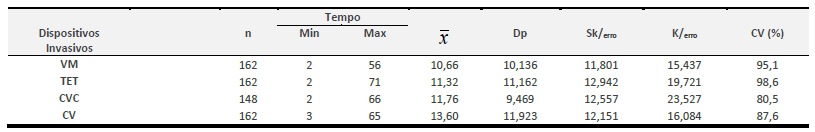
Na amostra calculou-se um total de 1717 dias de ventilação mecânica, constatou-se que o tempo médio de exposição à ventilação mecânica invasiva variou entre o mínimo de dois dias e um máximo de 56 dias, com um valor médio de cerca de 11 dias (DP=10.136), com uma dispersão elevada em torno da média (CV=95.1). A Taxa de Exposição ao ventilador na amostra corresponde a 0,76.
O tempo de exposição total ao TET da amostra correspondeu a 1828 dias, verificou-se que em média os doentes estiveram expostos a este dispositivo cerca de 11 dias, variando entre 2 dias e 71 dias de utilização deste dispositivo, correspondendo a uma Taxa de Exposição de 0,81.
A análise relativa à utilização de dispositivos invasivos para além do TET evidencia que em média os doentes mantiveram, o cateter venoso central cerca de 12 dias (DP=9.469) e o cateter vesical cerca de 13 dias (DP=11,923, (cf. Tabela 7). O tempo total que os doentes da UCIP foram submetidos ao CVC correspondeu a 1773 dias, o que equivale a uma Taxa de Exposição de 0,79, enquanto que o CV foi utilizado num total de 2190 dias, significando uma Taxa de Exposição a este dispositivo de 0,98.
4. Discussão
A temática central deste estudo é a infeção, mais especificamente as IACS, associadas ao uso de dispositivos invasivos, como o TET e Ventilação Mecânica, CVC e CV, bem como os microrganismos envolvidos e antimicrobianos utilizados, em contexto de cuidados intensivos.
As IACS são uma das complicações mais comuns e preocupantes que podem afetar a pessoa quando admitida numa unidade hospitalar ou outra instituição de saúde.
As IACS estão associadas a tempo de internamento hospitalar prolongado e taxas de morbilidade e mortalidade aumentadas, inflacionando também os custos a nível socioeconómico e familiar. Bonten
(2011) refere que as UCI são os serviços com maior probabilidade para a ocorrência de IACS e resistência à antibioterapia, sendo os profissionais de saúde confrontados com a gravidade do estado clínico dos doentes e com a sua susceptibilidade para a aquisição de IACS.
A IRAV é considerada a IACS mais comum nas UCI, estando associada a taxas de mortalidade que variam entre 20% a 70%, e quando causadas por microrganismos multirresistentes ou associadas ao uso de antibioterapia inadequada, os resultados são menos favoráveis, (Resende et al, 2013).
No Relatório Epidemiológico Anual do ECDC, com base nos dados de 2017, constatou-se que cerca de 8,3% (11787) dos doentes admitidos na UCI, por um período superior a dois dias, adquiriu pelo menos uma IACS em estudo (IRAV, INCS associada ao CVC e ITU associada ao CV), (ECDC, 2019). Também concluiu que 97% das pneumonias estavam associadas à intubação, 37% das INCS foram relacionadas com o uso de CVC e 98% das ITU foram associadas ao uso de cateter vesical, (ECDC, 2019).
Perante este cenário é essencial reduzir o uso de dispositivos invasivos para prevenir a infeção e minimizar a transmissão cruzada, (Bonten, 2011). A problemática da resistência aos antimicrobianos é superior nas UCI, maioritariamente associada à severidade da situação clínica dos doentes, ao uso frequente de antibióticos e à heterogeneidade na implementação das medidas de prevenção e controlo das IACS, (ECDC, 2019).
Este estudo inclui doentes internados numa UCIP, que pertence a um Centro Hospitalar da zona centro de Portugal, submetidos a ventilação mecânica num período superior ou igual a 48 horas, com três ou mais dias de internamento nesta unidade. Na amostra a idade média corresponde aos 64,31 anos. Os homens têm maior representatividade em relação às mulheres, corresponde a 74,7% dos doentes estudados, mas as mulheres apresentam em média idades mais elevadas. Diversos estudos que abordam esta temática, analisam várias características demográficas dos doentes intervenientes, e o género masculino, surge como dado de referência, e na sua maioria é aquele mais representado nos casos com IACS. No estudo quasi-experimental de Caserta et al (2012), realizado numa UCI médico-cirúrgica, numa amostra total de 5422 doentes, cerca de 58,2% pertenciam ao género masculino, em que a média de idades era superior aos 65 anos. Mais recentemente, no estudo observacional e prospectivo de Wang, L., Zhow, K-H., Chen, W., Yu, Y. & Feng, S-F. (2019), desenvolvido em UCI, no período de 2013-2015, constatou-se que na totalidade de 1347 doentes, 66,3% pertenciam ao género masculino e a média de idades correspondia a 58,6 anos (DP=17,1).
A UCIP admite doentes do foro médico e cirúrgico, é uma unidade mista. Nos anos em estudo verifica-se que a proveniência dos doentes, corresponde em grande parte a outro serviço do Centro Hospitalar (35,8%), seguida do Bloco Operatório com 35,2% dos doentes admitidos. Quanto aos motivos de admissão é maioritariamente devido a patologia médica (53,1%). A maioria dos doentes são transferidos com alta para outro serviço da referida unidade hospitalar (75,9%), sendo a taxa de mortalidade 17,9%.
A WHO (2011) refere que os fatores de risco para as IACS dependem do tipo de instituição de saúde e o tipo de serviço onde é admitido o doente, em que a idade superior a 65 anos e o internamento numa UCI são descritos como fatores de risco mais comuns para a ocorrência de IACS.
Bonten (2011) explica que durante o internamento na UCI, muitos doentes passam por um período de imunodepressão induzido por uma patologia grave, muitos têm diversas co-morbilidades associadas à sua situação clínica grave e a maioria é submetido a dispositivos invasivos, como a entubação endotraqueal e dispositivos intravasculares, quebrando as barreiras de defesa naturais do hospedeiro.
Neste estudo verifica-se que a grande maioria dos doentes é submetido a outros dispositivos invasivos para além do TET e do ventilador. Nos três anos a totalidade dos doentes é submetido à algaliação vesical, bem como a grande maioria, 148 dos 162 doentes críticos em estudo (91,3%) foi sujeito à utilização de CVC. Num estudo de Vigilância Epidemiológica Ativa em UCI mista, num período de um ano, também é identificada a exposição significativa dos doentes a este tipo de dispositivos, em que 70% foram submetidos a ventilação mecânica, 58% foram expostos a CVC e na maioria dos casos (99%) recorreu-se à cateterização vesical, (Iordanou, S., Middelton, N.,Papathonossoglou, E. e Raftopoulos, V. (2017).
Com base em diversos estudos, Iordanou et al (2017) referem os procedimentos cirúrgicos, a utilização de dispositivos invasivos, o uso de antimicrobianos e o tempo de internamento como os principais fatores de risco para as IACS. A existência de co-morbilidades, tais como a desnutrição, doença pulmonar obstrutiva crónica, sinusite crónica e higiene oral pobre são descritos como fatores de risco adicionais para a instalação da IRAV, (Lawrence e Fulbrook, 2011). Outros autores definem outro tipo de co-morbilidades (cardíacas, pulmonares, renais, a diabetes, vasculares, neoplásicas e hepáticas) que podem predispor o doente a desenvolver complicações como a infeção, (Quartin, Scerpella, Puttagunta & Kett, 2013).
O presente estudo não aborda as co-morbilidades dos doentes participantes, a colheita de dados cinge-se apenas ao motivo de admissão e não explora a situação clínica especifica que motivou ao internamento na UCIP, bem como os antecedentes patológicos desses indivíduos. Admite-se que estes aspetos sejam importantes para uma caracterização mais completa e aprofundada da amostra em estudo, considerando-se como uma limitação desta investigação a sua omissão.
Este estudo analisa essencialmente os fatores de risco para as IACS extrínsecos ao doente, tais como o tempo de exposição aos dispositivos invasivos, como o TET e a Ventilação Mecânica, o CVC e o CV, mas também analisa a situação prévia, dos doentes críticos, à admissão na UCIP, quanto aos dias de hospitalização e submissão a antibioterapia, acreditando-se que é nestes fatores que a mudança das práticas pode diminuir a incidência deste tipo de infeção, ao contrário dos fatores intrínsecos ao doente, que são pouco modificáveis.
Na UCIP, no período em estudo, 26 doentes (16%) desenvolveram IACS durante o internamento, verificando-se também uma diminuição destes valores ao longo dos três anos.
Um dos principais resultados deste estudo consiste na identificação da IRAV como a IACS mais incidente, 18 doentes (69,2%) dos 26 que adquiriram IACS; em segundo plano ficam a infeção nosocomial da corrente sanguínea associada ao CVC e a infeção do trato urinário associada ao cateter vesical, ambas com 15,4% de taxa de incidência. No estudo analítico, descritivo e prospectivo de Resende et al (2013) referem que a pneumonia associada à ventilação é a infeção nosocomial mais comum nas UCI, cuja incidência varia entre 9% e 27% dependendo do tipo de população, do tipo de UCI e os critérios de diagnósticos aplicados. Estes autores estudaram uma amostra de 126 doentes, submetidos a VM por mais de 48 horas, em que 26,2% destes desenvolveram IRAV. No presente estudo a taxa de incidência de IRAV é menor, verifica-se que na amostra, 18 doentes desenvolveram IRAV, correspondendo a uma percentagem de 11,1%. Iordanou et al (2017), no seu estudo obtiveram resultados diferentes, neste caso a INCS associada ao CVC foi a mais incidente, com um taxa de 48,8% de todas as IACS associadas a dispositivos invasivos, a IRAV ficou em segundo plano com 37,2% dos casos e a ITU com 14%.
Para além de analisar as taxas de incidência da IACS, este estudo também calcula a densidade deste tipo de infeções que consiste na relação entre o número de IACS e o número de dias totais de utilização do dispositivo invasivo, o ventilador e TET, CVC e o CV (fatores de risco extrínsecos ao doente). A nível internacional, diversos estudos utilizam os valores da densidade da infeção, permitindo comparar dados. O National Healthcare Safety Network (NHSN) é um programa norte-americano de Vigilância Epidemiológica assente numa metodologia padronizada, que permite comparar resultados por densidades de incidência e classes de risco (tipo de unidades), (CCI, 2013). A nível europeu existe o programa de monitorização da infeção designado Hospitals in Europe Link for Infection Control (HELICS) que também se foca neste tipo de estudos. A UCIP participa neste programa desde o ano de 2004.
No presente estudo, a análise da densidade de IRAV por 1000 dias de ventilação, mostra que a densidade desta infeção corresponde a 10,5/1000 dias de ventilação. Estes resultados refletem os dados obtidos através da Vigilância Epidemiológica que é realizada durante todo o ano na UCIP, englobando todos os doentes admitidos. Nos três anos em estudo, quando comparada com os dados de 2011 do NHSN é superior ao percentil 90 (4.3 por 1000 dias de ventilação), (CCI, 2013). Ao comparar com os dados de 2011 do HELICS-UCI, também se observa uma semelhança nos valores obtidos neste estudo e a média nacional da densidade da IRAV (número de IRAV/1000 dias de entubação) que corresponde a 8,9/1000 dias de entubação, (Paiva, Pina e Silva, 2013). Dados mais recentes do PPCIRA, no período de 2013 a 2017, a Densidade da IRAV decresceu de 7,4/1000 dias de entubação para 6,6/1000 dias de entubação nas UCI Portuguesas que participam na VE em Rede Europeia e que correspondem a uma cobertura da maioria (68,18%) das UCI a nível nacional, (PPCIRA, 2018). Um dado importante do relatório do ECDC (2018) aponta a média nacional de 7,2/1000 dias de entubação, comparativamente inferior à média Europeia (9.5/1000 dias entubação).
A Densidade da INCS associada ao CVC correspondeu a 2,25/1000 dias de CVC nos três anos em estudo, que comparada com os dados do NHSN, é superior ao percentil 75 (1,1 por 1000 dias de CVC). O mesmo constatou-se no caso da ITU associada ao uso de CV, com uma Densidade de 1,82/1000 dias de CV, igualmente superior ao percentil 75 do NHSN (1,6/1000dias de CV). De acordo com o CDC (2013) é importante as instituições de saúde/unidades identificarem em que patamar (percentil) se situam face a cada tipo de IACS associada aos dispositivos invasivos, caso esses valores superem o percentil 50 (media) e se aproximem do percentil 90, podem sugerir a existência de um problema que requer uma intervenção adequada. O sistema de vigilância epidemiológica do PPCIRA monitoriza a incidência de infeções relacionadas com cateter venoso central através de dois programas o Hospital Acquired Infection (HAI)-ICU e o Infeção Nosocomial da Corrente sanguínea (INCS). Os dados do Relatório do PPCIRA (2018) mostram que a Densidade das INCS associadas ao CVC diminuíram no período de 2013 a 2017, evoluindo de 1,3 para 0,9/1000 dias de CVC nas UCI portuguesas. E comparando os dados de 2017, a média da Densidade desta infeção nas UCI portuguesas foi 1,7/1000 dias de CVC, inferior à média Europeia (3/1000 dias de CVC), (ECDC, 2018). O estudo prospetivo de Bianco, A., Capano, MS, Mascaro, V., Pileggi, C., & Pavia, M. (2018), numa UCI, no período de 2013-2016, com uma amostra de 1283 doentes, revelou que 89,5% das bacteriemias corresponderam a INCS associadas ao CVC, com uma Densidade de Infeção de 7,7/1000 de CVC (superior ao percentil 90 do NHSN), dados menos favoráveis em relação àqueles obtidos na UCIP. No entanto, Bianco et al (2018) identificam uma Densidade de ITU associada ao CV de 1,6/1000 dias de CV (percentil 25-50 do NHSN), enquanto neste estudo obtiveram-se valores ligeiramente mais elevados (1,82/1000 dias de CV). Os dados mais recentes, a nível europeu, descrevem que em média a Densidade da ITU associada ao CV foi de 3,6/1000 dias de CV no ano de 2017, (ECDC, 2019).
Outra questão pertinente centra-se no tempo a que os doentes são submetidos a determinado dispositivo invasivo, e vários estudos constatam que quanto maior esse período de tempo, maior será o risco de se instalar um processo de infeção associado ao mesmo. Pina et al (2010) explicam que dispositivos, como o TET, o CVC ou CV, criam um desequilíbrio nos mecanismos de defesa natural do organismo, abrindo portas de entrada artificiais para os microrganismos. O CDC (2013) considera pertinente que o estudo da Densidade de incidência da IACS deve ser acompanhado pela análise do tempo de exposição aos respetivos dispositivos. Neste estudo também foram calculadas as Taxas de Exposição aos dispositivos invasivos, com o intuito de se avaliar mais objetivamente o tempo que os doentes da UCIP são submetidos a estes fatores de risco, e de alguma forma contribuir para a melhoria na prática clinica, tentando reduzir a sua utilização. Constatou-se que o CV foi o dispositivo com Taxas de exposição mais elevadas (0,98), ficando em segundo plano o TET com 0,81 e o CVC foi o dispositivo com taxas mais baixas (0,79), no entanto todas elas superiores ao percentil 90 do NHSN (0,81;0,44 e 0,63 respetivamente), (NHSN, 2013). No estudo de Iordanou et al (2017) verificou-se a mesma tendência, o CV foi o dispositivo com taxa de utilização mais elevada (99%), com uma taxa de exposição de 0,99, de seguida o TET e o CVC, com taxas de 0,70 e 0,58 respetivamente. No estudo de Bianco et al (2018), explicam que a elevada incidência de INCS associadas a CVC (7,7/1000 dias de CVC) poderá estar relacionada com a taxa de exposição elevada a este dispositivo, superior ao percentil 90 do NHSN. No entanto, associam a incidência baixa de ITU associada ao CV, com a eficácia das intervenções implementadas, tais como: formação dos profissionais, redução da cateterização vesical, definição rigorosa das razões para o uso do CV e revisão diária da necessidade do CV, (Bianco et al, 2018). Huis et al (2020) referem que aproximadamente 65% das ITU associada ao CV, 55% das INCS associadas ao CVC e 55% das IRAV são possíveis de prevenir com base na implementação de estratégias preventivas baseadas na evidência científica.
Mas estas medidas devem ser complementadas pela vigilância contínua das IACS relacionadas com o uso de dispositivos, por parte das equipas ou instituição, possibilitando o acesso contínuo da efetividade das medidas implementadas, a identificação precoce de situações problemáticas, bem como a obtenção de dados para comparação ou “Benchmarking”, (Bianco et al, 2018). No Inquérito realizado por Huis et al (2020), com objetivo de avaliar, perante as equipas de Prevenção de Infeção dos Hospitais de Agudos Holandeses, que tipo de monitorização era realizada às IACS relacionadas com o uso de dispositivos invasivos, concluíram que a INCS associada ao CVC foi a IACS sujeita a maior monitorização pelas instituições (95,4% dos casos), seguida pela IRAV com 26,2% e a ITU surgiu como a IACS menos implicada nas medidas de vigilância por parte das equipas. Estes autores explicam que a diferença observada devia-se essencialmente aos seguintes aspetos: o uso de CVC acontece quase exclusivamente no contexto de cuidados intensivos, enquanto que o uso de CV é mais generalizado, e respetivas medidas preventivas e monitorização teriam que ser implementadas com base numa iniciativa da instituição, envolvendo as diferentes unidades/enfermarias, (Huis et al, 2020). Por outro lado, a monitorização da INCS associada ao CVC esteve facilitada pelo fato de a nível nacional existir um programa de Vigilância bem estabelecido, com critérios rigorosos de monitorização baseados no ECDC, (Huis et al, 2020). Por fim, a monitorização reduzida da IRAV, fundamentou-se em questões não resolvidas acerca dos critérios de definição e diagnóstico que devem ser aplicados perante esta complicação, (Huis et al, 2020).
No caso particular da UCIP, alvo deste estudo, desde o ano de 2004 participa e debita dados no programa de VE em rede europeia designado HELICS, e realiza em paralelo a VE em colaboração com a Comissão de Controlo de Infeção e Resistências aos Antimicrobianos do Centro Hospitalar no levantamento de dados relativos às IACS associadas ao TET, CVC e CV, bem como ao uso de antibioterapia e microrganismos envolvidos, (CCIRA, 2017). Quanto à implementação de boas práticas, no ano de 2012 foi implementada a “Bundle” de prevenção da IRAV na UCIP, constatando-se que o maior desafio reside na motivação dos profissionais para a adesão ao conjunto de medidas a longo prazo, bem como todo o processo de vigilância/auditorias que esta metodologia de trabalho implica. A partir do ano de 2019 reuniram-se esforços com o intuito de se implementarem os “Feixes de Intervenções” da DGS (2015) para a prevenção das IACS associadas ao TET, CVC e CV, que, atualmente, ainda se encontram numa fase embrionária.
Quanto aos microrganismos responsáveis pelas IACS diagnosticadas neste estudo foram maioritariamente o Staphylococcus aureus Meticilino-Resistente (45,8%), a Escherichia coli (12,4%), e a Enterobacter aeroginosas (8,4%). Observou-se também casos em que existiam mais do que um agente causal para o mesmo episódio de infeção, por exemplo MRSA e a pseudomonas aeruginosa ou pseudomonas aeruginosa, Escherichia coli e candida correspondendo a 4,2% dos casos, respectivamente. No estudo de Bianco et al (2018) constatou-se que no grupo de bactérias Gram negativo as mais comuns foram Klebsiella pneumoniae (17.8%), Acinetobacter baumannii (10.2%), Escherichia coli (8.5%), e no grupo de bactérias Gram positivo o Staphylococcus epidermidis (10%) foi o mais incidente como agente causal das IACS. Estes autores no seu estudo descrevem que cerca de 66,6% de Staphylococcus epidermidis eram resistentes à Meticilina, e 52,3% de Klebsiella pneumoniae e 30% de escherichia coli eram resistentes às cefalosporinas de 3ª geração (cefotaxime e ceftazidime).
Neste estudo, grande parte dos microrganismos identificados revelaram algum tipo de resistência a antimicrobianos, mais especificamente a resistência à Meticilina. O PPCIRA (2017) refere que em Portugal o perfil de resistências de diversos microrganismos tem vindo a diminuir: o MRSA teve uma diminuição de 20%, desde 2011 até 2016 (54,6% para 43,6% respetivamente), a Escherichia coli resistente a quinolonas demosntrou tendência a decrescer de 2013 a 2016, mas com uma percentagem de 30,2% (superior à média europeia, 21%), o Acinetobacter baumannii com resistência combinada a fluroquinolonas, aminoglicosídeos e carabapenemos também diminuiu de 64,3% em 2013 para 37,9% em 2016 (superior à média da Europa, 31,7%).Um dado preocupante refere-se à proporção de isolados de Klebsiella pneumoniae resistentes aos carbapenemos, que teve um aumento de 73% do ano de 2015 para 2016, refletindo a tendência europeia, (PPCIRA, 2017).
Relativamente aos microrganismos responsáveis pela IRAV isolados neste estudo, o que surge em maior número nos três anos é o Staphylococcus aureus meticilino-resistente (50%), seguido da Escherichia coli (12,4%) e Pseudomonas aeruginosa (6,2%). Estes dados refletem os resultados obtidos através da Vigilância Epidemiológica da UCIP, sendo o Staphylococcus aureus o mais incidente nos casos de IRAV, com um perfil de resistência aos antimicrobianos entre os 40 a 50%, ou seja, em cerca de metade dos casos de IRAV causada por Staphylococcus aureus, estes eram meticilino-resistentes, (CCI, 2013). Ao comparar com outros estudos verifica-se uma diversidade de microrganismos isolados, em alguns deles são coincidentes com este estudo, como no caso do estudo de Arroliga et al (2012) em que a bactéria identificada em maior número nos doentes com IRAV foi o Staphylococcus aureus, sendo 22% meticilino-resistente e 18% meticilino-sensível, seguidos pela pseudomonas aeruginosa (12%).
Enquanto em outros estudos é identificada uma maior incidência de microrganismos gram-negativos, como no estudo de Resende et al (2013), identificaram como principais responsáveis pela IRAV a pseudomonas aeruginosa e o Acinectobacter spp, ambos em 34,4% das infeções, seguidos pelo Staphylococcus aureus em 15,6% dos casos. Quanto aos perfis de resistências, relatam multirresistências aos antimicrobianos entre os 70 a 80%, (Resende et al, 2013). No estudo de Caserta et al (2012), 80% dos microrganismos identificados eram gram-negativos, sendo 40% pseudomonas aeruginosa, para além desta surge o Acinectobacter baumannii como os mais prevalentes.
O ECDC (2019), reporta no Relatório Epidemiológico Anual das IACS em UCI, os microrganismos mais comumente isolados foram a Pseudomonas aeruginosa no caso das pneumonias, o Staphylococcus coagulase-negativo nas INCS e a Escherichia coli nos casos de ITU. Também descrevem os níveis de resistência de diversos microrganismos, em que 64% de Acinetobacter baumannii e 26% de Pseudomonas aeruginosa eram resistentes aos Carbapenemos, em casos de infeções por Klebsiella spp 40% destes microrganismos eram resistentes às Cefalosporinas de 3ª geração e 24% dos Staphylococcus aureus eram Meticilino-resistentes.
O tempo que decorre desde o início da exposição ao TET e ventilador até à instalação da IRAV é um dado epidemiológico importante e um fator de risco para a presença de determinados microrganismos e consequentes resultados do doente, (American Thoracic Society, 2005). A infeção respiratória é considerada como estando associada à ventilação se o doente estiver pelo menos 48 horas exposto ao TET e ventilador antes de existirem sinais de infeção, não está determinado um tempo mínimo de exposição para que a infeção respiratória seja considerada como associada à ventilação, (Lawrence & Fulbrook, 2011). Estes autores, consideram a IRAV de início tardio quando se instala a partir das 72 horas ou mais após a intubação. A ATS (2005) por sua vez, classifica a IRAV como precoce quando se inicia até 4 dias após exposição ao TET e ventilação, e tardia se a infeção acontece após 5 dias ou mais. Esta classificação do tipo de IRAV é importante porque pode predizer o tipo de microrganismo causal envolvido. Nas situações de início precoce frequentemente os microrganismos envolvidos correspondem aos adquiridos na comunidade, como o Strepttococus pneumoniae e Haemophilus influenzae, com melhores prognósticos, enquanto a IRAV tardia na maioria dos casos envolve microrganismos multirresistentes à antibioterapia, como o caso do Staphylococcus aureus, Acinectobacter baumannii e Pseudomonas aeruginosa, associada a taxas de mortalidade e morbilidade mais elevadas, (Lawrence & Fulbrook, 2011).
Neste estudo também se analisou o tempo decorrido desde o início de exposição ao TET e ventilador e o dia em que se estabeleceu o diagnóstico de IRAV, e observa-se que na amostra global 72,2% dos casos o diagnóstico é estabelecido 5 dias ou mais depois da intubação. Sendo assim os resultados deste estudo coincidem com o que os autores referidos anteriormente afirmam, existem mais casos de IRAV tardias e o microrganismo responsável pela IRAV na maioria dos casos é o Staphylococcus aureus meticilino-resistente.
Em 96,2% dos casos de IACS foi instituída antibioterapia, na sua maioria como antibioterapia empírica (65,2%), denotando-se que apenas 34,8% correspondiam a antibióticos dirigidos ao agente causal. Quanto ao tempo de utilização verificou-se que 69,2% dos tratamentos teve duração de 1 a 7 dias, e os restantes (30,8%) 8 dias ou mais. Deve-se analisar estes dados com reservas, porque neste estudo foi apenas registado os dias de antibioterapia durante o internamento na UCIP, e muitos doentes após a alta mantinham a prescrição do antibiótico, não sendo possível contabilizar o total de dias de antibiótico para a situação específica. O tempo de duração da antibioterapia é um aspeto essencial, quando administrada em menos tempo que necessário, existe um maior risco de insucesso no tratamento e irradicação do microrganismo; quando em excesso pode estar associada à seleção de microrganismos resistentes, como também ao maior risco para situações adversas e maiores custos, (Vicent at al, 2010). Estes autores, tendo como referência as recomendações da ATS, explicam que a duração da antibioterapia pode ser determinada de acordo com a severidade da doença, a resposta clínica e o microrganismo envolvido, sendo de 7-14 dias para as infeções causadas por Staphylococcus aureus ou o Haemophilus influenzae, e de 14-21 dias para os casos que envolvem a pseudomonas aeruginosa, (Vicente et al, 2010). Tendo em conta a estas recomendações, o tempo de antibioterapia durante o internamento na UCIP observado neste estudo pode considerar-se como adequado.
Na análise mais aprofundada ao padrão de antibioterapia instituída no tratamento da IRAV, verificou-se que o meropenem e a piperaciclina+tazobactam foram os antibióticos mais utilizados, 21,7% e 19,7%, respetivamente e ambos com maior representatividade na terapia empírica. De acordo com o Relatório da VE do ano 2012, realizado pela CCIRA em colaboração com a UCIP, face ao padrão das resistências encontradas nos agentes infetantes, os protocolos de antibioterapia empírica para a IRAV deveriam incluir a Vancomicina e a Piperaciclina+tazobactam, tendo em conta as susceptibilidades encontradas. Como antibióticos dirigidos ao microrganismo causal o grupo mais utilizado corresponde a outros antimicrobianos como a ampicilina, amicacina, ciprofloxacina, linezolide e tigeciclina. Na maioria dos casos iniciam-se como terapia empírica e posteriormente passam a antimicrobianos dirigidos aos microrganismos identificados através de exames microbiológicos ao aspirado traqueal. Os resultados deste estudo diferem do estudo retrospectivo de Gonzalez et al (2013), realizado numa UCI, em que a antibioterapia empírica mais prescrita correspondia às quinolonas (48,7%), penicilinas do grupo A (43,2%) e cefalosporinas de 3ª geração (33,2%). Com este estudo estes autores conseguiram demonstrar que a redução do espectro de ação da antibioterapia empírica, na maioria dos casos foi possível, sem impactos clínicos negativos na UCI médica, (Gonzalez et al, 2013).
Vicente et al (2010) explicam que um dos fatores de sucesso no tratamento da IRAV é a antibioterapia direcionada para o organismo causal e deve ser instituída o mais precocemente possível, pois a antibioterapia inadequada ou atraso na sua instituição conduzem a resultados menos favoráveis. Os mesmos autores referem que assim que existe a suspeita de IRAV, a antibioterapia empírica deve ser instituída com base no histórico microbiológico da unidade/instituição e perfil de sensibilidades, na existência ou não de risco para a presença de microrganismos multirresistentes, e a partir do momento que se conheça o microrganismo responsável, deve dirigir-se a antibioterapia para a eliminação do mesmo, (Vicente et al, 2010). Com base no relatório Epidemiológico Anual de 2017, em UCI, o ECDC descreve que foram registados 484221 dias de terapia antimicrobiana, em que a maioria (57,8%) correspondeu a tratamento empírico, em 24,3% foi direcionado ao microrganismo causal e apenas 13,2% de terapia profilática.
Outro dado relevante apurado neste estudo, reside no fato de a maioria dos doentes admitidos na UCIP (86,5%) nos três anos é submetido a antibioterapia prévia ao internamento nesta unidade, e na maioria dos casos (84,8%) de forma empírica, a dirigida corresponde somente a 5,1% dos casos. E o tempo de duração decorre entre 1 a 7 dias em 74,1% dos doentes. Estes resultados são importantes, na medida em que num estudo prospectivo de coorte, num hospital universitário, envolvendo doentes com infeção, verificou-se que os doentes infetados com microrganismos multirresistentes tinham uma taxa significativamente elevada de antibioterapia inicial inadequada, (Cardoso, Ribeiro, Aragão, Costa-Pereira & Sarmento, 2012). Com este estudo estes autores identificaram fatores de risco adicionais para a IACS causada por microrganismos multirresistentes, nomeadamente idade superior a 60 anos, Índice de Karnofsky <70, hospitalização prévia no período de um ano, e antibioterapia prévia inadequada, referindo que estes podem trazer benefícios clínicos conduzindo a um diagnóstico precoce e diminuir o uso inadequado de antimicrobianos neste tipo de doentes, (Cardoso et al, 2012). Tendo em conta a este aspeto é importante conhecer o historial do doente face à administração de antibioterapia, para além de outros fatores de risco, a fim de se determinar mais adequadamente e em menor tempo possível a susceptibilidade dos doentes a este tipo de infeções.
No relatório que analisa as IACS e a resistência aos antimicrobianos no ano de 2013, Portugal não se situava entre os países europeus com maior consumo de antibióticos em ambiente hospitalar, no entanto os autores guardavam reservas em relação a estes dados, visto a colheita de dados ainda não estar normalizada, (Paiva et al, 2013). Relativamente aos antibióticos mais utilizados a nível nacional correspondiam às Penicilinas e às Cefalosporinas e outros beta lactâmicos, (Paiva et al, 2013). Os mesmos autores identificaram vários erros na utilização dos antibióticos a nível nacional, dois deles correspondiam ao tempo de duração da antibioterapia profilática cirúrgica, que na maioria dos casos era excessiva (superior ás 24h) e a duração da terapêutica antimicrobiana, que era excessiva em relação à duração mínima necessária para curar a infeção e evitar recidiva, (Paiva et al, 2013). Mais recentemente, o relatório do PPCIRA (2018) refere que o consumo global de antimicrobianos a nível nacional, em meio hospitalar, reduziu, de 2013 a 2017, 4,96% (de 1,64 DHD para 1,53DHD), devido à redução de utilização de quinolonas (-29,58%) e aminoglicosídeos (-19,43%).
O ECDC (2019) relembra que uma estratégia de intervenção eficaz e efetiva terá que englobar um reforço das medidas de prevenção e controlo das IACS associada à implementação de um programa de gestão da utilização dos antimicrobianos, envolvendo quer profissionais de saúde, quer os órgãos de gestão.
Conclusões
A IACS é uma das complicações mais graves e preocupantes que podem afetar o doente crítico em contexto de cuidados intensivos. Atualmente são vários os esforços no sentido de se desenvolverem várias estratégias para a prevenção deste tipo de infeção, diversos estudos demonstram estar associada a tempo de internamento na UCI e hospital prolongados, taxas de morbilidade e mortalidade elevadas e custos socioeconómicos acrescidos.
Apesar da diversidade de microrganismos identificados nos diferentes estudos, incluindo este estudo, constata-se uma tendência preocupante que é a incidência crescente de infeções causadas por microrganismos multirresistentes, evidenciando que as medidas de controlo das IACS devem estar cada vez mais interligadas com a prevenção da resistência aos antimicrobianos.
Com este estudo apurou-se que a maioria dos doentes admitidos na UCIP (86,5%) nos três anos é submetida a antibioterapia prévia ao internamento nesta unidade, e na maioria dos casos (84,8%) de forma empírica. A maioria das IACS na UCIP afeta o sistema respiratório (69.2%), as restantes correspondem à INCS associada ao CVC e à ITU associada ao CV, que surgiram em igual número, 15,4% cada, com Densidade de Infeção de10,5/1000 dias de ventilação, 2.25/1000 dias de CVC e 1,82/1000 dias de CV, respectivamente. Os microrganismos mais frequentes identificados foram o MRSA (45.8%), a Escherichia coli (12.4%) e a Enterobacter aeroginosa (8,4%). A antibioterapia foi aplicada em 96.2% dos doentes que adquiriram IACS, na sua maioria entre 1 e 7 dias (69.2%) e foi usada de forma empírica em 65.2% dos casos. Os doentes da UCIP estiveram mais expostos ao CV, com uma Taxa de Exposição de (0,98), ficando em segundo plano o TET com 0,81 e o CVC foi o dispositivo com taxas mais baixas (0,79).
Emerge do estudo ser crucial a diminuição das taxas de IACS por MMR, dependendo de cada instituição/unidade de saúde implementar um conjunto de intervenções consistente e ajustado à sua realidade. Por sua vez a redução das resistências aos antimicrobianos deve estar assente numa prática clínica adequada, baseada na melhor evidência científica e inserida na rotina diária dos profissionais de saúde, doentes e familiares.
Para tal considera-se relevante instituir boas práticas não só a nível da prestação dos cuidados de saúde, com a aplicação das precauções básicas de controlo de infeção, e as medidas baseadas nas vias de transmissão dos MMR. Mas também a nível organizacional deve ser implementada uma abordagem multimodal que englobe a monitorização contínua de resultados e de processo, uma participação ativa dos órgãos de gestão, formação contínua dos profissionais intervenientes, e acima de tudo, uma mudança na metodologia de trabalho entre as equipas com um objetivo comum: a segurança do doente.