Introdução
A gripe sazonal, definida como uma doença viral aguda das vias respiratórias causada pelos vírus Influenza A, B ou C, ocorre geralmente nos meses mais frios, correspondentes aos meses de Inverno de cada hemisfério1.
Na maioria da população cursa como uma doença benigna e autolimitada, manifestando-se por sintomas respiratórios e sistémicos, como o início súbito de febre alta, mal-estar geral, mialgias, poliartralgias, cefaleias e tosse seca2), (3. No entanto, em determinados grupos mais vulneráveis, como grávidas e puérperas (até duas semanas pós parto) (4, a gripe pode acarretar um maior risco de doença grave e de complicações materno-fetais, designadamente desidratação, pneumonia, doença cardiopulmonar, trabalho de parto prematuro e perda fetal4.
A presença do complexo feto-placenta condiciona o sistema imunitário materno no sentido da viabilidade fetal. A resposta imunitária após a infeção pelo vírus influenza, promove a resposta inflamatória pulmonar, com possível elevação da morbimortalidade. A função respiratória está alterada pela elevação diafragmática provocada pelo aumento uterino, pelas alterações na parede torácica e pelo aumento dos níveis de gonadotropina coriónica humana β e progesterona; aumenta ainda o consumo materno de oxigénio. Do ponto de vista cardiovascular, existe aumento do volume sanguíneo e da massa eritrocitária, bem como do débito cardíaco; ao mesmo tempo, verifica-se redução dos valores de pressão arterial e da resistência vascular periférica5. Deste modo, as mudanças que ocorrem durante a gravidez, nomeadamente a nível dos sistemas imunitário, respiratório e cardiovascular, contribuem para os resultados adversos materno-fetais desta doença, implicando maior morbimortalidade6), (7.
Estudos recentes recomendam o uso atempado de inibidores da neuraminidase no tratamento da gripe em mulheres grávidas, mais especificamente, o oseltamivir. Este tem sido alvo de vários estudos para avaliar a sua segurança neste grupo mais vulnerável.
A neuraminidase é uma glicoproteína existente na superfície dos vírus Influenza A e B, que lhes confere virulência, sendo responsável pela penetração do vírus nas células por pinocitose e libertação do vírus da célula hospedeira através da membrana celular. O Oseltamivir é um análogo ciclo-hexénico do ácido siálico, sendo comercializado, em Portugal, na forma galénica de cápsula de 30, 45 ou 75 mg, para administração per os, sob nome comercial de Tamiflu® e Ebilfumin®. O fosfato de oseltamivir é um pró-fármaco que, após metabolização pelo fígado e trato gastrointestinal, se transforma em carboxilato de oseltamivir (metabolito ativo), que apresenta atividade contra o vírus influenza dos tipos A e B1. Pensa-se que o oseltamivir, ao inibir a neuraminidase do vírus, altera a sua possibilidade de agregação e de libertação de partículas. O carboxilato de oseltamivir é excretado por via renal. Os principais efeitos secundários são as náuseas, vómitos e cefaleia8.
Estudos de segurança revelam que a exposição pré-natal ao oseltamivir não está associada a um aumento de hemorragia e púrpura trombocitopenica trombócita materna, nem a outcomes fetais adversos como morte fetal (aborto espontâneo ou induzido antes das 22 semanas de gestação), parto pré-termo (antes da 37ª semana de gestação), índice de APGAR baixo (menor que 7), baixo peso à nascença (peso inferior a 2500 gramas) ou malformações major e minor (designadamente cardíacas) e patologia neonatal (dificuldade respiratória, pneumotórax, icterícia, patologias metabólicas, sépsis) (9),(10),(11),(12),(13.
Desta forma, o objetivo deste trabalho é rever a evidência acerca da efetividade do oseltamivir no tratamento da gripe nas grávidas.
Métodos
Para a revisão, foi realizada, a 11/09/2020, uma pesquisa da literatura nas bases de dados MEDLINE, DARE, Cochrane, Web of Science, TRIP e NICE, utilizando a seguinte query: (Treat* OR Therapy) AND (oseltamivir OR neuraminidase inhibitors) AND pregnan*. A pesquisa foi restrita às espécie humana e línguas portuguesa, inglesa e espanhola, com data de publicação nos últimos 10 anos. Foram aceites estudos originais de meta-análise, revisões sistemáticas, ensaios clínicos aleatorizados e controlados e estudos observacionais. Os estudos potencialmente elegíveis para revisão adicional foram selecionados através da análise dos respetivos títulos e resumos. Se, através desta análise, um estudo foi considerado relevante, prosseguiu-se à sua leitura integral. As referências dos estudos incluídos foram usadas para encontrar estudos em falta na pesquisa inicial. Foram excluídos os estudos que não reportavam os outcomes propostos.
Para além disso, foi realizada uma pesquisa abrangente de guidelines ou normas de orientação clínica que fornecessem informação relevante para a presente revisão.
Critérios de Elegibilidade
Para serem incluídos na revisão, os estudos teriam de abordar a efetividade do uso do oseltamivir em grávidas com suspeita ou confirmação de infeção pelo vírus Influenza, através da comparação com grávidas com suspeita ou confirmação de infeção pelo vírus Influenza não tratadas ou tratadas com outros fármacos que não sejam oseltamivir ou outros inibidores da neuraminidase. Assim, os critérios de inclusão respeitaram a seguinte definição PICO:
População: Grávidas com diagnóstico suspeito ou confirmado de gripe.
Intervenção: Grávidas com gripe expostas a oseltamivir.
Comparação: Grávidas com gripe não expostas a oseltamivir.
Resultados: Efetividade do tratamento das grávidas com gripe com oseltamivir.
Todos os estudos que não cumprissem o objetivo da revisão ou que não apresentassem o grupo controlo definido foram excluídos. As guidelines, por sua vez, foram incluídas na sua totalidade, de forma a expor e comparar as diferentes recomendações de atuação na prática clínica.
A escala Strenght Of Recommendation Taxonomy - SORT14 foi utilizada para avaliar o nível de evidência (NE) dos artigos incluídos e a força de recomendação (FR).
Resultados
Pesquisa Bibliográfica
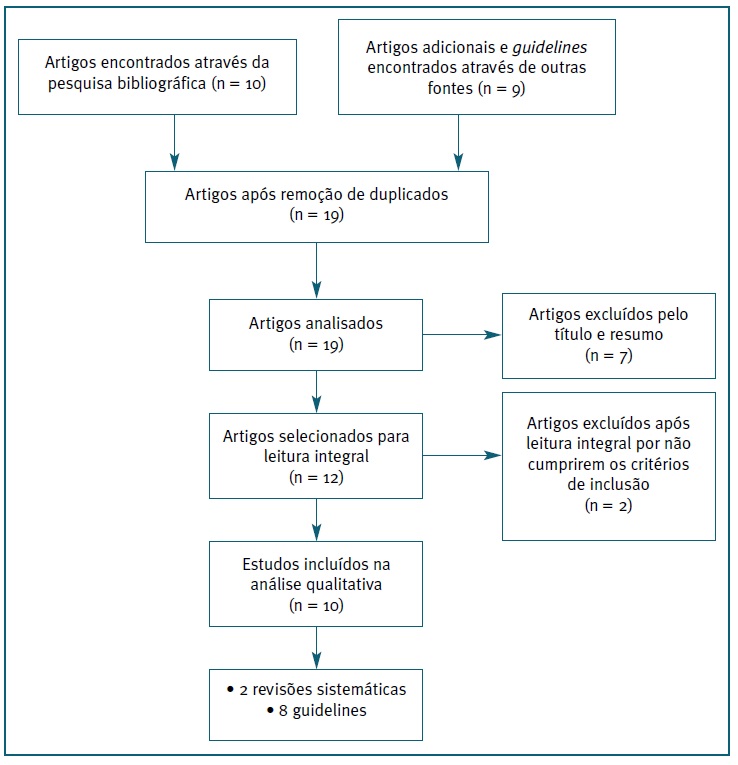
A pesquisa inicial incluiu 10 artigos. Subsequentemente, 7 estudos foram excluídos após leitura do título e resumo. Após leitura integral dos 3 artigos restantes, 2 foram excluídos por não cumprirem os critérios de inclusão. Após leitura das referências dos estudos encontrados, 1 estudo foi adicionado para avaliação uma vez que respeita os critérios de inclusão da presente revisão. A estes estudos foram adicionadas 8 guidelines, provenientes de US Centers for Disease Prevention and Control (CDC), Royal College of Obstetricians and Gynecologists (RCOG), National Health System (NHS), Public Health England (PHE), The American College of Obstetricians and Gynecologists (ACOG), Infectious Diseases Society of America (IDSA), Health Protection Surveillance Centre (HPSC) e Direção-Geral da Saúde (DGS). Assim, avaliou-se um total de 10 estudos, duas revisões sistemáticas15), (16 e oito guidelines orientadoras da prática clínica. O processo da pesquisa bibliográfica encontra-se sumariado na Figura 1.
Características dos Estudos Incluídos
Revisões Sistemáticas (Quadro I)
Em 2017, Boikos, C et al. (15 publicaram uma revisão sistemática (RS) com o intuito de resumir a evidência científica relativamente à efetividade e segurança dos antivirais inibidores da neuraminidase (IN), usados durante situações de pandemia ou durante o novo vírus influenza, entre os anos 2009 e 2015. Foram incluídos os estudos observacionais (EO) e os ensaios clínicos aleatorizados controlados (ECACs) que abordaram os efeitos dos IN no tratamento de indivíduos com diagnóstico confirmado de gripe, na profilaxia dos contactos próximos e no controlo de surtos. Os autores definiram uma população alvo abrangente, nomeadamente, população geral, crianças com idade inferior a 18 anos, adultos com idades compreendidas entre os 18-65 anos, idosos com idade superior ou igual a 65 anos e indivíduos imunocomprometidos ou portadores de doenças crónicas. Avaliaram, também, um subgrupo de mulheres grávidas e puérperas.
QUADRO I Resultados das revisões sistemáticas incluídas na presente revisão
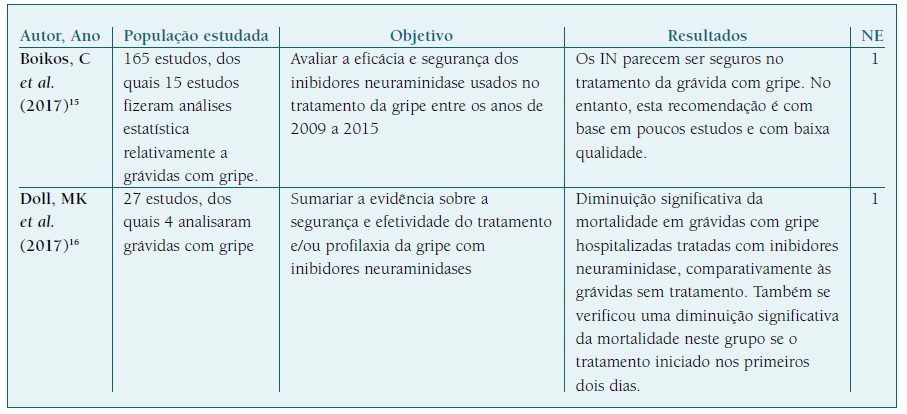
Legenda. NE - Nível de evidência; IN - Inibidores da neuraminidase
Nesta RS, os autores incluíram 165 estudos, dos quais, 155 corresponderam a EO e 10 a ECACs. De todos os estudos avaliados, 15 apresentaram resultados de interesse no subgrupo de grávidas e puérperas. Apesar de dois estudos (Yates, L et al. (8 e Varner, MW et al. (17) terem demonstrado um benefício significativo na administração dos IN nas primeiras 48 horas do início dos sintomas, um estudo (Yu, H et al. (18) não demonstrou diferenças no outcome de severidade da gripe com a administração precoce destes antivirais, tanto na população geral como nas grávidas. Relativamente à segurança, quatro EO avaliaram este parâmetro nas grávidas com gripe. Desta forma, os autores concluíram que apesar de parecer ser segura a utilização dos IN nas grávidas, mais estudos com maior qualidade na metodologia e uma amostra maior são necessários para sustentar a sua segurança e efetividade.
Em 2017, Doll, MK et al. (16. publicaram uma RS de várias revisões sistemáticas e meta-análises (MA), ECACs e EO com o objetivo de quantificar a evidência relativamente à efetividade e segurança dos IN no tratamento e profilaxia da gripe (com diagnóstico confirmado ou suspeito). Tal como a RS anterior, os autores não restringiram a população de estudo e dividiram-na em seis subgrupos: população geral, crianças com idade inferior a 18 anos, adultos com idades compreendidas entre os 18-65 anos, idosos com idade superior ou igual a 65 anos, indivíduos imunocomprometidos ou portadores de doenças crónicas e grávidas e puérperas a amamentar.
No total, foram analisados 27 artigos, dos quais, duas RS, nove MA e 16 RS com MA. A média do número de participantes por cada RS com MA foi 11539 (3908 de mediana). Destes artigos, quatro analisaram especificamente a segurança e efetividade dos IN no tratamento (mas não na profilaxia) da gripe na grávida (Muthuri, SG et al. (19, Hsu, J et al. (20, Meijer, WJ et al. (21 Muthuri, SG et al. (22). Os autores concluíram que o uso dos IN em mulheres grávidas com gripe, comparativamente ao não uso de IN, resultou na diminuição, estatisticamente significativa, da taxa de mortalidade nas grávidas que foram hospitalizadas. Adicionalmente, verificaram que o uso dos IN nas primeiras 48 horas, em comparação com o início do tratamento após este período de tempo, também resultou numa mortalidade inferior nas grávidas hospitalizadas.
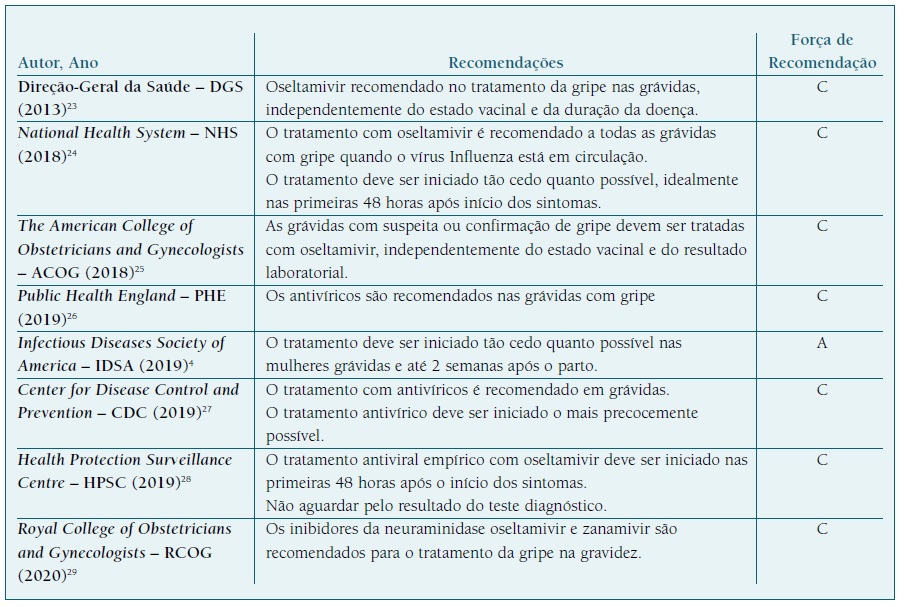
Guidelines (Quadro II)
A DGS23, na orientação relativa à terapêutica e quimioprofilaxia da gripe sazonal, época gripal 2013/2014, recomenda a terapêutica com oseltamivir nas grávidas, nas primeiras 48 horas após o início dos sintomas de infeção por Influenza. Esta recomendação insere-se numa estratégia de prevenção e minimização da evolução para doença grave e da transmissão da infeção a pessoas de risco.
O NHS24 recomenda o tratamento com oseltamivir a todas as grávidas com gripe e refere que este deverá ser iniciado nas primeiras 48 horas após o início dos sintomas. Considera existir benefício em iniciar tratamento até ao quinto dia após início dos sintomas.
O ACOG25 afirma que os profissionais de saúde devem reconhecer prontamente os sintomas da gripe e instituir tratamento antivírico com oseltamivir às grávidas com infeção suspeita ou confirmada. O tratamento deverá ser presuntivo, independentemente do estado vacinal da grávida e do resultado do teste laboratorial, e deve ser iniciado nas primeiras 48 horas após o início dos sintomas. Contudo, este não deve ser evitado se a janela ideal for ultrapassada. Recomendam-no até às 2 semanas após o parto.
De acordo com as recomendações da PHE26, o tratamento das grávidas com gripe com oseltamivir deverá ser instituído nas primeiras 48 horas, com benefício até ao quinto dia após o início dos sintomas.
A IDSA4 inclui as grávidas no grupo de muito alto risco para o desenvolvimento de complicações materno-fetais provocadas pela gripe. Recomenda que o tratamento antiviral com oseltamivir seja iniciado tão cedo quanto possível após o início dos sintomas em grávidas com suspeita ou diagnóstico confirmado da infeção pelo vírus Influenza, independentemente da história vacinal de gripe. A IDSA refere o benefício deste tratamento até às duas semanas após o parto.
O CDC27, nas suas orientações sobre a época de gripe 2019/2020, recomenda que seja instituído tratamento antiviral com oseltamivir às grávidas com gripe, idealmente nas primeiras 48 horas após o início dos sintomas. Sublinham que este é um grupo de muito alto risco para o desenvolvimento de complicações materno-fetais graves provocadas pelo Influenza. Esta entidade alerta, ainda, para o facto do tratamento antivírico da gripe estar sub-prescrito neste grupo de doentes.
As orientações do HPSC28 aconselham que o tratamento antiviral empírico com oseltamivir deve ser iniciado nas primeiras 48 horas após o início dos sintomas, sem aguardar pelo resultado do teste diagnóstico.
O RCOG29 recomenda o uso do inibidor da neuraminidase, oseltamivir, no tratamento da gripe na grávida, o qual deverá ser instituído o mais precocemente possível.
Discussão e conclusão
Os estudos relativos à pandemia do H1N1, em 2009, revelaram o impacto clínico da infeção pelo Influenza A pdm09 nas grávidas30),(31),(32),(33. Sabe-se ainda que o risco de morbimortalidade materno-fetal é superior durante o segundo e terceiro trimestres30.
A RS de Doll, MK et al. (16 demonstrou um claro benefício na administração dos IN nas primeiras 48 horas em mulheres grávidas hospitalizadas com infeção pelo vírus influenza. Apesar disto, esta revisão não estabeleceu uma relação entre o uso destes antivíricos na grávida com gripe e a necessidade de hospitalização, admissão nos cuidados intensivos, risco de desenvolver pneumonia ou tempo de melhoria sintomática.
Por outro lado, a RS de Boikos, C et al. (15 abordou a segurança da utilização deste grupo farmacológico na gravidez mas não demostrou resultados conclusivos acerca da efetividade dos IN nas grávidas com gripe, concluindo apenas que parece haver evidência na redução da mortalidade e do risco de pneumonia na população geral.
Ambas as revisões englobaram todos os IN, sendo os resultados transponíveis para a classe em geral. Doll, MK et al. (16 analisaram apenas o oseltamivir oral e o zanamivir inalado, uma vez que não foram encontradas RS/ MA que medissem os efeitos do peramivir ou do laninamivir. No entanto, o oseltamivir foi o fármaco mais utilizado (mais do que 90%) nos ECACs que foram incluídos para análise, pelo que as autoras transpuseram os resultados para o oseltamivir, sem prejuízo do significado estatístico.
Não obstante, estes achados corroboram as recomendações de diversas entidades mencionadas anteriormente, nomeadamente de iniciar o tratamento antivírico o mais precocemente possível após o início dos sintomas, idealmente nas primeiras 48 horas. O RCOG afirma que os inibidores da neuraminidase reduzem a duração dos sintomas e as taxas de morbimortalidade materna e fetal29. O ACOG, PHE e NHS consideram que poderá existir benefício na instituição de tratamento até cinco dias após o início dos sintomas24), (25), (26. O ACOG, IDSA, PHE e HPSC sugerem não aguardar pelo resultado do teste laboratorial para iniciar o antivírico, devendo este ser instituído de forma empírica4), (25), (26), (28. As entidades ACOG, HPSC, NHS, DGS sugerem o esquema posológico de oseltamivir 75 mg, duas vezes por dia, per os, durante 5 dias23)-(25), (28.
De referir que a norma da DGS23 reporta aos anos 2013/2014, pelo que o presente artigo sustenta a sua atualização e consequente generalização e aplicação na prática clínica contemporânea.
Como limitações aos estudos incluídos dever-se-ão referir a existência de poucos estudos sobre o assunto, a inexistência de ensaios clínicos aleatorizados controlados, bem como de mais estudos bem desenhados metodologicamente, muito pelas questões éticas inerentes à realização de estudos na população grávida. Por outro lado, embora as guidelines o recomendem, são raros os estudos bem desenhados que abordam o tratamento com inibidores da neuraminidase na grávida em contexto ambulatório o que condiciona a abrangência dos resultados e aumento o risco de viés de seleção da população grávida que foi avaliada. Outra limitação da presente revisão a ter em conta é o facto de a maioria das guidelines analisadas consistirem na opinião de peritos, limitando assim as conclusões delas retiradas e a força de recomendação.
Ainda assim, os autores consideram que esta revisão apresenta uma evidência consistente e de boa qualidade pela restrição dos critérios de inclusão, com resultados orientados para o doente. De facto, a evidência científica atual parece ser consensual em indicar que, nas grávidas com infeção, suspeita ou confirmada, pelo vírus Influenza, o tratamento com oseltamivir (75 mg, duas vezes por dia, per os, durante 5 dias), idealmente iniciado nas primeiras 48 horas após o início dos sintomas, é recomendado, eficaz e seguro do ponto de vista materno-fetal.
Para além disso, tendo em consideração que a infeção pelo atual COVID-19 pode manifestar-se com sintomas muito semelhantes a uma infeção pelo vírus Influenza, os estudos defendem a segurança do uso do oseltamivir em ambas as entidades34), (35, acrescentando que o tratamento de oseltamivir deverá ser iniciado empiricamente e descontinuado se a análise por PCR para Influenza for negativa35.
Desta forma, as autoras atribuem à presente revisão baseada na evidência um Nível de Recomendação B. Contudo, são necessários mais estudos de boa qualidade para fundamentar esta evidência.
Agradecimentos
As autoras agradecem à Dr.ª Mafalda Oliveira, médica de Medicina Geral e Familiar, pela orientação fornecida ao longo da realização do presente trabalho, assim como pela disponibilidade, entusiasmo, motivação e inspiração constantes, que nos têm guiado durante este percurso.