Introdução
A contraceção oral é, sem dúvida, um dos métodos contracetivos mais utilizados, em particular pelas mulheres portuguesas1. A introdução do etinilestradiol (EE) na contraceção hormonal combinada (CHC), na década de 60, constituiu um avanço considerável quanto à segurança quando comparado com o estrogénio então usado, o mestranol2. A segurança tem sido uma preocupação constante, particularmente no que concerne ao risco tromboembólico venoso e arterial (TEV/TEA).
A evolução da CHC tem como objetivo encontrar soluções contracetivas de eficácia elevada, que aumentem a segurança e otimizem os benefícios não-contracetivos. Neste sentido, procurou-se minimizar o impacto da CHC nos fenómenos de TEV/TEA com a redução progressiva da dose de EE, otimizando a segurança e o controlo do ciclo. O uso de progestativos mais seletivos foi outra linha de abordagem, com o objetivo de garantir uma eficácia contracetiva elevada e aumentar os benefícios não-contracetivos. Todavia, a utilização dessas combinações contracetivas foi questionada quando se verificou que as mesmas doses de EE associadas a progestativos mais androgénicos (por exemplo, o levonorgestrel - LNG) eram as que otimizavam a segurança (menos eventos trombóticos), mas eram as que menos garantiam os benefícios não-contracetivos, nomeadamente na pele3,4.
O E4, um estrogénio descoberto por Diczfalusy e colaboradores em 19655, é sintetizado exclusivamente pelo fígado fetal durante a gravidez e é produzido industrialmente para uso clínico a partir de fontes vegetais6. Este estrogénio tem um mecanismo de ação singular, sendo simultaneamente agonista do recetor de estrogénio-alfa (REα) nuclear e antagonista do REα membranar7, o que o caracteriza como um estrogénio nativo com atividade tecidual seletiva (NEST na sigla inglesa) (8. Esta atividade seletiva resulta em ações estrogénicas na inibição da ovulação, proliferação do endométrio e do epitélio vaginal, uma ação muito menos marcada no epitélio mamário que o estradiol e significativamente mais ligeira que o EE a nível hepático e vascular9-11.
A combinação E4 com a DRSP tem sido estudada como contracetivo oral combinado (COC), apresentando um perfil eficaz de ação contracetiva e maior segurança12. O primeiro estudo em humanos com E4, por via oral, mostrou uma supressão significativa da secreção da hormona folículo-estimulante (FSH) e da hormona luteinizante (LH), critérios basilares para a função contracetiva13. Os ensaios clínicos de fase II confirmaram que a associação E4/DRSP provoca uma supressão efetiva da ovulação12,14, um padrão hemorrágico favorável15 e um impacto limitado nos parâmetros endócrinos, metabólicos e hemostáticos16-21. Adicionalmente, esta associação mantém a proliferação endometrial em níveis adequados, havendo um equilíbrio entre a ação proliferativa induzida pelo E4 e a atividade secretora induzida pela DRSP, que se traduz clinicamente na descamação do endométrio e consequente perda hemática/incidência de spotting.
O COC com E4/DRSP é atualmente comercializado com a designação Nextselis® nos Estados Unidos da América (EUA) e Drovelis® ou Ludisika® na Europa22, sob a forma de comprimido de toma única diária, no regime de 24/4 (24 comprimidos com 15 mg E4 e 3 mg de DRSP, e 4 placebo), com indicação aprovada para contraceção oral.
Este artigo apresenta os resultados de uma revisão da literatura sobre as propriedades terapêuticas, eficácia, tolerância e segurança do COC com E4/DRSP aprovado na Europa e nos EUA.
MÉTODOS
Foi realizada uma revisão da literatura com base numa pesquisa bibliográfica em diferentes bases de dados como a EMBASE, MEDLINE e PubMed de 1946 a janeiro de 2023. A seleção foi efetuada com base na informação disponível no abstract. Os dados relevantes sobre ensaios clínicos também foram pesquisados. As palavras-chave utilizadas foram estetrol e drospirenona. Apenas foram consideradas publicações em língua inglesa ou portuguesa. Foram revistos 31 artigos, nos quais se fundamenta a construção deste manuscrito.
Eficácia contracetiva e controlo de ciclo
Desde o primeiro estudo de exposição do E4 em ratos do sexo feminino verificou-se que esta molécula apresenta uma ação contracetiva significativa23. Seguiram-se vários estudos, entre os quais dois ensaios clínicos de fase II, que levaram à identificação da combinação de 15 mg E4 com 3 mg de DRSP como a mais favorável no controlo de ciclo e perfil de hemorrágico15. A eficácia do COC 15 mg E4/DRSP 3 mg foi avaliada em dois ensaios clínicos internacionais de fase III com braço único [E4 FREEDOM] conduzidos nos EUA/Canadá24 e Europa/Rússia25. Em ambos os estudos, esta combinação apresentou-se como um COC eficaz, com um índice de Pearl (IP), de 0.44 no estudo europeu, 2.65 no estudo americano e 1,52 (95% IC 1,04-2,16) após análise conjunta das 3.027 mulheres com idades entre 16 e 35 anos, incluídas nos 2 estudos. O IP é habitualmente mais alto nos EUA que nos países europeus, por razões culturais e locais26.
A análise conjunta dos resultados do ensaio clínico de fase III validam E4/DRSP como um COC eficaz para a globalidade das mulheres, mas também nos subgrupos estratificados por idade, história prévia de utilização de contraceção hormonal e IMC26.
Nos dois ensaios clínicos avaliados, os períodos de hemorragia de privação e perda hemorrágica não programada (tipo spotting) mantiveram-se estáveis durante a utilização de E4/DRSP na maioria das mulheres22,24. Foram observados padrões de hemorragia cíclica durante a fase placebo dos ciclos de tratamento de 24/4 dias, com duração média de 4 a 5 dias. A análise agregada dos dados dos dois ensaios demonstrou que a maioria das participantes (87,2 - 90,4%) experienciaram hemorragias regulares programadas. A frequência de hemorragia não programada ou eventos de spotting foi de 27,1% no ciclo 1, com tendência a ser menos frequente a partir do ciclo 5, mas a incidência foi sempre inferior a 17,5% (Figura 1) (27. Contudo, no estudo EUA/Canadá, a proporção de mulheres que relataram que ausência de sangramento programado foi maior no ciclo 3 (18,0%), baixando para 13,3% no ciclo 12 (19). No estudo Europa/Rússia, o relato de ausência de hemorragia de privação foi sempre igual ou inferior a 10% durante todos os ciclos de tratamento22. Neste mesmo estudo, o perfil de hemorragia das participantes não foi aparentemente afetado pela idade, nem pelo uso prévio de contracetivo hormonal25, porém, a falta de compliance no tratamento e o IMC superior afetaram o padrão menstrual durante a utilização de E4/DRSP27.
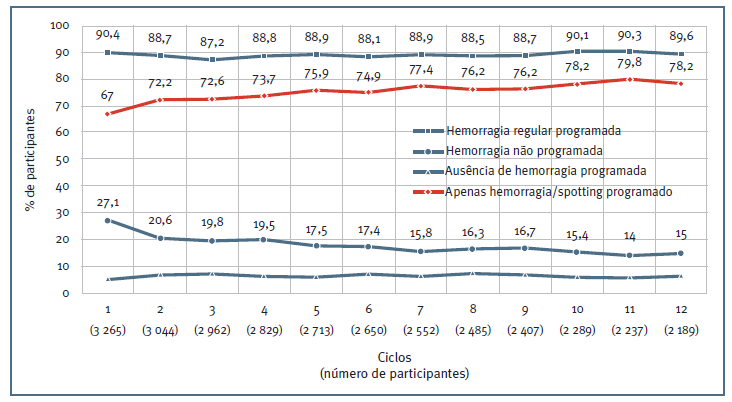
Figura 1 Percentagem de participantes que relataram hemorragia regular programada, hemorragia não programada, ausência de hemorragia programada e apenas hemorragia ou spotting programado por ciclo durante o uso de contraceção oral com E4/DRSP. Note-se que o resultado não perfaz 100% em cada ciclo, porque as participantes podem relatar perda hemorrágica programada e spotting não programado no mesmo ciclo e, portanto, serão contadas duas vezes27.
Face aos dados disponíveis é possível associar o uso do COC com 15 mg E4/DRSP 3 mg a uma menor taxa de hemorragia não-programada e ausência de hemorragia programada, em comparação com as opções atualmente disponíveis no mercado, nomeadamente com as pílulas progestativas no mesmo regime 24/428.
Perfil de tolerância e segurança
Ao longo dos estudos clínicos realizados, o tratamento com E4/DRSP foi, em geral, bem tolerado, com baixas taxas de efeitos indesejáveis reportados22. O relato de qualquer efeito indesejável foi registado por 50,5% das participantes no estudo realizado na Europa/Rússia e 53,8% no estudo realizado na América do Norte24-26, dos quais apenas 29% foram considerados associados ao tratamento.
A análise conjunta dos ensaios de fase III (Europa/Rússia e América do Norte), incorporando 3.417 mulheres, reiterou que os eventos indesejáveis mais frequentes são a hemorragia uterina anormal (4,7%), o acne (3,3%) e a cefaleia (3,2%)27. Durante esses estudos, seis mulheres (0,05%) descontinuaram o uso de E4/DRSP devido a enxaquecas graves enquanto uma participante descontinuou devido a hipercaliemia. Este evento poderá ter ocorrido devido às propriedades anti-mineralocorticóides da DRSP, todavia a maioria dos casos de hipercaliemia foi de gravidade leve e transitória. Adicionalmente, nove mulheres (0,3%) do estudo realizado na América do Norte descontinuaram o uso de E4/DRSP devido a depressão. A incidência de depressão (relacionada ao tratamento ou qualquer evento) no estudo Europa/Rússia foi inferior a 2%22. De salientar que o perfil de segurança observado nestes estudos foi consistente com o demonstrado com o uso de outros COCs22.
Apenas foram relatados 3 casos (0,1%) de eventos indesejáveis graves relacionados com o tratamento, nomeadamente 1 caso de agravamento da depressão, 1 caso de TEV e 1 caso de gravidez ectópica, este último foi igualmente uma falha do método. O tratamento foi interrompido nos últimos dois casos27. O evento de TEV ocorreu durante o quarto ciclo de uso de E4/DRSP, numa mulher com 32 anos e histórico de uso prévio de contraceção hormonal. Este evento foi resolvido sem sequelas após tratamento anticoagulante22.
Existe uma relação entre o grau de estimulação hepática pelo componente estrogénico e o risco de TEV/TEA29. É, por isso, importante que se procurem novas soluções contracetivas que não tenham impacto hepático significativo de modo a controlar o risco TE, o que é essencial atendendo que um evento tromboembólico associado à contraceção é sempre motivo de alarme30. Devido à singularidade do seu metabolismo, E4 apresenta um impacto reduzido na função hepática, na medida em que após a primeira passagem hepática não induz a produção de metabolitos ativos que se mantenham em circulação, o que redunda num aumento mais ligeiro das proteínas hepáticas e menor inibição das enzimas do citocromo P450, em contraste com moléculas como o EE e mesmo o estradiol (E2) (7,31. Em combinação com a DRSP, o uso de E4 demonstrou nos ensaios clínicos um efeito reduzido nas lipoproteínas e nos níveis da globulina transportadora de hormonas sexuais (na sigla inglesa, SHBG) e, não induziu alterações nos fatores associados à hormona de crescimento20,21.
No que respeita à interferência nos fatores de coagulação o E4, em contraste com o EE, tem um menor impacto na produção de trombina32. A combinação E4/DRSP mostrou, em estudos de fase II , um perfil de risco favorável para TEV, com baixo impacto na cascata de coagulação ao nível de distintos marcadores de hemóstase, dos quais se destacam os fragmentos 1 e 2 da protrombina, trombina, proteína S e rácio normalizado de sensibilidade à proteína C ativada - nAPCsr) (18. Douxfils e col., num estudo publicado em 2020 comparou o impacto nos parâmetros hemostáticos de três combinações contracetivas, duas com o mesmo progestativo na mesma dose - 15 mg E4/DRSP 3 mg vs 20 mcg EE/DRSP 3 mg - e uma terceira com 30 mcg EE/150 mcg de LNG, tendo concluído que as alterações nos fatores de coagulação após o tratamento com 6 ciclos de E4/DRSP foram menores ou semelhantes às observadas com a combinação EE/LNG. Foram verificadas alterações mais pronunciadas com a combinação EE/DRSP o que suporta a hipótese de que o efeito dos COCs nos fatores de coagulação é mediado principalmente pelo componente estrogénico (Figura 2) (33. Além disso, E4/DRSP tem também menor impacto sobre a SHBG, um biomarcador que reflete a estrogenicidade total de um estroprogestativo, também apontado como indicador do risco de TEV, embora seja insensível para coagulopatias hereditárias33.
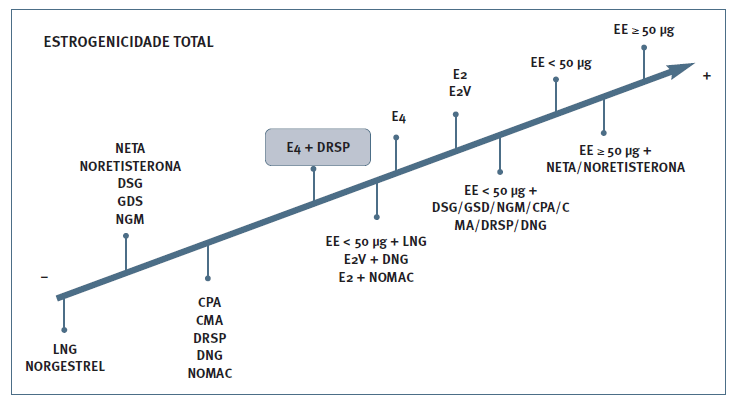
Figura 2 Escala de estrogenicidade dos contracetivos hormonais. CMA, acetato de clormadinona; CPA, acetato de ciproterona; DNG, dienogeste; DRSP, drospirenona; DSG, desogestrel; EE, etinilestradiol; E2, estradiol; E2V, valerato de estradiol; E4, estetrol; GSD, gestodeno; LNG, levonorgestrel; NETA, acetato de noretisterona; NGM, norgestimato; NOMAC, acetato de nomegestrol. Figura adaptada de Morimont et al. (2021) (2.
A meta-análise realizada por De Bastos e col. em 2013 com projeção do risco relativo de TEV para diversas combinações contracetivas fundamentada no rácio normalizado de sensibilidade à proteína C ativada (nAPCsr), serviu de base à projeção de risco da combinação E4/DRSP alicerçada nos mesmos critérios. Podemos verificar que o risco de 15 mg E4/DRSP 3 mg é significativamente inferior à associação com EE/DRSP e equivalente ou inferior à combinação EE/LNG. Esta combinação é a pilula de referência quanto ao risco de TEV, revelando assim um risco relativo inferior de TEV (Figura 3) (22,34. O E4 posiciona-se, assim, como alternativa de estrogénio mais segura que o EE29. Contudo, são necessários estudos de fase IV para validar clinicamente o menor potencial trombótico associado a E4/DRSP.
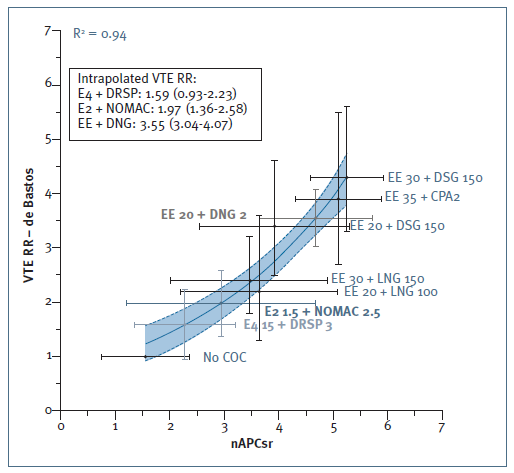
Figura 3 Relação entre rácio normalizado de sensibilidade à proteína C ativada (nAPCsr) e o risco relativo de TEV (VTE RR) para as diferentes combinações de contracetivos orais combinados. Adaptado de Gemzell et al. (22, inicialmente desenvolvido por De Bastos et al. (34.
O impacto no metabolismo ósseo é sempre uma preocupação acrescida quando consideramos o uso de estrogénios, particularmente em jovens, atendendo ao possível impacto na formação óssea. Os estudos com E4/DRSP revelaram que esta combinação promove o equilíbrio entre a reabsorção óssea e a formação óssea, mantendo a regulação da densidade mineral óssea20. A interferência na mama é sempre também um aspeto a ter em consideração. Em concentrações terapêuticas, E4/DRSP tem um efeito neutro no risco de cancro da mama35. Estudos realizados in vitro e in vivo mostraram uma potência 100 vezes inferiores do E4 em comparação ao E2 na estimulação da proliferação do tecido mamário36. Na presença de E2, o E4 atuou como antagonista parcial, inibindo a proliferação induzida por este estrogénio nas células epiteliais do tecido mamário humano e o crescimento da glândula mamária em ratinhos36-38. O impacto da combinação de E4 com um progestativo demonstrou que E4 combinado ou não com a progesterona ou DRSP não promove o desenvolvimento de células cancerígenas na mama, nem a respetiva disseminação metastática35. Este estudo corrobora os dados previamente publicados que demonstraram que a DRSP, em contraste com os progestativos androgénicos, não estimula a proliferação de células do tecido mamário em modelos animais de oncogénese de cancro da mama com recurso a xenoenxertos39.
Na análise do conjunto de doentes incluídas nos estudos de fase III, verificou-se que a dor e sensibilidade mamária esteve presente em 4% das utilizadoras de E4/DRSP e em apenas 1,6% de todos os ciclos. Esses sintomas ocorreram principalmente nos ciclos 1-3, diminuíram posteriormente até aos ciclos 10-13 e não foram causa de descontinuação do tratamento40.
Benefícios não contracetivos
A eficácia contracetiva é um pressuposto básico, quando a mulher é confrontada com várias opções contracetivas. A escolha contracetiva, por esta ou aquela opção, após o aconselhamento, radica nas preocupações sobre segurança (tromboembolismo e cancro da mama) e nos benefícios não contracetivos (controle do ciclo, da dismenorreia e dos sinais de androgenização) e não impacto no peso41. É imperativo que o grau de satisfação e o perfil de aceitabilidade das formulações contracetivas sejam estudadas de forma a melhorar, não só a adesão, como também a satisfação das utilizadoras. No caso específico da CHC, este tópico ganha maior relevância atendendo que a adesão é essencial para garantir a efetividade e menor risco de gravidez não planeada.
O estudo FIESTA comparou diferentes grupos de utilizadoras com doses de 15 mg ou 20 mg de E4 combinado com 3 mg DRSP ou 150 µg de LNG quanto à aceitabilidade e satisfação, tendo sido também avaliado o bem-estar geral das participantes42. O grau de satisfação das utilizadoras das combinações E4/DRSP foi significativamente superior às utilizadoras da combinação de E4/LNG. Contudo, não houve diferença estatisticamente significativa entre as pontuações obtidas para os grupos contendo E4/DRSP e valerato de estradiol e dienogest (E2V/DNG) (42.
Adicionalmente, os dois estudos multicêntricos de fase III, também calcularam o impacto do tratamento no bem-estar físico e psicológico com a combinação E4/DRSP24,25. Ambos os estudos mostraram que o bem-estar geral das participantes se manteve no nível 4, numa escala de 5 pontos (onde 1 é a pontuação mais baixa e 5 a mais alta), após 13 ciclos de utilização em comparação com o início do seu uso. Supletivamente, os sintomas menstruais também foram investigados por uma metodologia similar. Os resultados mostraram melhorias nos sintomas pré-menstruais, humor e função sexual. Globalmente houve elevada satisfação e mais de 97% das mulheres não reportou redução do desejo sexual42. Diferenças mínimas foram detetadas nas utilizadoras que mudaram de outro contracetivo oral combinado para a combinação E4/DRSP25,43. Estes resultados apontam para uma boa aceitabilidade e um impacto positivo na qualidade de vida das utilizadoras de E4/DRSP. Contudo, são necessários estudos adicionais na vida real, com amostras mais alargadas, para validar estes dados.
As questões relacionadas com a pele são também de grande importância. Após seis ciclos de tratamento, a combinação E4/DRSP induziu reduções similares às verificadas nos grupos de utilizadoras de combinações com EE, nos parâmetros endócrinos relacionados com os androgénios - níveis de androstenediona, sulfato de desidroepiandrosterona (DHEAS), di-hidrotestosterona (DHT), testosterona total e testosterona livre. (21 O perfil endócrino semelhante entre as combinações de EE ou E4 com drospirenona, sugere que os efeitos anti-androgénicos e de melhoria da acne induzida são semelhantes e decorrem sobretudo da ação do progestativo20.
O impacto no peso foi avaliado, comparando 15E4/DRSP com outras combinações estroprogestativas (E4/LNG e E2V/DNG) tendo-se constatado que a proporção de mulheres com perda de peso de 2 kg foi a mais alta para 15E4/DRSP e menor para 15E4/LNG, concluindo-se que o impacto sobre o peso é favorável42.
Contraceção verde
O impacto dos estrogénios nos ecossistemas é uma preocupação crescente, em particular nos sistemas aquáticos, como se constata do facto da União Europeia (UE) ter incorporado o estriol, estradiol e EE na lista de compostos sob vigilância44. As análises ecotoxicológicas mostram um aumento exponencial da concentração de estrogénios nos ecossistemas terrestres. Os estrogénios, designadamente o E1, o E2 e o EE, podem induzir, mesmo em baixas concentrações ambientais, efeitos nocivos sobre o sistema endócrino e imunitário de algumas espécies animais. Entre outras consequências descritas numa ampla gama de espécies (moluscos, crustáceos, peixes, aves e mamíferos), os estrogénios reduzem o crescimento dos peixes, afetam o desenvolvimento de características sexuais secundárias e a formação de ovotestis em machos. Os valores médios de estrogénios nas águas Portuguesas foram de ≈13 ng/L para E1, ≈12 ng/L para E2 e ≈15 ng/L para 17-α-etinilestradiol, (EE2), o que de acordo com os estudos in vivo são quantidades capazes de causar efeitos disruptivos em animais aquáticos e mesmo em humanos45.
O E4 diferencia-se do EE e do estradiol quanto ao impacto ambiental, pois o seu metabolismo não produz resíduos metabolicamente ativos. Os estudos de avaliação de risco ambiental com estetrol, incluindo um estudo alargado sobre a reprodução numa geração de peixe medaka japonês, indicaram que a exposição ambiental prevista ao estetrol não afetará o ecossistema aquático46. Um estudo recentemente publicado reforçou esta posição, demonstrando que o E4 tem menor impacto do que EE na capacidade reprodutiva de peixes zebra47.
Conclusão
A combinação E4/DRSP é uma solução contracetiva eficaz inibindo sustentadamente a ovulação e promovendo um perfil de hemorragia estável e regular.
Tem efeitos nos fatores de coagulação menos pronunciados que a combinação EE/DRSP, com realce para o facto de induzir alterações de menor relevância no rácio de sensibilidade à proteína C ativada, reforçando a evidência de que a molécula estrogénica é o agente fundamental no impacto pró-coagulante das combinações hormonais contracetivas. Estes elementos configuram um avanço no perfil de segurança da CHC, com inclusão do E4 em detrimento do EE, embora estes resultados claramente positivos não dispensem novas avaliações em estudos de base populacional, no decorrer do período de pós-comercialização.
Os benefícios não-contracetivos assegurados por E4/DRSP: controlo do ciclo, hemorragia previsível, ação na pele, no peso e na mama - respondem às exigências das mulheres que optam por CHC, com elevado grau de satisfação.
O menor impacto ambiental do E4, em relação às outras moléculas estrogénicas que incorporam a CHC, é mais um avanço que vai de encontro às preocupações crescentes com o meio ambiente.















