Os obstetras são os principais médicos das mulheres em idade fértil, pelo que estão numa posição privilegiada para fazer o rastreio do seu estado de imunização e para prescrever as vacinas adequadas. No entanto, fatores financeiros e falta de conhecimento sobre aconselhamento e segurança das vacinas parecem ser obstáculos à sua administração1.
A vacinação é um tema fundamental na consulta de obstetrícia desde a pré-conceção até ao puerpério, pelos benefícios significativos que algumas vacinas trazem quer para a mãe, quer para o feto. Globalmente, a transferência de anticorpos das grávidas para os fetos é fundamental para a saúde e sobrevivência de recém-nascidos e lactentes e sabemos que a imunização ativa das mulheres antes ou durante a gravidez pode aumentar a proteção do RN contra infeções específicas2,3.
Idealmente, as imunizações maternas deverão ser administradas antes da conceção, mas a administração durante a gravidez está indicada em algumas situações1. De facto, as mulheres devem ser vacinadas contra doenças preveníveis no seu ambiente antes da conceção, de acordo com o calendário de vacinação recomendado para adultos, reservando a vacinação durante a gravidez para todas as situações em que o risco de exposição é elevado, a infeção apresenta riscos para a mãe e/ou o feto e a vacina não é suscetível de causar danos1.
Apesar das adaptações imunológicas maternas à gravidez, as grávidas saudáveis têm uma resposta imunitária às vacinas semelhante às não grávidas. Após uma imunização materna, a Imunoglobulina G (IgG) fetal é menor que a materna na primeira metade da gravidez, aumenta para 50% dos níveis maternos pelas 28-32 semanas, iguala os níveis maternos às 36 semanas e excede esses mesmos níveis a termo. O pico da concentração da IgG fetal ocorre 4 semanas após a imunização1.
Pré-conceção
Mulheres que receberam uma ou duas doses de vacina contra a rubéola e têm níveis séricos de IgG que não são claramente positivos devem receber uma dose adicional da vacina (num máximo de três doses) e não precisam de ser novamente testadas para obter provas serológicas de imunidade à rubéola4-6.
De acordo com o Advisory Committee on Immunization Practices (ACIP), as doentes não grávidas sem provas de imunidade, e que não planeiam engravidar no mês seguinte, são candidatas à imunização com a vacina contra a varicela, que é administrada em duas doses com quatro a oito semanas de intervalo4,7.
Durante a gravidez
Os prestadores de cuidados de saúde devem administrar vacinas não vivas, adequadas a grávidas, com indicações médicas ou de exposição que as coloquem em risco de contrair infeções evitáveis por vacinação1,4,6-10.
Gripe
A gripe aumenta o risco de complicações maternas e perinatais graves, incluindo trabalho de parto pré-termo, morte fetal e necessidade de hospitalização materna e neonatal. Assim, e porque a vacina contra a gripe é segura durante a gravidez, a vacinação em qualquer trimestre, durante o período sazonal da gripe, é uma vertente essencial dos cuidados pré-natais11. Um estudo multinacional recente demonstrou que a vacina da gripe tem uma eficácia de 40% na prevenção da hospitalização por gripe nas grávidas e que reduz 34% das infeções nos recém-nascidos (RN) 12.
Assim, as grávidas devem ser vacinadas em qualquer idade gestacional, antes ou durante o período sazonal da gripe, podendo ser usadas vacinas inativadas ou recombinantes6,8,10.
Tosse convulsa (Tdpa)
Uma vez que as taxas mais elevadas de morbilidade grave e mortalidade causadas pela infeção a Bordetella pertussis ocorrem em lactentes com menos de três meses, a vacina Tdap deve ser administrada durante cada gravidez, independentemente do estado de imunização anterior. A vacinação contra a tosse convulsa em qualquer trimestre é segura, mas é preferível a sua administração no terceiro trimestre. Em Portugal a Direção-Geral da Saúde (DGS) recomenda a sua administração entre as 20 e as 36 semanas de gestação (32 semanas), depois da ecografia morfológica6.
As razões para vacinar uma mulher grávida antes das 27 semanas de gestação incluem uma história vacinal desconhecida ou história clínica incompleta, acompanhamento inconsistente de cuidados pré-natais ou como parte integrante da abordagem terapêutica de rotina de feridas quando o reforço do tétano está indicado11.
A produção de anticorpos maternos após a vacina Tdap requer duas semanas para atingir títulos suficientemente elevados para garantir a imunidade materna protetora e a transferência fetal passiva. Por conseguinte, o terceiro trimestre é a altura ideal para a vacinação do ponto de vista da imunidade fetal ou do recém-nascido. Este calendário permite tempo suficiente para que os anticorpos maternos atinjam níveis adequados e sejam transferidos, enquanto garante que os níveis de anticorpos permaneçam elevados no recém-nascido o mais próximo possível da série de vacinação inicial programada. Com a administração no terceiro trimestre, os anticorpos transmitidos ao feto apresentaram uma eficácia de 77,7% contra a doença nos recém-nascidos, e uma proteção de 90,5% contra os casos graves10,11,13.
COVID-19
Grávidas com COVID-19 têm complicações mais graves na gravidez, nomeadamente taxas mais elevadas de parto pré-termo e maior morbilidade e mortalidade. De facto, a gravidez ou uma gravidez recente são fatores de risco para doença SarsCov2 grave1,5.
Para além da eficácia na prevenção da COVID-19 materna durante a gravidez, a vacina tem sido associada a diminuição da taxa de nados-mortos. Adicionalmente, resultados recentes demonstraram que a vacinação materna reduziu as taxas de morbilidade e de hospitalização entre os lactentes com menos de 6 meses de idade, um grupo que tem um maior risco de doença grave e hospitalização, mas que não pode ser vacinado. Este benefício também se deve à transferência de imunidade protetora ao RN através do leite materno14. Mais recentemente, num estudo de coorte prospetivo que incluiu 2.261 e 1.940 bebés com idade entre 12 e 18 meses, respetivamente, a exposição in útero à vacinação contra COVID-19 não foi associada a scores anormais de desenvolvimento neurológico no Ages and Stages Questionnaire, aos 12 ou 18 meses de vida, sendo assim segura do ponto de vista do neurodesenvolvimento15.
Desta forma, a vacinação primária ou reforço da vacinação contra o SarsCov2 na gravidez são recomendados e doentes pertencentes a grupos de risco com indicação para reforços adicionais mantêm a indicação mesmo que estejam grávidas e independentemente da idade gestacional1,4,10,11.
Outras
As vacinas contra o papilomavírus humano e o herpes zoster não são vacinas vivas; no entanto, não são atualmente recomendadas durante a gravidez por falta de dados de segurança, e não devido a riscos documentados4,10,11.
As imunizações contra a hepatite A, a hepatite B e a doença meningocócica devem ser consideradas em mulheres grávidas com qualquer fator de risco para estas doenças, sendo seguras4,10,11.
O risco associado à vacinação deve ser ponderado em relação ao benefício para a mulher grávida que possa estar em risco elevado de exposição à febre amarela e suas complicações graves4,10,11.
As vacinas da varíola ou da raiva podem ser usadas na profilaxia pós-exposição4,10,11.
Contra-indicadas
As vacinas vivas atenuadas não são recomendadas para mulheres grávidas com base na teoria de que a exposição a um vírus vivo poderá condicionar doença materna e fetal. É o caso da VASPR, BCG, Varicela e a vacina do vírus influenza atenuado. No entanto, a vacinação inadvertida contra o sarampo, papeira, rubéola ou varicela durante a gravidez não deve ser considerada motivo para interrupção da gravidez4,10,11.
PÓs-Parto
As puérperas devem receber todas as vacinas recomendadas que não puderam ser ou não foram administradas durante a gravidez, incluindo as vacinas vivas atenuadas1,8,11,16.
As vacinas inativadas e as de vírus vivos são seguras durante o aleitamento materno. Foi demonstrado que a maioria dos vírus vivos das vacinas não é excretada no leite humano, ou quando é excretado no leite humano não infeta o lactente (exemplo mais comum - vírus da vacina contra a rubéola) 1,11,16.
Novidades
Várias vacinas foram recentemente desenvolvidas para alargar a lista de potenciais produtos de imunização materna, entre as quais as mais relevantes são as vacinas para o vírus sincicial respiratório e o Estreptococcus do Grupo B, uma vez que são as principais causas de morbilidade e mortalidade infantil em todo o mundo2.
Vírus sincicial respiratório (VSR)
Metade das hospitalizações por doenças do trato respiratório em crianças com menos de 1 ano de idade foram associadas ao VSR, e aproximadamente 60% destas doenças ocorreram em lactentes com menos de 3 meses de idade17. Assim, uma estratégia para a prevenção da doença neonatal semelhante à da tosse convulsa, baseada na vacinação materna, seria o ideal.
Clinicamente foi testada uma vacina proteica num ensaio fase 3, administrada entre as 24 e as 36 semanas, em 18 países, em que foram incluídas 3682 mulheres vacinadas (Vs. 3676 placebo). A eficácia ficou demonstrada na prevenção de doença do trato respiratório inferior associada ao VSR (81,8 % aos 90 dias de vida; 69,4% aos 180 dias de vida; se administrada entre as 32 e as 36 semanas, a eficácia foi de 91,1 % aos 90 dias de vida; 76,5% aos 180 dias de vida), sem problemas de segurança17.
Recentemente foi autorizada a comercialização desta vacina pela agência europeia do medicamento18, estando disponível em Portugal desde o final do ano de 2023.
A SPOMMF, a par doutras Sociedades médicas e científicas (ACOG, ACIP, CDC) recomenda a administração única desta vacina entre as 24 e as 36 semanas, devendo ser repetida em cada gravidez1,7,9.
Estreptococos tipo B (SGB)
O SGB é considerado um fator de risco de parto prematuro. Apesar da sua ampla implementação, a profilaxia intraparto do SGB é 80% eficaz na doença inicial do RN mas não tem sido eficaz na doença tardia ou na diminuição das sequelas pós-parto1,4,16. Pela baixa incidência da doença neonatal, a eficácia da vacina contra o SGB na gravidez tem sido difícil de demonstrar1,5,16. Num estudo recente, um ensaio da vacina (GBS6) fase 2, aleatório e controlado por placebo, realizado em três centros de investigação clínica, foram vacinadas 360 mulheres no 3.o trimestre. Ficou demonstrado que a vacinação gerou anticorpos contra o estreptococo do grupo B em mulheres grávidas, e que estes foram transferidos para os fetos em níveis associados a um risco reduzido de doença estreptocócica invasiva do grupo B (redução em 75 % do risco de doença ao nascer) 19.
Desafios
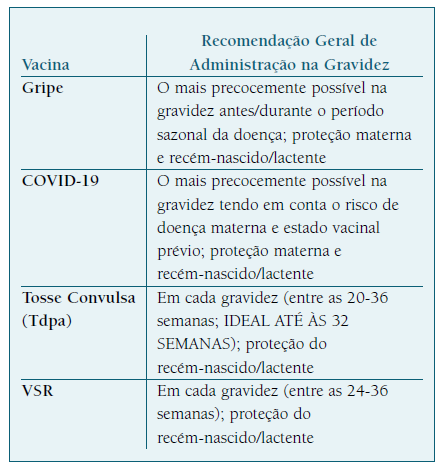
A hesitação vacinal, definida pela OMS como “um atraso na aceitação ou recusa de vacinação, apesar da disponibilidade de serviços de vacinação” é considerada uma das 10 principais ameaças à saúde mundial e pode ser particularmente perigosa durante a gravidez20. Muitos fatores contribuem para a relutância à vacinação entre as mulheres grávidas, incluindo o medo, desinformação e falta de preparação dos profissionais de saúde20.(Quadro I)
Resumo e recomendações práticas SPOMMF
A co-administração da vacina da Gripe e da vacina COVID-19 é segura e desejável se aumentar a adesão vacinal.
As vacinas Tdpa e VSR não devem ser administradas em conjunto, nem em co-administração com as vacinas COVID-19 ou gripe9.
O intervalo entre vacinas deverá ser de 2 semanas no mínimo9.
A administração da imunoglobulina anti-D na gravidez não deve ser realizada em co-administração com as vacinas, devendo o intervalo recomendado entre administrações ser de 2 semanas21.
Conclusão
A imunização materna é uma abordagem de longa data, bem estabelecida para proteger as grávidas de infeções evitáveis por vacinação. Após a imunização ativa da grávida, os anticorpos maternos são naturalmente transferidos para o feto, o que protege os lactentes de patógeneos infeciosos nos primeiros meses de vida, até que possam receber as suas próprias imunizações e/ou ultrapassar a idade das doenças mais graves. A estratégia para melhorar a adesão vacinal passa por perceber melhor as razões da hesitação vacinal, promovendo a literacia em saúde das grávidas, bem como a formação dos profissionais de saúde envolvidos nos cuidados de saúde materna.