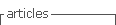Introdução
A infeção protésica é uma das complicações mais temidas da cirurgia aórtica (0,19% após cirurgia convencional e 0,16% após EVAR). Nestes casos, o tratamento de escolha nem sempre é consensual, dada a multiplicidade de opções e a elevada morbimortalidade que lhes está associada1. A estratégia mais comum é a revascularização extra-anatómica dos membros inferiores, seguida da remoção da prótese infetada e laqueação do coto aórtico. Para reduzir o elevado risco de rotura do coto aórtico estão descritas várias técnicas tais como dupla sutura, reforço com pledgets venosos, reforço com fáscia pré vertebral ou de epíplon, sendo que neste caso foi utilizado pacth de pericárdio bovino para reforço do coto. Os autores apresentam um caso de infeção de patch de pericárdio bovino usado como reforço da laqueação de coto aórtico.
Caso clínico
Doente de 53 anos, com antecedentes de hipertensão arterial, cardiopatia hipertensiva, hipercolesterolémia, ex fumador e acidente vascular cerebral com sequelas minor, foi submetido em 2015 a bypass aorto-bifemoral com prótese de Dacron® por doença aorto-ilíaca oclusiva. Em Setembro de 2019 inicia quadro clínico caracterizado pelo reaparecimento súbito de vários abcessos (músculos gémeos e glúteos) com identificação de microrganismos após colheita de liquido (Enterococcus faecalis + E. coli + Klebsiella pneumoniae). O doente não apresentava febre, melenas, anemia, hematémese, dor abdominal ou outras queixas. Em Outubro de 2019, apresenta em angio TC sinais de infeção protésica (presença de coleção líquida e ar periprotésico) e fistula aorto paraprotésica ABF - duodenal (D3). Doente refere realização de procedimento dentários sob AB profilática, assim como colonoscopia no último ano.
Iniciou antibioticoterapia dirigida com vancomicina durante 3 semanas, e foi submetido a bypass axilo-bifemoral e, após 5 dias, a remoção de prótese de bypass aorto-bifemoral, laqueação de coto aórtico (reforçado com patch de pericárdio bovino) e secção do jejuno proximal e remoção do arco duodenal distal interessando o orifício fistuloso com anastomose latero-lateral de D2 ao jejuno proximal. A microbiologia da prótese identificou Candida glabrata, Enterobacter cloacae e Klebsiella pneumoniae e o doente cumpriu ertapnem e anidulofungina dirigidos, com boa evolução clinica e laboratorial.
Após cerca de 3 meses, no angio TC de follow-up detetou-se coleção muito sugestiva de coleção infetada, apesar de o doente se manter assintomático, em apirexia e sem aumento dos parâmetros inflamatórios. O doente realizou AB empírica, e manteve-se em vigilância clínica, analítica e imagiológica.
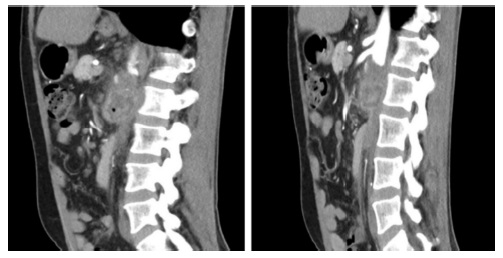
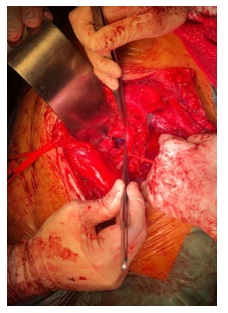
Foi solicitado novamente angio TC (Fig. 1) após 2 semanas de antibioterapia, tendo-se verificado um aumento da coleção acima descrita. Por este motivo, foi submetido a abordagem do coto aórtico retroperitoneal por tóraco-freno-laparotomia e abordagem da aorta infra-diafragmática através de rotação visceral esquerda. Imediatamente abaixo de coto aórtico constatou-se loca de tecido infectado e exsudado purulento, em que se encontrava o patch de pericárdio bovino não incorporado (Fig. 2 e 3).
Procedeu-se a desbridamento extenso de todo o tecido infectado e à excisão do patch, lavagem da loca e preenchimento da mesma com retalho vascularizado de epíplon. A microbiologia do patch identificou Candida glabrata e no líquido pericoto aórtico foi identificado, para além do acima referido, Enterococcus faecium. Foi realizada terapêutica com linezolide, metronidazol e anidulofungina, sendo que teve alta após boa evolução clínica e laboratorial, sob AB dirigida. O doente mantém-se clinicamente assintomático aos 5 meses de follow-up.
Discussão/conclusão
Os autores descreveram um caso de infecção de patch de pericárdio bovino utilizado para reforço do coto aórtico após explantação de prótese aorto-bifemoral infectada.
A infeção protésica é uma complicação rara mas uma das mais temidas da cirurgia aórtica convencional e endovascular, sem diferenças significativas na incidência após cirurgia eletiva e urgente1.
A apresentação clínica é variável sendo que 70% dos doentes apresentam dor, febre e leucocitose e 33% perda de peso, fadiga ou astenia2. Na presença de fístula aorto-entérica, a apresentação mais comum é sob a forma de hemorragia (71%), sépsis (39,7%) e choque hipovolémico (33.1%)1. No caso descrito, o doente apresentou como manifestações clínicas aumento dos parâmetros inflamatórios, febre e aparecimento súbito de vários abcessos (músculos gémeos e glúteos), sendo que o diagnóstico de infeção protésica com fístula aorto entérica foi realizado através de angio TC.
Em doentes com fístula aorto-entérica secundária, o tratamento não é consensual, dada a multiplicidade de opções e a elevada morbi-mortalidade que lhes está associada. A classificação proposta por Vollmar e Kogel divide as fístulas aorto-entéricas entre aquelas onde existe uma efetiva comunicação entre o tubo digestivo e o lúmen aórtico (tipo I) e aquelas em que existe perda da integridade da parede do tubo digestivo, sem compromisso da parede vascular ou da prótese (tipo II ou fístulas para-protésicas)3. A fístula no caso descrito pelos autores é tipo II ou para-protésica.
Na ausência de hemorragia digestiva, a contaminação protésica por contacto com o conteúdo entérico é o fator decisivo, sendo que, nestes casos, o tratamento definitivo passa pela remoção do material protésico. A cirurgia de revascularização dos membros inferiores constitui assim o principal ponto de divergência no tratamento destes doentes. A estratégia mais largamente utilizada é a revascularização extra-anatómica dos membros inferiores, seguida da remoção da prótese infetada e laqueação do coto aórtico, sendo que nestes casos uma abordagem faseada está associada a menor taxa de mortalidade e amputação4. No caso acima descrito, esta foi a estratégia escolhida pelos autores.
No entanto, esta técnica cirúrgica associa-se a uma reduzida taxa de permeabilidade (64 a 75% aos 5 anos), elevada taxa de amputação (até 11% aos 5 anos) e a um risco de rotura do coto aórtico com hemorragia maciça (até 27%)5.
O risco de rotura do coto aórtico está relacionado quer com as consequências mecânicas a longo prazo de um coto aórtico curto, quer com as propriedades dos tecidos infectados remanescentes de uma ressecção incompleta. Existem várias técnicas descritas para diminuir este risco tais como sutura dupla, reforço com pledgets venosos, com fascia pre-vertebral ou epíploon. Neste caso os autores realizaram uma dupla sutura e reforço com patch de pericárdio bovino.
Nos doentes submetidos a revascularização extra anatómica, a taxa de reinfeção varia entre 0 a 27% dependendo das séries. A mortalidade aos 30 dias ronda os 18% e a mortalidade tardia varia entre 22 a 44%1. Apesar da antibioterapia prolongada, no caso clínico descrito houve uma re-infecção local, detectável no angio TC de follow-up sob a forma de abcesso justa coto aórtico, apesar ausência de clínica e parâmetros analíticos de infecção. Dados os sinais imagiológicos muito sugestivos de re-infecção e o baixo risco anestésico-cirúrgico, os autores optaram por re-abordar via retroperitoneal o coto aórtico, confirmando-se a presença de abcesso e infecção do patch de pericárdio bovino.
Segundo conhecimento dos autores, apesar da técnica de reforço do coto aórtico com patch de pericárdio bovino estar descrita, não existem casos descritos de re-abordagem cirúrgica deste por infecção do patch de pericárdio bovino.
Concluindo, em doentes que apresentem um reduzido risco anestésico-cirúrgico, uma estratégia cirúrgica agressiva oferece as melhores hipóteses de tratamento eficaz em contexto de infeção de prótese aórtica e posteriormente de infeção de patch de coto aórtico. No entanto estes doentes carecem de vigilância a longo prazo, assim como eventual antibioterapia prolongada. A utilização de pericárdio bovino como reforço da laqueação do coto aórtico pode aumentar o risco de re-infecção, pelo que a utilização de material autólogo deve ser privilegiada.
Responsabilidades éticas
Proteção dos seres humanos e animais.
Os autores declaram que os procedimentos seguidos estavam de acordo com os regulamentos estabelecidos pelos responsáveis da Comissão de Investigacão Clínica e Ética e de acordo com os da Associacão Médica Mundial e da Declaracão de Helsinki.