Introdução
A canábis (Cannabis sativa L) é uma planta cujos constituintes (sobretudo os canabinoides) têm vindo a ser associados a diversos efeitos psicoativos e medicinais.1-2 Já foram identificados mais de 100 canabinoides,1 presentes na planta sob a forma de ácidos.2 Os mais predominantes são, por ordem decrescente, o ácido tetrahidrocanabinólico (ATHC), o ácido canabidiólico (ACBD), o ácido canabigerólico (ACBG) e o ácido canabicroménico (ACBC). Após aquecimento, estes ácidos são descarboxilados e originam as suas formas neutras, das quais as mais importantes e abundantes são o tetrahidrocanabinol (THC), responsável pelos efeitos psicoativos, e o canabidiol (CBD).2 Com o desenvolvimento de canabinoides sintéticos, como dronabinol e nabilona, e a descoberta de ligandos endógenos aos recetores canabinoides cerebrais, os originários na planta receberam a denominação de fitocanabinoides.3
O uso potencial destes compostos para efeitos terapêuticos tem motivado alterações da legislação em alguns países.4 Em Portugal, a Lei n.º 33/2018, de 18 de julho, estabeleceu o quadro legal para a utilização de medicamentos, preparações e substâncias à base da planta da canábis para fins medicinais, nomeadamente a sua prescrição e a sua dispensa em farmácia.5 Foi complementada pelo Decreto-Lei n.º 8/2019, de 15 de janeiro, o qual regulamenta as atividades de cultivo, extração e comerciais envolvendo estas preparações.6 No ano de 2019, o INFARMED publicou uma lista de condições para as quais o uso de canabinoides com intuito medicinal se encontra aprovado, com a ressalva de que estes devem ser ponderados apenas nos casos em que os tratamentos convencionais com medicamentos autorizados não produzam os efeitos esperados ou provoquem efeitos adversos relevantes.7 Nessa lista encontra-se a dor crónica (seja de origem oncológica ou neuropática), que se define como dor que recorre ou persiste por mais de três meses e se associa a impotência funcional ou perturbação emocional.8
O médico de família é, habitualmente, o primeiro ponto de contacto dos utentes com os serviços de saúde e estabelece com eles uma relação de continuidade e proximidade. Este facto contribui para que seja muitas vezes solicitado a esclarecer informação científica. Por outro lado, será porventura o clínico que mais se ocupa da gestão de dor crónica. Assim, perante estas recentes aprovações e o aumento do interesse público no tema, é necessário que detenha a melhor informação disponível nesta área. Com esta revisão pretende-se avaliar a evidência existente relativa à eficácia destas substâncias no tratamento da dor crónica.
Métodos
Realizou-se, em agosto de 2019, uma pesquisa de meta-análises (MA), revisões sistemáticas (RS), estudos observacionais, ensaios clínicos e guidelines, publicados nas línguas portuguesa e inglesa, sem limite temporal, utilizando os termos MeSH cannabis e chronic pain nas bases de dados científicas MEDLINE/PubMed, The Cochrane Library, TRIP Database, National Guideline Clearing House e Canadian Medical Association Practice Guidelines.
Os critérios de elegibilidade foram os seguintes:
• População: indivíduos adultos com dor crónica, independentemente da causa;
• Intervenção: tratamento com substâncias derivadas da planta de canábis;
• Comparação: utilização de placebo ou tratamento com outros fármacos analgésicos;
• Outcome: melhoria sintomática, definida por diminuição da intensidade da dor.
Foram excluídos estudos que avaliassem a eficácia destas substâncias na dor aguda. Artigos de opinião e artigos de revisão clássica de tema foram também excluídos, à semelhança dos ensaios já incluídos em meta-análise ou revisão sistemática.
Utilizou-se a escala Strength of Recommendation Taxonomy (SORT), da American Academy of Family Physicians, para a avaliação dos níveis de evidência (NE) e da força de recomendação (FR).
Resultados
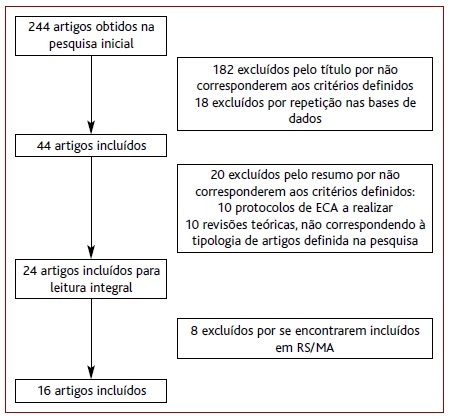
Da pesquisa realizada resultou um total de 244 publicações, dos quais 16 cumpriam os critérios de inclusão: três RS com MA, cinco RS, uma revisão de RS, quatro ensaios clínicos aleatorizados e controlados (ECAC), dois estudos retrospetivos de série de casos e um estudo prospetivo de série de casos. O fluxograma representado na Figura 1 resume o processo de seleção dos estudos, que se encontram resumidos nas Tabelas 1, 2, 3, 4 e 5.
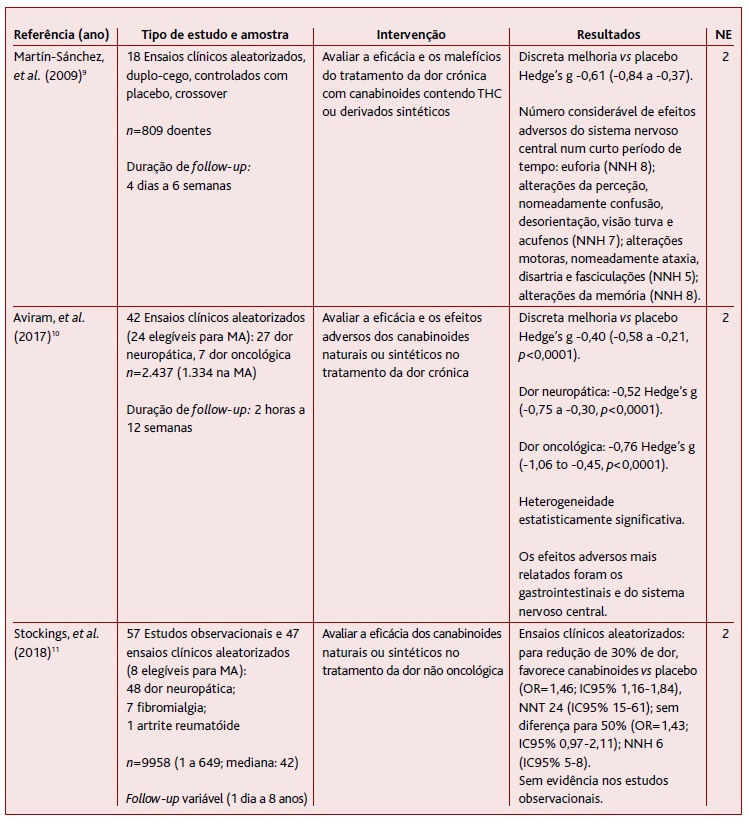
Das três RS com MA (Tabela 1), duas procuraram avaliar eficácia e efeitos adversos de qualquer preparação contendo canabinoides em doentes com dor crónica de várias causas, comparativamente com placebo.9-10 Os resultados favorecem ligeiramente a utilização destes compostos, no que diz respeito a melhoria sintomática, com tamanho do efeito (g de Hedges) de -0,61 (-0,84 a -0,37) no trabalho de Martín-Sanchez e colaboradores9 e de -0,40 (-0,58 a -0,21) na revisão de Aviram e colaboradores10 (NE 2). Aviram e colaboradores demonstraram que o efeito pode ser maior na dor neuropática e na dor oncológica, sobretudo pela via inalatória. No entanto, ambos os trabalhos fazem referência a efeitos adversos importantes, tanto nas funções cognitiva e motora9 como gastrointestinais10 (NE 2).
A RS com MA de Stockings e colaboradores estudou a eficácia de canabinoides em doentes com dor crónica não oncológica.11 Os ECAC incluídos na MA favorecem estas substâncias comparativamente com placebo para uma melhoria de 30% na intensidade da dor (Odds Ratio [OR]=1,46; IC95% 1,16-1,84), embora não se tenha demonstrado diferença para os 50% (OR=1,43; IC95% 0,97-2,11) (NE 2). Obteve-se, para 30% de melhoria, um Number Needed to Treat (NNT) de 24, com Number Needed to Harm (NNH) de 6. Os estudos observacionais incluídos na RS não demonstraram evidência.
As RS com MA apresentaram várias limitações. Em todas verificou-se grande variabilidade entre os ensaios incluídos, não só no que respeita ao desenho dos mesmos, mas sobretudo à heterogeneidade de intervenções e etiologia da própria dor. A maioria dos ensaios incluídos tinha amostras de pequena dimensão e intervenções de curta duração. Como tal, o NE atribuído a estes estudos foi de 2. Na MA de Martín-Sanchez e colaboradores é também feita referência a ensaios com cruzamento com período washout curto.9 Stockings e colaboradores afirmam haver alto risco de viés na maioria dos ECAC incluídos.11
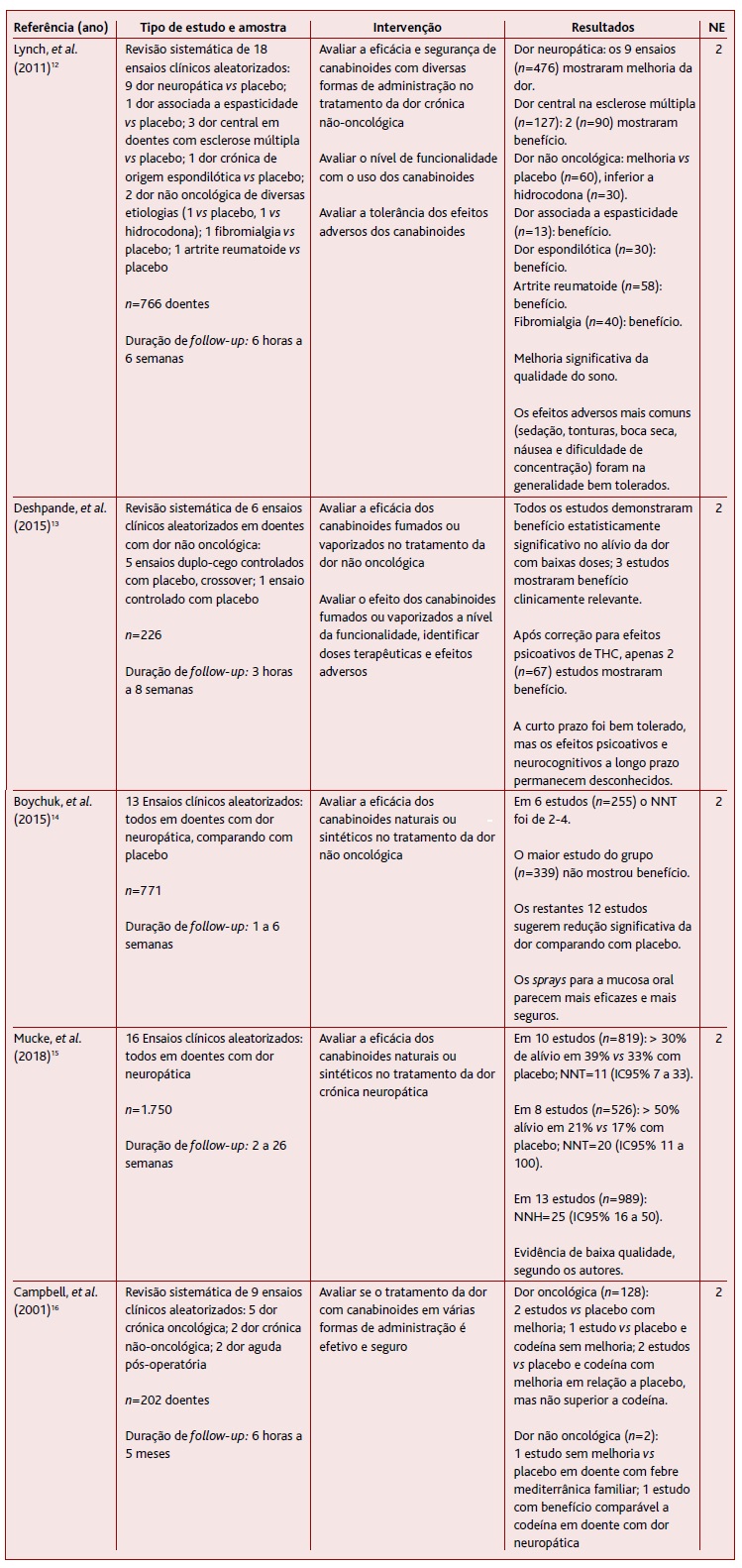
Das RS (sem MA) incluídas nesta revisão (Tabela 2), uma incidiu no tratamento de dor crónica não oncológica,12-14 três em dor neuropática13-15 e uma em dor crónica, independentemente da causa,16 avaliando a eficácia de diferentes preparações e formas de administração dos canabinoides. Dos dezoito ensaios incluídos na revisão de Lynch e colaboradores, nove incidiram em dor neuropática, tendo demonstrado benefício comparando com placebo sobretudo nas vias inalada e sublingual/mucosa oral.12 Um destes estudos comparou ainda nabilona com hidrocodona; o efeito deste canabinoide na dor foi menor. Poderá haver melhoria das queixas álgicas de origem central em doentes com esclerose múltipla (dois em três ensaios mostraram eficácia). Nesta revisão foi incluído um artigo incidindo na dor em doentes com fibromialgia, que demonstrou melhoria com nabilona oral. O único ensaio que abordou a dor na artrite reumatoide obteve bons resultados com spray para a mucosa oral. Na globalidade verificou-se boa tolerância aos compostos e sem efeitos adversos graves (NE 2).
Deshpande e colaboradores incluíram na sua RS seis ECAC que demonstraram benefício estatisticamente significativo na utilização de fitocanabinoides inalados para tratamento da dor neuropática.13 No entanto, apenas três apresentaram benefício clinicamente relevante, definido por melhoria da intensidade da dor superior a 30%. Após correção para os efeitos psicoativos dos canabinoides, dois ECAC mantiveram benefício demonstrado (NE 2). Não houve descrição de efeitos adversos graves.
Dos ensaios incluídos no artigo de Boychuk e colaboradores, apenas o que tinha maior amostra e que comparou nabiximols (spray para mucosa oral com fitocanabinoides THC e CBD) com placebo não demonstrou eficácia para dor neuropática.14 Os restantes fizeram-no, com seis ensaios a apresentar NNT variável entre 2 e 4, parecendo haver maior benefício na utilização destas mesmas preparações em spray para a mucosa oral (NE 2). Os efeitos adversos (sobretudo cognitivos) foram mais frequentes nos ensaios que administraram canabinoides através da inalação de fumo da planta. Uma limitação importante deste trabalho é não ter havido critérios estabelecidos para definição de “diminuição de dor”.
Mucke e colaboradores avaliaram 16 ensaios clínicos aleatorizados, dos quais 10 utilizaram nabiximols.15 Compilando a informação de dez desses ensaios, os autores obtiveram valores de alívio da dor neuropática superior a 30% em 39% dos doentes sob canabinoides, comparando com 33% daqueles a quem se atribuiu placebo, chegando a um NNT de 11 (IC95% 7-33). Para 50% de diminuição da intensidade da dor oito estudos continham informação, tendo-se atingido esses parâmetros em 21% dos doentes no braço terapêutico contra 17% no braço sob placebo, NNT de 20 (IC95% 11-100) (NE 2). Não se verificaram efeitos adversos clinicamente relevantes, tendo sido obtido um NNH de 25, com base em dados de 13 artigos. Os próprios autores classificam os estudos incluídos como de baixa qualidade.
A RS de Campbell e colaboradores, ao incluir estudos realizados em indivíduos com dor crónica, independentemente da causa, avaliou cinco ensaios clínicos realizados em doentes com dor de origem oncológica e dois em casos de dor não oncológica.16 Em relação à dor oncológica, os autores verificaram que um estudo não demonstrou melhoria sintomática, enquanto dois outros demonstraram superioridade em relação a placebo, mas não quando comparado com codeína (NE 2). Os artigos com resultados favoráveis utilizaram preparações de THC oral em doses variáveis (5-20mg), com maior incidência de efeitos adversos (sobretudo sedação e alterações cognitivas) nas dosagens superiores a 10mg. Na dor não oncológica, um artigo não demonstrou superioridade em relação a placebo, enquanto outro mostrou benefício superior a placebo e comparável a codeína. Em ambos foram utilizadas formulações de THC oral. Realça-se que ambos correspondem a estudos com cruzamento, mas apenas com um doente em cada estudo, o que não permite formular conclusões. Como sucedeu no trabalho de Boychuk e colaboradores, os critérios para definição de alívio de dor não foram especificados.
Como verificado nas RS com MA, às RS incluídas neste estudo atribuiu-se NE 2. As limitações das RS são semelhantes às explicitadas para as RS com MA, nomeadamente no que respeita ao tamanho das amostras dos ensaios e heterogeneidade das intervenções e de etiologias.
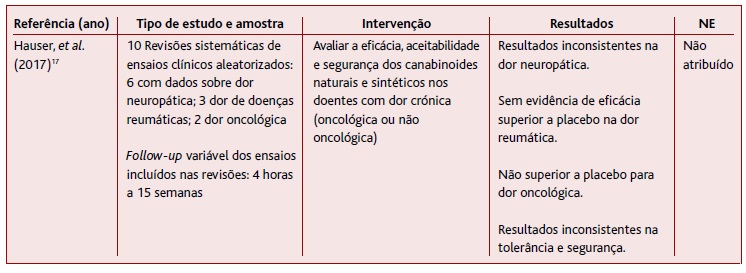
O trabalho de Hauser e colaboradores17 corresponde a uma revisão de RS (Tabela 3), uma metodologia recente que agrega a informação de diferentes RS que abordem o mesmo tópico.18 Foram incluídas 10 RS de ensaios clínicos aleatorizados, das quais seis abordaram a dor neuropática, três a dor de origem reumatológica e duas a dor oncológica. Nos ensaios clínicos incluídos em cada RS foram utilizadas diferentes substâncias, formas de administração e dosagens de canabinoides. Relativamente à dor neuropática, os resultados foram inconsistentes entre as RS, não permitindo inferir a eficácia. Não houve eficácia superior a placebo, tanto na dor de origem reumatológica como na oncológica. A este trabalho não foi atribuído nível de evidência dado tratar-se de uma metodologia não contemplada nos critérios da escala SORT.
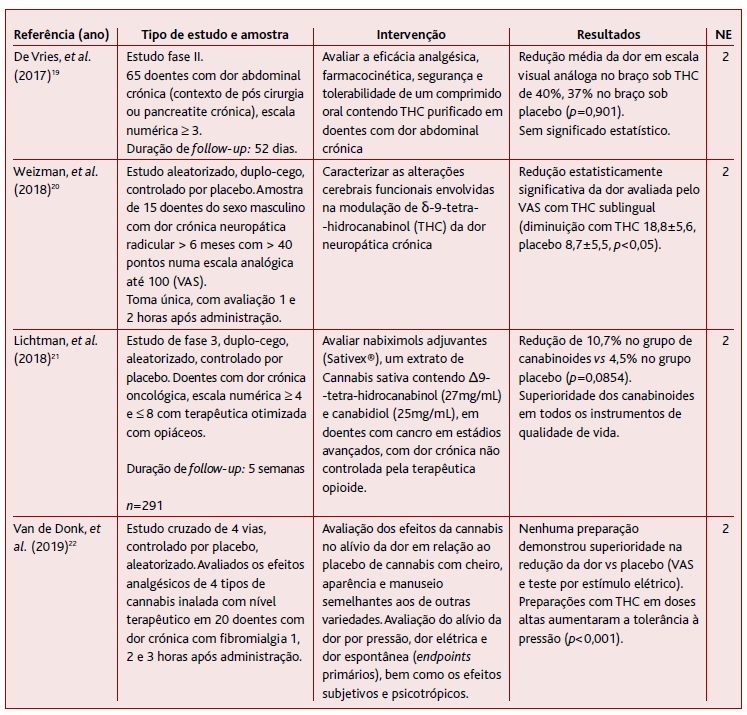
Relativamente aos ECAC (Tabela 4), todos os incluídos na revisão foram duplamente cegos. De Vries e colaboradores investigaram a eficácia de comprimidos de THC para a dor abdominal crónica em contexto pós-cirúrgico ou de pancreatite crónica, não tendo obtido melhoria estatisticamente significativa comparativamente com placebo (NE 2).19
O ECAC com cruzamento de Weizman e colaboradores incidiu em doentes com dor crónica neuropática radicular, avaliando a eficácia de THC sublingual.20 Verificou-se diminuição estatisticamente significativa da dor avaliada em escalas visuais com o THC sublingual (NE 2). No entanto, este estudo teve uma amostra de apenas 15 doentes, todos do sexo masculino e com avaliação em toma única.
Lichtman e colaboradores avaliaram a utilização de spray para a mucosa oral com THC e CBD na proporção de 1:1 em doentes com dor crónica de origem oncológica, já sob analgesia com opiáceos, ao longo de cinco semanas.21 Apesar de se ter verificado benefício através dos instrumentos de avaliação de qualidade de vida e ligeira melhoria das queixas álgicas no braço sob tratamento, esta não foi estatisticamente significativa (p=0,0854) (NE 2). Verificou-se heterogeneidade tanto no que respeita à origem da neoplasia como no tipo e dose de opiáceo realizado pelos doentes.
No trabalho de Van de Donk e colaboradores, um estudo com cruzamento, os autores investigaram os efeitos de diferentes preparações, contendo concentrações diferentes de THC e CBD, em mulheres com fibromialgia.22 Nenhuma preparação mostrou superioridade na redução da dor comparativamente com o placebo (NE 2).
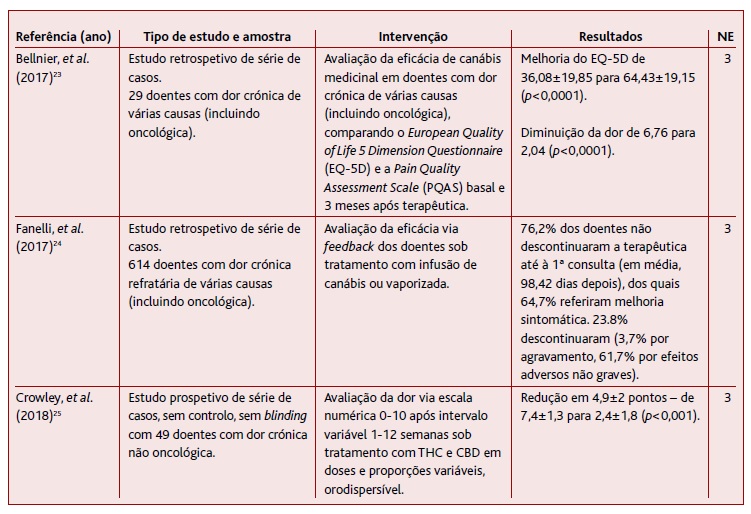
Os dois estudos retrospetivos de série de casos incluídos nesta revisão (Tabela 5) utilizaram amostras de doentes com dor crónica de diferentes etiologias, nos quais foram utilizados canabinoides em diferentes proporções e com diferentes formas de administração, excluindo a via inalatória.23-24 Bellnier e colaboradores obtiveram resultados de diminuição de dor de média de 6,76 para 2,04 em escala de avaliação da dor (p<0,0001) (NE 3).23 No estudo de Fanelli e colaboradores, os doentes foram submetidos a tratamento com canabinoides de administração oral com concentrações variáveis de THC e CBD.24 Dos 76,2% dos doentes que não descontinuaram a terapêutica até à primeira consulta de reavaliação, 64,7% referiram melhoria sintomática, não tendo sido utilizada nenhuma escala validada. Dos 23,8% que descontinuaram, 3,7% fizeram-no por agravamento das queixas e 61,7% por efeitos adversos não graves (NE 3).
O único estudo prospetivo incluído nesta revisão (Tabela 5) foi de Crowley e colaboradores, de uma série de casos, realizado em doentes com dor crónica não oncológica.25 Foram utilizados tratamentos com preparações orodispersíveis contendo CBD e THC em doses variáveis. Os autores obtiveram melhoria das queixas álgicas estatisticamente significativa (p<0,001) (NE 3).
Conclusões
De acordo com a literatura disponível atualmente, esta revisão permite concluir que a evidência para a utilização de canabinoides na dor crónica é limitada (FR B), com maior benefício potencial nos casos de dor crónica de origem neuropática e oncológica, para os quais há mais estudos realizados. A evidência atual não é suficiente para demonstrar benefício para a dor crónica por patologia do foro reumatológico (FR B).
No que respeita à dor neuropática, a maioria dos estudos incluídos demonstrou benefício desta terapêutica, destacando-se uma RS com MA,10 três RS12-13,15 e o ECA de Weizman e colaboradores.20 No entanto, para além das limitações já referidas para estes estudos, destaca-se o facto de o NNT para doentes com dor crónica não oncológica, calculado em duas destas RS com MA,11,15 variar entre 11 e 24. Estes valores são elevados, sobretudo quando comparados com os NNT para outros fármacos utilizados em dor crónica neuropática, como o caso da pregabalina (NNT 7,7), gabapentina (NNT 7,2), tramadol (NNT 4,7) e amitriptilina (NNT 3,6).26
Na dor crónica oncológica, a RS com MA de Aviram e colaboradores concluiu haver ligeiro benefício.10 O ECA de Lichtman e colaboradores não demonstrou alívio estatisticamente significativo da dor, mas melhoria na sensação de bem-estar e qualidade de vida dos doentes, potencial variável de confusão em alguns estudos.21
Dos artigos que abordaram a dor crónica de origem reumática, apenas os incluídos na revisão sistemática de Lynch e colaboradores mostraram diminuição das queixas álgicas.12 Dos restantes, nenhum demonstrou evidência para a utilização de canabinoides.17,22
A revisão de revisões sistemáticas não concluiu benefício para dor crónica de qualquer etiologia.17
Relativamente a efeitos adversos, a incidência destes parece estar relacionada com formulações com maior concentração de THC relativamente a CBD, tendo-se verificado heterogeneidade entre os estudos no que respeita às formulações utilizadas.24 O NNH obtido no trabalho de Stockings e colaboradores11 foi de seis, valor inferior ao de outros fármacos, como a pregabalina (NNH 13,9).26
A dor crónica, pelo impacto que apresenta na qualidade de vida dos doentes e, muitas vezes, pelo seu caráter incurável, constitui um desafio para os clínicos. O aparecimento de novos fármacos permite alargar o espectro da terapêutica a utilizar. No caso das formulações contendo canabinoides são necessários mais estudos, com amostras de maiores dimensões e mais homogéneas, por forma a que estas possam vir a ser consideradas opções terapêuticas que não de última linha. A forma de administração (oral/inalada/sublingual) e a concentração e proporção dos diferentes constituintes dos fármacos variam consideravelmente de estudo para estudo, resultando em evidência díspar e perfil de efeitos adversos variável, sendo também necessários ensaios de maior duração para avaliar a segurança destes fármacos a médio e longo prazo.
Com esta revisão, a prática do médico de família na abordagem da dor não sofrerá alterações. No entanto, este tema é atual e tem despertado crescente interesse de domínio público. Reforça-se a necessidade de o médico de família, como primeiro contacto do utente com o serviço de saúde, estar informado e facultar respostas tão cientificamente comprovadas quanto possível.