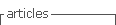Introdução
A vacinação evita 3.5 a 5 milhões de mortes por ano e auxilia na proteção contra mais de vinte doenças infeciosas em todo o mundo. (1 A vacinação foi um grande contributo da era moderna da medicina e constitui uma intervenção médica de saúde pública de sucesso e com um efeito positivo significativo na saúde da população mundial. Segundo a Organização Mundial da Saúde, é a segunda medida no âmbito da saúde pública com maior impacto na saúde e bem-estar das populações, apenas ultrapassada pelo fornecimento de água potável. (2
A Medicina Geral e Familiar é a especialidade em que, por excelência, a prevenção é uma tarefa primordial. Neste contexto, a vacinação reveste-se de uma elevada importância, como se constatou com o combate da pandemia à COVID-19.
A infeção por S. pneumoniae é um problema de saúde global responsável por 1.6 milhões de mortes por ano em todo o mundo, sendo a principal causa de morte prevenível através da vacinação. (3
Existem cerca de 100 serotipos capsulares do pneumococo serologicamente distintos. Todavia, um restrito número de serotipos é responsável pela maioria das doenças pneumocócicas, assim como existem diferenças etárias e geográficas na sua distribuição. A infeção por um determinado serotipo não induz proteção contra os restantes.
A infeção por S. Pneumoniae pode causar doença grave e está associada a morbilidade e mortalidade consideráveis. Tem um atingimento bastante variável, desde doença pneumocócica não invasiva (DNIP), sem bacteriemia, como pneumonia, otite média ou sinusite, a formas invasivas com bacteriemia e possível infeção secundária de locais à distância, como meningite, pneumonia, peritonite, artrite sética ou endocardite.
A taxa de incidência de doença pneumocócica é mais elevada nos extremos etários, ou seja, nas pessoas com idade inferior a dois anos e superior a 50 anos. O risco de doença pneumocócica aumenta com a idade, determinadas doenças crónicas e patologias com compromisso do sistema imune. (2
A maioria da população com mais de 50 anos não está vacinada contra o pneumococo e provavelmente a maioria não o faz por falta de aconselhamento médico. A população acima dos 65 anos, devido à imunosenescência, aliada muitas vezes a outros fatores como a imunodeficiência ou a doenças crónicas, é mais vulnerável a doenças infeciosas, como a doença pneumocócica. O médico de família deve ter um papel ativo na promoção da vacinação da população adulta, de forma a poder contribuir para um envelhecimento sem risco acrescido de doenças infeciosas potencialmente preveníveis pela vacinação.
A introdução das vacinas pneumocócicas conjugadas (PCVs) em crianças levou a alterações na incidência dos principais serotipos causadores de doença invasiva pneumocócica (DIP), não apenas em crianças vacinadas, mas também em adultos. Adicionalmente, o uso crescente da vacina polisacarídica 23-valente (PPV23) e da vacina conjugada 13-valente (PCV13) em adultos também contribuiu para a alteração dos principais serotipos causadores de DIP na população adulta.
Doença pneumocócica em Portugal
Em Portugal, no período entre 2006 e 2008, o uso da vacina pneumocócica conjugada 7 valente (PCV7) em crianças levou a uma diminuição da incidência dos serotipos incluídos na PCV7 como agentes causais de DIP em adultos. Os serotipos mais frequentes de DIP passaram a ser o 3, 1, 7F, 19A e 14. (4
Posteriormente, num estudo levado a cabo em Portugal no período compreendido entre 2015 e 2018, após a introdução das vacinas conjugadas PCV7 e PCV13 verificou-se uma diminuição da incidência de DIP pediátrica e alterações na distribuição dos serotipos. Os mais frequentemente encontrados foram o 3, 10A, 8 e 19A, destacando-se a importância do serotipo 8 na DIP do adulto. Os serotipos contidos na PCV13 foram responsáveis por cerca de 46% de casos de DIP. (5
Noutro estudo realizado na população portuguesa pelo grupo português de estudo de infeções estreptocócicas constatou-se que, após a introdução da PCV13 no Plano Nacional de Vacinação (PNV), os serotipos que mais frequentemente causaram DIP entre 2015 e 2018 foram os 8 e 3, seguidos dos 22F, 14 e 19A. (6 A infeção pelo serotipo 3 está associada a idade avançada e a maior mortalidade. O serotipo 8 associou-se a doença em adultos mais jovens, enquanto os serotipos 22F, 6C e 31 se associaram a doença nos mais idosos. Verificou-se associação entre a resistência antimicrobiana e a idade mais avançada, assim como com os serotipos 6C, 11A, 14, 15A, 19A e 19F. Constatou-se que, decorridos três anos da introdução da PCV13 em Portugal, houve uma estabilização da doença causada pelos serotipos contidos na vacina. Contudo, alguns serotipos vacinais, como o 3 e o 19A, continuam em circulação apesar de estarem contemplados nas vacinas PCV13 e PPV23 e outros serotipos não vacinais adquiriram importância no desenvolvimento de DIP. Os autores apontaram as seguintes taxas de cobertura vacinal para os serotipos causadores de DIP na população portuguesa: 13% para a PCV7, 36% para PCV13 e 80% para a PPV23. Com o lançamento de mais duas vacinas conjugadas, a PCV15 e a PCV20, e com base neste estudo, registar-se-ia uma taxa de cobertura para os serotipos vacinais de 44% e 72%, respetivamente, para estas novas vacinas.
O uso da PCV7 e da PCV13 em crianças teve um impacto moderado na redução da DIP entre adultos e crianças. Houve um aumento significativo de DIP causada por serotipos do tipo não vacinal entre adultos, especialmente naqueles com mais de 65 anos.
A incidência de doença em adultos causada pelos serotipos 3 e 19A do S. pneumoniae não foi reduzida, o que poderá ser explicado pelo serotipo tipo 3 não induzir uma resposta imune eficaz dos anticorpos e pelo serotipo tipo 19A não induzir uma resposta duradoura dos anticorpos.
Conhecer a realidade portuguesa revela-se importante, uma vez que apenas os serotipos 3, 14 e 19A estão incluídos na PCV13 e os serotipos 3, 19A, 8, 22F e o 14 estão incluídos na PPV23. Daqui resulta, na atualidade, a importância da vacinação sequencial com estas duas vacinas antipneumocócicas, com uma grande proporção de doença prevenível coberta pela vacinação nestes moldes.
Imunização pneumocócica
Antes do lançamento da PCV15 e da PCV20 existiam duas vacinas antipneumocócicas, a PCV13 conjugada e a PPV23 polissacárida, para a imunização da doença pneumocócica, sendo a vacina conjugada mais eficaz, porque induz maior imunogenicidade e memória imunológica através da indução de uma resposta imune T dependente.
A vacina PPV23 não induz uma resposta T dependente nem resposta imune ao nível da mucosa nasofaríngea, daí não ser eficaz nas crianças com menos de dois anos, nem na diminuição do estado de portador. A produção de anticorpos induzida pela vacina diminui ao longo do tempo e é menor e reduz mais rapidamente nos mais idosos, nos portadores de doenças crónicas e nas pessoas com imunodeficiência. Esta vacina, apesar de eficaz na redução de DIP no adulto para os serotipos incluídos, apresenta uma eficácia controversa e modesta na redução da DNIP, nomeadamente de pneumonia adquirida da comunidade. (7
A vacinação pneumocócica polissacarídea diminuiu o risco de eventos adversos cardiovasculares, como o enfarte agudo do miocárdio, na população vacinada, particularmente nos doentes com idade superior a 65 anos. (8
O esquema vacinal recomendado pela Direção-Geral da Saúde (DGS) e várias Sociedade Médicas em Portugal é a administração sequencial da PCV13 seguida da PPV23, com intervalo de seis meses a um ano, apesar de ter um intervalo mínimo de oito semanas. (9
A administração de uma vacina pneumocócica conjugada, como a PCV13, antes de uma vacina polisacarídica, como a PPV23, tem o potencial de aumentar a resposta imunológica à vacina polisacarídica, com estimulação das células B de memória.
O desenvolvimento das vacinas pneumocócicas conjugadas foi um avanço nos cuidados preventivos da doença pneumocócica. O seu sucesso deve-se à sua capacidade de prevenir diretamente a infeção em indivíduos imunizados e de induzir, indiretamente, imunidade de grupo por meio da redução das taxas de colonização nasofaríngea.
Recentemente foram aprovadas pela FDA (Food and Drug Administration), para pessoas com idade ≥18 anos, duas vacinas pneumocócicas conjugadas com 15 e 20 serotipos, a PCV1510-14 e a PCV20. (15-17 Comparativamente à vacina PCV13, a vacina PCV15 acrescenta os serotipos 22F e 33F. A vacina PCV20, para além dos serotipos da PCV15, inclui os serotipos 8, 10A, 11A, 12F e 15B. Todos estes novos serotipos contidos nestas duas vacinas conjugadas já estão incluídos na vacina PPV23. Os estudos realizados com ambas as vacinas mostraram eficácia, segurança, tolerabilidade e capacidade de indução de uma boa imunogenicidade, através de uma resposta imune robusta na produção de anticorpos para os serotipos adicionais incluídos, bem como a não inferioridade comparativamente às vacinas PCV13 e PPV23.
Atualmente, os serotipos circulantes mais frequentes de DIP na população portuguesa com ≥18 anos são o 8, 3, 11A, 22F e 9N. Destes, apenas o 3 e o 22F estão incluídos na PCV15. Na PCV20, para além dos já mencionados, estão ainda incluídos o 8 e o 11A, os quais, associados ao serotipo 3, também são uma causa frequente de DNIP. Esta maior cobertura da vacina PCV20 traduz-se numa maior eficácia vacinal para DIP estimada em cerca de 30%, com um benefício adicional na proteção de DNIP e, consequentemente, numa maior proteção global contra a doença pneumocócica.
Na Figura 1 estão representados os principais serotipos que constituem as vacinas pneumocócicas atualmente disponíveis, assim como os principais serotipos causadores de DIP na população portuguesa e a respetiva taxa de cobertura vacinal pelas várias vacinas.
Recomendações da vacina pneumocócica
A ACIP (Advisory Committee on Immunization Practices) da CDC (Centers for Disease Control and Prevention), em 2019, (18 recomendou a vacinação pneumocócica de todos os adultos com idade ≥65 anos e adultos com <65 anos com risco acrescido de infeção ou de complicações graves decorrentes da infeção pneumocócica. Para adultos com idade ≥65 anos recomendou a vacina PPV23. Nesta população não recomendou a vacina PCV13, a não ser que a pessoa tenha outra indicação para a vacina (e.g., asplenia ou imunossupressão), porque a incidência de doença pneumocócica causada por serotipos da vacina PCV13 era muito baixa, fruto da considerável cobertura vacinal da população no passado com a vacina PCV13. A dose de reforço da vacina PPV23 estava recomendada para pessoas selecionadas, nomeadamente os imunocomprometidos, uma vez que a imunidade às vacinas polisacarídicas diminui com o tempo.
A Norma n.º 011/2015, da DGS, atualizada em 01/11/2021, sobre a vacinação de adultos (≥18 anos de idade) contra infeções por Streptococcus pneumoniae de grupos com risco acrescido de DIP, introduziu algumas alterações.
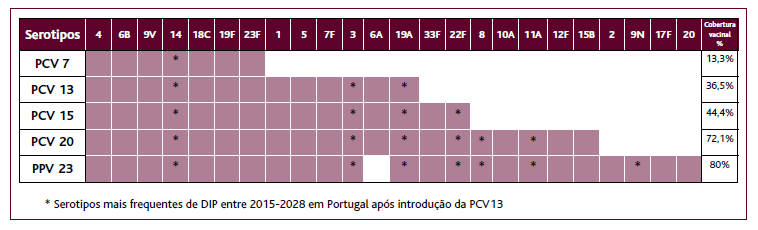
As principais atualizações foram as seguintes: recomendação da PPV23 para todos os adultos com idade ≥65 anos; gratuitidade da vacina PPV23 para grupos de risco selecionados, para os quais já era gratuita a vacina conjugada, PCV13; alargamento da gratuitidade, agora para ambas as vacinas, para pessoas com critérios de insuficiência respiratória crónica (insuficiência respiratória crónica em programa de oxigenoterapia de longa duração e insuficiência respiratória crónica grave - PaO2 <70 mmHg e FEV1 <50%), assim como para candidatos a transplante, aquando da inclusão na lista de espera ativa. Continuam a preconizar a vacinação sequencial a todas as pessoas com ≥18 anos imunocompetentes e portadoras de doenças crónicas, como doença cardíaca crónica, doença hepática crónica, dador de medula óssea antes da doação, diabetes, doença respiratória crónica e insuficiência respiratória crónica. A todas as pessoas com ≥18 anos de idade imunocomprometidas ou com risco acrescido de meningite bacteriana está indicado, adicionalmente, o reforço da vacina PPV23, pelo menos cinco anos após a dose anterior.
A Figura 2 traduz o algoritmo com as recomendações atualmente em vigor em Portugal, de acordo com a Norma n.º 011/2015, da DGS.
Segundo a Portaria n.º 200/2021, de 21 de setembro, (19 são comparticipadas a 69% a PPV23, para todas as pessoas com idade ≥65 anos, e a PCV13 para pessoas com idade ≥65 anos e uma das condições clínicas para as quais a gratuitidade se encontra prevista na Norma n.º 011/2015.
Face às vacinas conjugadas aprovadas nos Estados Unidas em 2022, o CDC publicou novas orientações para a vacinação pneumocócica em que recomendam as vacinas PCV15 ou PCV20 em adultos sem aplicação anterior de uma vacina conjugada, com idade ≥65 anos ou dos 19 aos 64 anos com certas condições subjacentes, como doenças crónicas, alcoolismo ou tabagismo. Recomendam ainda que a população adulta elegível pode seguir um esquema de vacinação apenas com a vacina PCV20 ou um esquema sequencial com a vacina PCV15 seguida da PPV23, tipicamente com intervalo ≥1 ano. (20
Recomendações futuras
Com a introdução no mercado nacional das duas vacinas pneumocócicas conjugadas, a PCV15 e a PCV20, e à semelhança das recomendações de 2022 do CDC e da evidência científica atual, será necessário adaptar as recomendações da DGS.
Face à realidade nacional, importa garantir uma maior cobertura vacinal contra os principais serotipos causadores de DIP e também de DNIP na população adulta portuguesa, nomeadamente nos portadores de doenças crónicas e de risco acrescido, como o alcoolismo e tabagismo, de forma a contribuir para um envelhecimento saudável e para uma redução da morbilidade e mortalidade por doença pneumocócica.
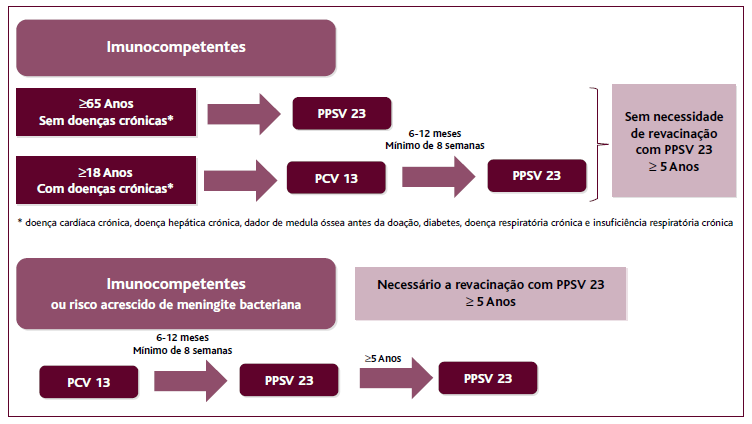
Nesse sentido, propõe-se, na Figura 3, uma atualização da recomendação da imunização para a doença pneumocócica na população adulta portuguesa.
É possível recomendar a toda a população portuguesa imunocompetente com ≥65 anos e às pessoas com ≥18 anos imunocompetentes e portadoras de doenças crónicas, ou à população imunocomprometida ou com risco acrescido de meningite bacteriana, uma estratégia simples e universal de vacinação, preferencialmente com uma única dose da vacina PCV20. Em alternativa, por decisão médica, poder-se-á optar pela estratégia de vacinação sequencial com a vacina PCV15 seguida, passado pelo menos um ano, da vacina PPV23. Contudo, independentemente de se poder vir a dar a livre opção ao médico pela escolha de uma das alternativas de vacinação sugeridas, entendemos que poderá ser mais adequado recomendar a realização preferencial apenas da vacina PCV20 a toda a população elegível. Suportamos esta opção atendendo à epidemiologia da doença pneumocócica, ao perfil de serotipos circulantes, à maior concordância vacinal de serotipos a nível nacional, à relevância dos serotipos 8 e 11A na DIP e na DNIP na nossa população, à maior efetividade e imunogenicidade da vacina conjugada, à maior simplicidade, à garantia de uma maior adesão e mais rápida cobertura vacinal e à otimização dos custos e ganhos em saúde. Face à aprovação da vacina PCV15 na população pediátrica, a estratégia vacinal proposta para a população adulta poderá ser reforçada com introdução da vacina PCV15 no PNV, em substituição da PCV13.
Neste cenário, as pessoas imunizadas apenas com a vacina PCV13 deverão complementar o esquema vacinal sequencial em curso com a vacina PPV23 ou PCV20. As pessoas imunizadas com a vacina PPV23 poderão realizar o reforço com a PCV15, mas idealmente com a PCV20.
Conclusão
A vacinação é reconhecidamente uma das medidas preventivas com maior impacto em termos de saúde pública a nível mundial, com obtenção de ganhos significativos em saúde para as populações.
O Streptococcus pneumoniae causa doença pneumocócica, sendo que as pessoas com ≥65 anos, portadoras de doenças crónicas ou imunocomprometidas têm um risco acrescido. As vacinas pneumocócicas reduzem a incidência de doença pneumocócica, nomeadamente de doença invasiva, corroborando a importância da vacinação da população adulta elegível.
A maior cobertura vacinal da população adulta poderá reduzir a carga de doença pneumocócica, refletindo a importância crescente da imunização. Fruto da dinâmica dos serotipos circulantes, muito determinada pela pressão vacinal, e do lançamento das novas vacinas conjugadas, PCV15 e PCV20, as recomendações deverão ser revistas face à evidência científica mais recente. Neste sentido, é fundamental a adequação periódica da estratégia vacinal.
Atendendo à realidade epidemiológica portuguesa da DIP, sugere-se a implementação preferencial de uma estratégia vacinal nacional simples e universal assente numa única dose da vacina conjugada PCV20. Esta opção poderá contribuir para uma maior adesão e superior cobertura vacinal, bem como uma mais rápida e duradoura obtenção de ganhos em saúde. Alternativamente, por decisão médica, poderá ser considerada a vacinação sequencial com a vacina PCV15 seguida da PPV23.
Contributo dos autores
Conceptualização, RC; metodologia, RC e RPC; validação, RC e RPC; investigação, RC e RPC; redação do draft original, RC e RPC; revisão, edição e validação do texto final, RC e RPC; supervisão, RC.