Introdução
Os Inibidores do Checkpoint Imunitário (ICI) revolucionaram o tratamento oncológico. Não obstante o seu mecanismo de ativação e proliferação dos linfócitos T na resposta tumoral imunitária têm um espectro de toxicidade único e amplo - referido como EAir - podendo potencialmente afectar todos os órgãos/sistemas desde graus ligeiros a graves ou serem fatais (Wang, Chen, Song et al., 2017).
Os dados estatísticos dos EAir têm sido amplamente divulgados sendo que o seu aparecimento foi descrito em até 80% dos doentes sob monoterapia e até 95% com terapia combinada (Inibidores programmed death protein-1 (PD-1) e T cell lymphocyte costimulation (CTLA-4)). Os sistemas dermatológicos, gastrointestinal, endócrino e hepático são os mais frequentemente atingidos. As doenças reumatológicas são, igualmente, outros dos EAir reportados nos ensaios clínicos (Champiat, Lambotte, Barreau et al., 2016; Postow, Sidlow e Hellmann, 2018).
Os EAir que afectam o sistema reumatológico são particularmente diferentes quer dos demais EAir quer das tradicionais doenças autoimunes, uma vez que podem surgir numa fase precoce do tratamento bem como ter um início tardio ou, ainda, poderem persistir cronicamente mesmo após o término da terapêutica (Jamal, Hudson, Fifi-Mah et al., 2020).
As doenças reumatológicas são classificadas em 2 grupos distintos: as doenças reumatológicas músculo-esqueléticas e as doenças reumatológicas não músculo-esqueléticas cuja incidência, em ambos os grupos, é bastante variável (1%-43%) quer em monoterapia (ICI) quer com terapêutica combinada (Benfaremo, Manfredi, Luchetti et al., 2018; Abdel-wahab, Suarez-almazor, 2019; Melissaropoulos, Klavdianou, Filippopoulou et al., 2020).
Em ensaios clínicos de grande dimensão publicados, é a patologia músculo-esquelética que apresenta maior incidência, nomeadamente as artralgias (até 40%), mialgias (2-20%), artrite inflamatória (AI) (≤7%), polimialgia reumática e miosite (<2%) Contudo há a registar outros EAir tais como vasculite, síndrome sicca, lesões ósseas de reabsorção, fracturas ósseas e sarcoidose (Cappelli, Gutierrez, Bingham et al., 2017; Benfaremo, Manfredi, Luchetti et al., 2018; Abdel-wahab, Suarez-almaz, 2019; Melissaropoulos, Klavdianou, Filippopoulou et al., 2020).
De acordo com Cappelli, Gutierrez, Bingham et al. (2017), embora raros, a verdadeira incidência da imunotoxicidade reumatológica é desconhecida ou mesmo subestimada devido a:
Inadequada caracterização - fraco reconhecimento dos sinais/sintomas;
Inconsistência das notificações - escassa clarificação relativamente aos critérios clínicos de distinção entre os diversos sintomas reumatológicos (diferentes maneiras de codificar/descrever o mesmo sintoma);
Utilização da Common Terminology Criteria for Adverse Events (CTCAE) nos ensaios clínicos na área da oncologia que definem o grau de severidade dos Eventos Adversos (EA) (Graus 1-2 ligeiro, graus 3 e 4 - severo e grau 5 indica óbito relacionado com EA) e estabelecem o respectivo tratamento;
Divulgação apenas de EA de grau ≥ 3, sendo os eventos reumatológicos excluídos, porque segundo a CTCAE versão 5.0 (2017), a EA como AI/derrame nas articulações/artralgia a atribuição de um grau 3 acontece quando existe necessidade de hospitalização ou compromisso total nas Actividades de Vida Diária (AVD).
Ao contrário dos ensaios clínicos, dados observacionais prospectivos demonstram uma incidência elevada, e por quantificar, de EAir reumatológicos. Constata-se que o conhecimento e a compreensão da prevalência e incidência bem como das características clínicas, da gestão óptima e prognóstico dos EAir reumatológicos continuam a evoluir a par com a experiência clínica contínua (Cappelli, Gutierrez, Bingham et al., 2017).
A gestão eficaz dos EAir requer uma abordagem multidisciplinar centrada no doente. Champiat, Lambotte, Barreau et al. (2016) propuseram uma abordagem prática para a gestão dos doentes sob imunoterapia, identificando cinco pilares norteadores para a gestão da imunotoxicidade, a prevenção (monitorização proactiva), antecipação, detecção, tratamento e monitoramento contínuo.
Embora as guidelines da pratica clínica desenvolvidas pelas European Society for Medical Oncology (ESMO) e pela American Society for Clinical Oncology (ASCO) careçam de ensaios clínicos no que diz respeito à gestão óptima dos EA e sendo a maioria das recomendações basedas na pratica e consenso clínicos, está determinado que o tratamento gold standard dos EAir é a corticoterapia e que a suspensão temporária dos ICI e o encaminhamento para a especialidade de reumatologia somente se torna necessária quando o grau de EAir >2. Para os doentes com sintomas ligeiros (Grau 1), o controlo sintomático é alcançado recorrendo-se à administração de AINE sem interrupção da imunoterapia (Haanen, Carbonnel, Robert et al., 2017; Brahmer, Lacchetti, Schneider et al., 2018).
Reacções de grau 2 implicam a instituição de corticosteroides orais (0,5 - 1,0 mg/kg/d), enquanto mantêm a terapêutica com ICI, iniciando-se o seu desmame gradual ao longo de 4 - 6 semanas. Nos casos mais graves (Grau ≥ 3) torna-se indispensável a administração de agentes biológicos imunossupressores (Disease-modifying anti-rheumatic drugs) bem como a suspensão definitiva da terapêutica com ICI (Haanen, Carbonnel, Robert et al., 2017; Brahmer, Lacchetti, Schneider et al., 2018; Benfaremo, Manfredi, Luchetti et al., 2018; Melissaropoulos, Klavdianou, Filippopoulou et al., 2020)
Para estas sociedades, o objetivo do tratamento dos EAir consiste em encontrar um equilíbrio entre a função imunológica e a administração de uma dose de imunossupressão específica que não diminua/comprometa a eficácia da imunoterapia, mas que concomitantemente seja suficiente para tratar o EA e possibilite a prevenção de danos nos órgãos.
O diagnóstico e tratamento tardios dos EAir reumatológicos têm impacto na QdV na medida em que estão associados a grande morbilidade, por provocarem limitações físicas e dor, que podem acarretar incapacidade funcional a longo prazo e consequente perda de autonomia, pelo que se torna crucial uma identificação precoce, gestão adequada e encaminhamento para a reumatologia (Steven e Fisher, 2019).
O re-challenge da terapêutica com ICI não é, habitualmente, recomendada para graus ≥ 3, contudo existem diversos factores que têm e devem de ser ponderados, tais como tipo e gravidade do EA, estadio e resposta tumoral, outras alternativas terapêuticas existentes e vontade do doente (Haanen, Carbonnel, Robert et al., 2017; Brahmer, Lacchetti, Schneider et al., 2018).
Segundo a European Society for Oncology Nursing, a Enfermagem Oncológica incide no tratamento do cancro, segurança e apoio da pessoa durante todas as fases da doença oncológica. Os Enfermeiros Oncológicos têm de estar na vanguarda do atendimento à Pessoa, com conhecimentos sobre o tratamento e seus EA e competências na gestão e educação da pessoa/família com intuito de limitar o seu agravamento/toxicidade severa, melhorar a QdV da Pessoa e diminuir custos sociais e económicos.
É a necessidade de estimar as necessidades afetadas, imediatas e a longo prazo, e planear os cuidados, físicos, de apoio emocional e de reeducação, que faz da enfermagem um serviço da maior importância. A consulta de enfermagem deve avaliar as necessidades de educação e conhecimento das pessoas em tratamento, para que participe nos processos de tomada de decisão, saiba controlar a sua doença e os sintomas associados ao tratamento e para consiga lidar com a experiência de ter um cancro (Henderson, 2007).
O programa de consulta de enfermagem de follow up delineado e sob coordenação de enfermeiros do hospital de dia de pneumologia (HDPNEU) e do hospital de dia de QT (HDQT), realiza-se ao longo do tratamento e pelo menos 2 anos após o seu término preconizando-se:
Consulta de enfermagem (CE) presencial de primeira vez, prévia ao tratamento, na qual se efetuará uma avaliação do estado geral com colheita de dados da pessoa incluindo o seu Performance Status (PS) e QdV, aplicação das escalas da Fadiga, Distress e Dispneia. Posteriormente são realizados ensinos acerca do papel da imunoterapia no tratamento do cancro e seu perfil de toxicidade e segurança; Disponibilização do contacto da equipa de enfermagem bem como se providencia material de leitura sobre os EA;
Consultas subsequentes telefónicas semanais, para antecipar e identificar EA e possibilitar a gestão dos sintomas, seguindo as guidelines da ESMO e CTCAE, comodamente a partir do domicílio;
Consultas não programadas em SOS.
O PS é um indicador decisivo e influenciador do tipo de tratamento a prescrever ao doente oncológico dado demonstrar o nível de autonomia e independência funcional daquele (avalia como a doença afecta as Actividades de Vida Diária (AVD) através da atribuição de um score de zero a cinco pontos) (Paredes, Simões, Canavarro et al., 2008; British Geriatrics Society, 2017).
A avaliação da QdV nos doentes oncológicos é fundamental, porque permite conhecer o impacto da doença e do seu tratamento, avaliar a eficácia dos tratamentos, aceder melhor ao doente, à sua evolução e adaptação à doença, melhorar o conhecimento acerca dos EA, definir, desenvolver estratégias e potenciar recursos pessoais com vista a uma melhoria do seu bem-estar, facilitar a sua reabilitação e proporcionar informação prognóstica relevante tanto para a resposta ao tratamento como para sobrevivência (Paredes, Simões, Canavarro et al., 2008).
A dor provocada pelas artralgias pode prejudicar o PS do doente e contribuir para uma deterioração da sua QdV. A dor torna-se o centro da atenção do doente, lembrando-lhe constantemente a existência de uma doença fatal e absorvendo toda a sua energia, levando a que a pessoa deixe de ser ela própria para passar a ser apenas a sua dor (Paredes, Simões, Canavarro et al., 2008).
Metodologia
Desenho de estudo
Pesquisa de natureza qualitativa e exploratória implementada de 1 de Dezembro de 2019 a 31 outubro de 2020 no Instituto Português de Oncologia de Lisboa.
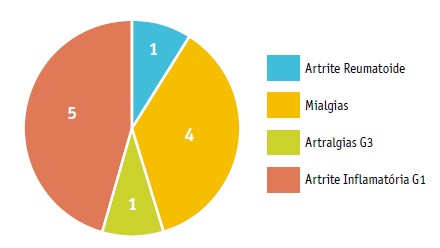
Os doentes foram selecionados tendo em conta o diagnóstico de cancro do pulmão e indicação para imunoterapia (pembrolizumab, nivolumab e durvalumab). Após consentimento informado para admissão no projeto de follow up, foram acompanhados 52 doentes. Onze doentes (21.6%) desenvolveram EAir reumatológicos (nenhum com doença auto-imune reumatológica conhecida), tal como patente no gráfico 1.
Objectivo
Descrever um estudo de caso em que tanto o PS como a QdV de um doente com Cancro do Pulmão submetido a terapêutica com ICI foram afetados pela imunotoxicidade reumatológica bem como o papel do enfermeiro na sua deteção precoce e os cuidados de enfermagem prestados de forma a minimizar o seu impacto na QdV.
RESULTADOS
Descrição do caso de enfermagem
Trata-se de um doente do género feminino, 77 anos, viúva, doméstica, vive sozinha numa moradia térrea. Tem 4 filhas. Hobbies: jardinagem.
Tem como Antecedentes Pessoais: DM II; HTA, angina de peito, depressão, psoríase.
Em abril de 2018 foi encaminhada ao IPOLFG para tratamento de um AdenoCarcinoma do Pulmão estadio IVa (mutações negativas; PD-L1 40%).
Iniciou 1ª linha com Carboplatina e Pemetrexed: 6 ciclos entre julho-novembro de 2018. Progressão de doença lenta até outubro de 2019. 2ª linha com Pembrolizumab (154mg 4/4semanas) em Dezembro pelo que é realizada uma CE de 1ª vez destacando-se PS1, EORTC QLQ-C30 (raw score 43 pontos; saúde global 6,5/Escala funcional 1.06/Escala sintomas 0,85) e Escala da Fadiga Normal. Programadas CEFU telefónicas semanais.
Janeiro de 2020:
1º ciclo sem EA. Na semana que antecede o 3º ciclo (20/01) exacerbação ligeira da psoríase e dorso-lombalgia (5/10 Escala numérica da dor) com irradiação para as coxas, sem rigidez muscular e/ou alterações da sensibilidade. Dor cede espontaneamente com o andar com agravamento ao afinal do dia. Reforçada a importância do exercício físico (recomendadas caminhadas 20 min/dia) e aplicação alternada de gelo e calor. Analgesia em SOS.
Cumpre 3º ciclo (27/01). Após 1 semana: restrita ao leito para conforto álgico. Incentivada a ir viver com uma das filhas para apoio nas AVD. Encaminhada para o pneumologista: ajuste da analgesia (opióide + analgésicos) com alívio parcial. Programa-se cintigrafia óssea.
Fevereiro de 2020:
4/02 Mantém quadro álgico com agravamento após o levante. Desmotivada (alteração rotina, cansaço). Distress 6. Sono comprometido. Contactado pneumologista - optimização terapêutica. Reforçados ensinos e medidas farmacológicas e não farmacológicas (gestão de esforços, higiene do sono, massagem, alternância do calor/frio). Incentivada a exploração e clarificação de sentimentos através de estratégias de âmbito psicoterapêutico. Utilização de técnicas de relaxamento progressivo para diminuição de ansiedade, o que facilitou o sono e aumento da resiliência. Cintigrafia óssea inconclusiva.
11/02 Recorre de modo não programado ao IPOLFG por quadro álgico descontrolado (8/10 Escala numérica da dor) + andar comprometido por dor ao nível da coxa bilateralmente quando faz carga + vómitos e intolerância alimentar. Sem alterações do trânsito intestinal. Informado pneumologista. Solicitada observação pelo neurologista que admite Lombalgia e Polirradiculopatia. Inicia AINE + repouso + TAC da coluna lombo-sagrada (não urgente).
17/2 Agravamento do estado geral (PS 2-3). Anorexia, períodos de náuseas e dificuldade na deglutição, perda de peso (-7kgs). Andar com apoio de canadiana. EORTC QLQ-C30 (raw score 73 pontos; saúde global 3,5/Escala funcional 3.06/Escala sintomas 1,85). Suspende temporariamente ICI. Inicia Corticoterapia (CCT).
24/2 Permanece em casa da filha para ter mais apoio. Cumpre analgesia com efeito. Nega dificuldade na deglutição, mas fezes endurecidas. Refere cansaço a pequenos esforços. Feito ensino sobre gestão de esforços, conservação de energia, hidratação, alimentação e terapêutica em SOS.
Março De 2020:
2/03 Segue as recomendações sobre o regime terapêutico acordadas. Dor controlada. PS2: regressou a casa. Refere hiperglicemias (300 g/dL) associadas a visão turva por períodos. Desmame lento do CCT.
9/03 Melhoria gradual da anorexia; mais animada; andar sem auxiliares de marcha; cuida do jardim. Sem dorsalgia/lombalgia.
17/3 TAC LS: sem metástases vertebrais. Alterações compatíveis com artroses em L4-L5.
20/3 Melhoria da sintomatologia (sem algias e aumento de apetite). Sem EA a registar. Glicémias capilares dentro dos valores estáveis. AVD não comprometidas. PS 1. Reforçada importância de realizar isolamento social na fase de pandemia. Incentivada a contactar se apresentar queixas.
30/3 Pára definitivamente Pembrolizumab.
Setembro De 2020:
Discussão
A doente apresentada neste estudo de caso, não obstante o PS1, pertence ao grupo dos idosos, tendo também diversas co-morbilidades prevalentes (DM II; HTA, angina de peito, depressão, psoríase) pelo que o conceito de frailty patient adequadamente lhe assenta. Os idosos considerados frailty patients estão e são mais suscetíveis às adversidades e às mudanças dramáticas ao seu bem-estar físico e mental decorrentes de um evento, aparentemente minor, e que desafia a sua saúde, como seja uma infecção ou a administração de um novo medicamento (British Geriatrics Society, 2017).
Para além disso, cuidar de uma pessoa idosa e à qual se acresce, ainda, uma doença oncológica é deveras exigente pela variante de condicionantes como as co-morbilidades, o decréscimo do status funcional, a polifarmácia e a disfunção de órgãos relacionado com a idade. Estas variáveis têm um significativo impacto na QdV, na tolerância à terapêutica e na sobrevivência (Hurria, Mohile, Gajra et al., 2016; Elias, Morales e Presley, 2017).
Os ensaios clínicos são peremptórios em afirmar que embora os idosos, na sua maioria, tenham mais toxicidades relacionadas com as terapêuticas standard, os resultados da eficácia da terapêutica revelam-se, contudo, semelhantes aos dos doentes mais jovens. A seleção criteriosa do doente, isto é, analisar e avaliar a suscetibilidade da pessoa à toxicidade imuno-mediada, torna-se, assim, essencial, porque no cenário do mundo real, muitas vezes, os doentes não são tão saudáveis quanto os inscritos nos ensaios clínicos (Noronha, Sekhar, Vijay et al., 2020).
Assim, a utilização de um novo medicamento - ICI (pembrolizumab) - em populações especiais como nos idosos, requer uma atenção especial devido à vulnerabilidade da pessoa seja pela cronicidade de outras doenças seja pela adaptação à doença ou pela necessidade de apoios sociais (Elias, Morales e Presley, 2017).
As publicações sobre EA em artigos científicos são feitos sobretudo nos ensaios clínicos que deram origem a novos fármacos (Champiat, Lambotte, Barreau, et al., 2016; Wang, Chen, Song et al., 2017; Postow, Sidlow e Hellmann, 2018).
A artralgia é, de entre os EA reumatológicos, aquele que surge com maior frequência (1 a 43%), no entanto é pouco valorizada por não constituir um problema eminente para a vida do doente (Benfaremo, Manfredi, Luchetti et al., 2018; Abdel-wahab, Suarez-almazor, 2019; Melissaropoulos, Klavdianou, Filippopoulou et al., 2020). No entanto é dos EA que mais perturba a pessoa, pois deixa-a com limitações físicas que podem dar origem a outras limitações, que vão contribuir para um decréscimo da QdV, como de facto se comprovou com a doente deste estudo de caso (Mooradian, Nasrallah, Gainor et al., 2018; Steven e Fisher, 2019).
O reconhecimento destas premissas impele a uma pro-actividade do enfermeiro na gestão, monitorização e controlo de sintomas destes doentes, na medida em que o seu papel é fundamental e determinante na identificação precoce dos efeitos da toxicidade imuno-mediada, conforme a descrição do estudo de caso apresentado.
O intuito dos planos educacionais consiste em garantir uma avaliação sistemática dos sintomas induzidos pelos tratamentos e o controlo/resposta imediata e atempada a toda e qualquer alteração causada ou experienciada pelo doente através das atividades educacionais realizadas, e assim promover a qualidade de vida e a segurança da pessoa oncológica (Aranda, Jefford, Yates et al., 2012).
Qual a melhor forma para realizar o acompanhamento a estas populações especiais com CPNPC submetidos a imunoterapia? O acompanhamento por telefone é uma intervenção de Enfermagem, estabelecida pela Nursing Interventions Classifications, que permite monitorizar as condições de saúde de um utente para actuar em situações de um estado anormal. O acompanhamento por telefone identifica antecipadamente a necessidade de alteração dos cuidados realizados no domicílio (Broens, Huis in’t veld, Vollenbroek-hutten et al., 2007; Butcher, Bulechek, Dochterman et al., 2018). Os contactos telefónicos são, assim, uma mais-valia na relação doente-enfermeiro e um potencializador para aprimorar o acompanhamento após tratamento dos doentes submetidos a terapêutica com ICI, porque contribuem para reduzir as idas ao hospital da área de residência/SANP do IPOLFG, detectar complicações potencialmente severas, diminuir a ansiedade dos utentes, esclarecer as dúvidas em momento oportuno e conferir segurança à díade utente-familia para gerir a sua situação a partir de casa.
A maioria dos EA são vivenciados no domicílio, pelo que se torna de extrema importância instruir a pessoa e os seus cuidadores para a ocorrência e monitorização contínua dos efeitos secundários da imunoterapia, para despiste precoce das toxicidades e sua respetiva gestão. Se a pessoa sentir que o tratamento lhe provoca efeitos adversos que não são manuseáveis existe a possibilidade de abandono do tratamento.
A CE deve emergir da necessidade de aplicar métodos mais eficazes para desenvolver a confiança e a motivação do doente para o seu potencial de autocuidado. Deve, igualmente, avaliar as necessidades de educação e conhecimento das pessoas em tratamento, para que participe activamente nos processos de tomada de decisão. É importante que a pessoa saiba identificar os sintomas associados ao tratamento e referi-los ao enfermeiro, para que este avalie a necessidade e planeie os cuidados, físicos, de apoio emocional e de reeducação (Mcilfatrick, Sullivan, Mckenna et al., 2007)
Garantir a manutenção da qualidade de vida da Pessoa com Doença Oncológica deve ser um dos principais objetivos para o Enfermeiro (Fabião, 2004). Com este caso clínico procurou-se identificar o problema que afetava a doente e que lhe trazia as limitações descritas.
Os algoritmos internacionais que descrevem a avaliação, gestão e tratamento específicos da toxicidade imuno-mediada orientaram uma parte do plano de cuidados de enfermagem. Estando perante o EA Artralgia Grau 1 este foi tratado inicialmente com analgésicos. No entanto, a resposta não foi satisfatória e a dor aumentou tendo provocado uma restrição de movimentos e progressivamente a permanência no leito, o que afectou a sua QdV. Com EA Grau 3 foi necessária a avaliação médica presencial e o início de corticoides. Obteve-se reversão do quadro, mas a terapêutica foi descontinuada (Haanen, Carbonnel, Robert et al., 2017; Brahmer, Lacchetti, Schneider et al., 2018).
Pelo efeito imunológico do fármaco conseguiu-se obter uma resposta parcial até os dias de hoje (Champiat, Lambotte, Barreau, et al., 2016; Wang, Chen, Song et al., 2017; Postow, Sidlow e Hellmann (2018).
Conclusão
Ao longo da doença e do seu tratamento são vivenciadas perdas e EA que comprometem habilidade funcionais, vocacionais e conduzem a uma incerteza quanto ao futuro.
As doenças reumatológicas estão entre os EAirs relatados com menos frequência mas têm um enorme impacto em todas as dimensões da pessoa.
A dor interfere com todas as mobilidades da pessoa dificultando a relação consigo mesma, com os outros e com a realidade circundante.
De todas as fontes de sofrimento, produzidas pela doença, o impacto da perda de autonomia e dependência progressiva são o mais desesperante, pois acresce maior sobrecarga para o cuidador e maior utilização dos recursos de saúde.
Apesar da maioria dos sintomas reumatológicos reportados serem considerados ligeiros a moderados e não acarretarem risco de vida, o seu espectro e curso de apresentação estão em contínua e franca descoberta, não existindo ainda uma visão clara de quais as melhores estratégias de gestão e controlo sintomático.
O enfermeiro detém um papel desafiante e fulcral na equipa multidisciplinar ao intervir ao nível da deteção e gestão precoces dos EAir reumatológicos com o intuito de alcançar um melhor controlo álgico, promover a autonomia e independência funcional e minimizar os efeitos das limitações apresentadas ou adquiridas pela pessoa ao longo do seu percurso de doença
Torna-se necessário encetar mais estudos prospectivos de forma a delinear melhor a prevalência e características das síndromes reumatológicas induzidas por ICI bem como desenvolver diretrizes terapêuticas relevantes.