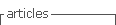Introdução
Após identificação de um novo coronavírus pelas Autoridades de Saúde Chinesas, a Organização Mundial da Saúde (OMS) declarou em janeiro de 2020, a existência deste novo vírus (o sétimo dos coronavírus infetantes para o homem), mais tarde designado de SARS-CoV-2, responsável pela doença denominada COVID-19, com uma clínica variável, desde casos assintomáticos até expressão clínica grave como pneumonia viral potencialmente fatal.1
Os primeiros casos confirmados de doença por coronavírus 2019 (COVID-19) em Portugal ocorreram em 02 de março de 2020 no Norte do país. Rapidamente se confirmaram novos casos a nível mundial, tendo sido declarada pela OMS disseminação pandémica em 9 de março.2
Em Portugal, perante a proliferação de casos registados de contágio, o Presidente da República declarou a 18 de março, o “Estado de Emergência” com início a partir das 00:00 de 22 de março.3
Em 26 de março, entrou em vigor a fase de mitigação da pandemia da COVID-19, por determinação da Direção-Geral da Saúde (DGS), envolvendo todo o sistema de saúde, público e privado, estando nessa data já reportados, na região de Lisboa e Vale do Tejo, mais de 1000 casos confirmados.4
Perante uma situação de pandemia, foi necessário de modo célere organizar as unidades hospitalares para esta nova realidade.
Como resposta à situação nacional, a Rede CUF decidiu disponibilizar, a 18 de março, o Hospital CUF Infante Santo (HCIS) como hospital de referência para o diagnóstico e tratamento de doentes com infeção pelo novo coronavírus na região da grande Lisboa.5
Neste contexto, surgiu a necessidade de organizar as equipas médicas para o internamento dos doentes com COVID-19. Criaram-se três níveis de internamento consoante a gravidade do doente, ficando o internamento do doente não crítico (IDNC) sob coordenação da Medicina Interna.
A equipa médica dedicada (EMD) a este internamento integrou médicos do HCIS, do Hospital CUF Sintra e do Hospital CUF Cascais e funcionou 24 horas, 7 dias por semana.
Houve um trabalho preparatório de formação da EMD para uma doença até então pouco conhecida, criando-se protocolos de avaliação e atuação, num tempo recorde de 1 semana, até ao internamento do primeiro doente com COVID-19, que aconteceu no dia 27 de março.
As recomendações para o tratamento farmacológico destes doentes foram baseadas em estudos in vitro de inibição da replicação viral de SARS-CoV-2; na evidência científica disponível à data, embora muito incompleta, inferida da experiência prévia de tratamento nos surtos de SARS-CoV-1 e MERS-CoV, além das orientações publicadas, para o tratamento da COVID-19, por entidades hospitalares e sociedades científicas nacionais e internacionais.6-11
Este estudo foi efetuado no HCIS e reporta as características demográficas, comorbilidades, resultados de exames complementares, terapêutica (baseada num protocolo interno), diagnósticos secundários e resultados dos doentes admitidos no IDNC.
Material e métodos
Estudo retrospetivo analisando todos os casos não críticos de COVID-19 admitidos no IDNC no período de 27 de março a 7 de maio de 2020.
O caso confirmado de COVID-19 foi definido laboratorialmente pela deteção de SARS-CoV-2 na zaragatoa nasofaríngea pelo teste de reverse-transcriptase-polymerase-chain-reaction (RT-PCR).12
Após avaliação nos Serviços de Atendimento Permanente (AP) da rede CUF, os doentes eram admitidos nos diferentes níveis de cuidados do HCIS de acordo com os critérios de internamento definidos. O IDNC recebeu doentes admitidos pelo AP do HCIS e transferidos do Hospital CUF Descobertas (HCD).
O doente não crítico foi definido clinicamente por ter um Modified Early Warning Score (MEWS) entre 0-2. Se score mantidamente acima de 3, tinham indicação para referenciação para nível mais elevado de cuidados (Tabela 1).13
Tabela 1: Score de deterioração clínica.
| Score de deterioração clínica - Modified Early Warning Signs (MEWS): | |||||||
| PARÂMETROS FISIOLÓGICOS | |||||||
| Sinais vitais | 3 | 2 | 1 | 0 | 1 | 2 | 3 |
| Frequência respiratória (cpm) | --- | < 9 | --- | 9-14 | 15-20 | 21-29 | ≥ 30 |
| Frequência cardíaca (bpm) | --- | ≤ 40 | 41-50 | 51-100 | 101-110 | 111-129 | ≥ 130 |
| Pressão arterial sistólica (mmHg) | < 70 | 71-80 | 81-100 | 101-199 | ≥ 200 | ||
| Temperatura (°C) | ≤ 35 | 35,1-38,4 | ≥ 38,4 | ||||
| Resposta a estímulos | Alerta | Reage à voz | Reage à dor | Não responsivo (GCS < 9) | |||
MEWS 0-2 - Doente estável com sintomas respiratórios e/ou sintomas sistémicos ligeiros a moderados. MEWS 3-4 - Sintomas respiratórios e/ou sistémicos moderados a graves, clinicamente instável, mas não crítico. MEWS ≥ 5 - Sintomas graves/pneumonia grave.
Foram admitidos no IDNC doentes com expressões clínicas diversas que se distribuíram por 4 grupos consoante a forma de apresentação clínica, laboratorial e imagiológica14-17:
Grupo I. Pneumonia e RT-PCR para SARS CoV-2 detetável;
Grupo II. Pneumonia e suspeita COVID-19 por critérios clínicos e imagiológicos com RT-PCR para SARS-CoV-2 não detetável;
Grupo III. Patologia não respiratória com critério de internamento e RT-PCR para SARS -CoV-2 detetável;
Grupo IV. Doentes paucissintomáticos/assintomáticos institucionalizados em residência sénior com RT-PCR para SARS-CoV-2 detetável (Tabela 2).
Excluíram-se da análise os doentes inicialmente suspeitos de terem COVID-19 nos quais não houve confirmação laboratorial por RT-PCR, durante o internamento e o diagnóstico final encontrado foi outro.
Foi considerado o dia do início dos sintomas como sendo o primeiro dia da doença.
Os dados foram coletados do processo clínico eletrónico e da base de dados criada pela EMD para registo de parâmetros protocolados para seguimento dos doentes internados no IDNC. Incluíram informação demográfica, comorbilidades, terapêutica de ambulatório, resultados dos exames complementares (laboratoriais, eletrocardiográficos e imagiológicos), opções terapêuticas de acordo com o protocolo interno, ocorrência de ventilação mecânica e necessidade de oxigenioterapia, diagnósticos secundários e resultados (incluindo demora média, destino na alta, readmissão e mortalidade). Utilizou-se o índice de comorbilidades de Charlson para quantificar o peso das comorbilidades e prever a sobrevida (um score superior a 6 corresponde a 0% de sobrevida a 10 anos.18-22
Resultados
Foram incluídos um total de 44 doentes (média de idades global de 67 anos; nos homens, 63 anos e, nas mulheres, 70,5 anos; intervalo de idades entre 29 e 94 anos); 52,3% eram homens (Tabela 2).
Ocorreu um pico de internamentos no dia 7 de abril, tendo o maior número de doentes sido admitido nas primeiras três semanas (Fig. 1).
Os doentes distribuíram-se por 4 grupos consoante a forma de apresentação: no Grupo I - 21 doentes (47,7%), no Grupo II - 12 doentes (27,3%), no Grupo III - 8 doentes (18,2%) e no Grupo IV - 3 doentes (6,8%) (Tabela 2).
Relativamente à proveniência dos doentes, 36 (81,8%) vieram do domicílio, 5 (11,4%) de residência sénior, e 3 (6,8%) vieram transferidos do HCD (Tabela 2).
Das comorbilidades conhecidas como fator de risco para doença COVID-19 mais grave, neste grupo de doentes as mais frequentes foram a idade > 65 anos (23; 52,2%), a hipertensão arterial (26; 59%), doença respiratória crónica (7; 15,9%), obesidade (7; 15,9%), neoplasia maligna ativa (6; 13,6%), diabetes (5; 11,4%), cardiopatia isquémica (5; 11,4%), insuficiência cardíaca (3; 6,8%), imunossupressão (3; 6,8%) (Tabela 2).23,24
A média do índice de comorbilidades de Charlson foi de 3,6 (índices variando entre 0 e 12) (Tabela 2) - para calcular o prognóstico a 10 anos.
Tabela 2: Características dos doentes.
| Nº. (%) | |
|---|---|
| Total Doentes | 44 |
| PROVENIÊNCIA | |
| Domicílio | 36(81,8) |
| Residência Sénior | 5(11,4) |
| HCD | 3(6,8) |
| MULHER/HOMEM | |
| Total | 21(47,7)/23(52,3) |
| Média de idades - anos | 70,5/63 |
| SINTOMAS NA ADMISSÃO | |
| Tosse | 24(54,5) |
| Febre | 19(43,2) |
| Dispneia | 11(25,0) |
| Mialgias | 8(18,2) |
| Toracalgia | 7(15,9) |
| Diarreia | 4(9,0) |
| Cansaço | 4(9,0) |
| Odinofagia | 4(9,0) |
| APRESENTAÇÃO CLÍNICA | |
| Grupo I | 21(47,7) |
| Grupo II | 12(27,3) |
| Grupo III | 8(18,2) |
| Grupo IV | 3(6,8) |
| COMORBILIDADES | |
| Hipertensão arterial | 26(59,0) |
| Doença respiratória crónica | 7(15,9) |
| Dislipidemia | 7(15,9) |
| Obesidade | 7(15,9) |
| Neoplasia maligna ativa | 6(13,6) |
| Diabetes mellitus tipo 2 | 5(11,4) |
| Cardiopatia isquémica | 5(11,4) |
| Tabagismo | 4(9,1) |
| Insuficiência cardíaca | 3(6,8) |
| Imunossupressão | 3(6,8) |
| Fibrilhação auricular | 3(6,8) |
| Demência | 2(4,5) |
| Doença renal | 1(2,3) |
| Depressão | 1(2,3) |
| SAOS | 1(2,3) |
| Índice de Comorbilidades de Charlson-média | 3,6 |
| Número de medicamentos de ambulatório - média | 5,3 |
| RT PCR SARS-CoV-2 | |
| Média de testes por doente | 2,95 |
| Resultado à entrada / saída: | |
| Detetável | 26/10 |
| Não detetável | 15/29 |
| Indeterminado | 3/3 |
| Não aplicável | 0/2 |
| SEROLOGIA CORONAVÍRUS-19 | |
| Número de testes | 14(31,8) |
| IgM(0 / >0<1 / >1) | 0 / 12 / 2 |
| IgG(0 / >0<1/ >1) | 7 / 4 / 3 |
| PADRÃO IMAGIOLÓGICO NA TC-T | |
| Localização “típica” | 30(68,2) |
| Localização “atípica” | 2(4,5) |
| Não sugestivo | 3(6,8) |
| Sem pneumonia | 9(20,5) |
| TEMPO DE SINTOMAS - DIAS | |
| Até ao diagnóstico | 7,43 |
| Até às complicações | 13,5 |
| MEWS médio | 1,18 |
| DIAGNÓSTICOS PRINCIPAIS | |
| Pneumonia | 33(75,0) |
| Traqueobronquite | 2(4,5) |
| Hemorragia digestiva | 2(4,5) |
| Cistite hemorrágica | 1(2,3) |
| Colecistite aguda | 1(2,3) |
| Diverticulite | 1(2,3) |
| Osteoporose fraturária | 1(2,3) |
| Espondilodiscite | 1(2,3) |
| Gastroenterite a SARS-CoV-2 | 1(2,3) |
| Colangite | 1(2,3) |
| DIAGNÓSTICOS SECUNDÁRIOS | |
| Insuficiência respiratória | 32(72,7) |
| Sobreinfeção bacteriana | 10(22,7) |
| ITU | 4(9,1) |
| Ventilação mecânica | 2(4,5) |
| Insuficiência cardíaca descompensada | 2(4,5) |
| Vertebroplastia | 2(4,5) |
| FA rápida | 1(2,3) |
| Anemia aguda | 1(2,3) |
| Neoplasia do pulmão | 1(2,3) |
| Osteoporose fraturária | 1(2,3) |
| Fractura traumática do olecrânio | 1(2,3) |
| Síndrome de Cushing | 1(2,3) |
| Rabdomiolise | 1(2,3) |
| Crise hipertensiva | 1(2,3) |
| Insuficiência renal aguda | 1(2,3) |
| Laminotomia | 1(2,3) |
| Orquiepididimite | 1(2,3) |
| Gripe A | 1(2,3) |
| TERAPÊUTICA ANTIMICROBIANA | |
| HCQ+AZT | 30(68,2) |
| HCQ | 2(4,5) |
| Sem terapêutica antimicrobiana | 11(25,0) |
| HCQ+Lopinavir | 1(2,3) |
| TEMPO MÉDIO DE TRATAMENTO - DIAS | |
| HCQ | 7,06 |
| AZT | 5,06 |
| Lopinavir+ Ritonavir | 5 |
| OUTRAS TERAPÊUTICAS | |
| Corticoterapia sistémica | 3(6,8) |
| Oxigenioterapia | 32(72,7) |
| Reinternamento | 1(2,3) |
| DESTINO | |
| Domicílio | 36 |
| Lar | 5 |
| HCD | 3 |
| Média de Internamento - dias | 10 |
| Mortalidade | 1,0(2,3) |
Apenas sete doentes (16%) não faziam qualquer terapêutica prévia. A média de medicamentos de ambulatório nos restantes foi de 5,3 (variação entre 1 e 16). Dos doentes hipertensos, 20 (77%) faziam uso de inibidores da enzima de conversão da angiotensina ou antagonistas dos recetores da angiotensina II (Tabela 2).
Tabela 3: Protocolo de tratamento da COVID-19 no internamento do doente não crítico (IDNC) - Medicina Interna. (cont.)
| COVID-19 - TRATAMENTO | ||||
| GRAVIDADE DA DOENÇA | QUADRO CLÍNICO | TRATAMENTO DE SUPORTE | Tratamento dirigido | Observações |
| Fármacos e Posologias | ||||
| Sintomas ligeiros + Com fatores de risco ## + Radiografia de tórax ou TC Torácica - Sem Pneumonia + Sat O2 ≥ 94% | Febre > 37,8ºC Tosse Coriza Obstrução nasal Anosmia Mal-estar Mialgias Sem dispneia | Tratamento sintomático EM INTERNAMENTO NA ENFERMARIA + O2 suplementa se SatO2 < 92% (ar ambiente) com objetivo de SatO2 -90% a 94% (conforme controlo sintomático) | Hidroxicloroquina: 400 mg de 12/12h nas primeiras 24h, depois 200 mg de 12/12h durante mais 5-7 dias - conforme benefício terapêutico OU Fosfato de Cloroquina: 500 mg de 12/12h durante 5-7 dias - conforme benefício terapêutico + Lopinavir/ritonavir: 200/500 mg - 2 cp 12/12h (7-14 dias) ** E/OU Azitromicina: 500 mg/dia em D1, depois 250 mg/dia de D2-D5, PO/EV | Ponderar terapêutica antibiótica (empírica ou dirigida) e/ou antiviral (Oseltamivir) de acordo com quadro clínico, epidemiologia local e discussão Multidisciplinar (Medicina Interna, Pneumologia, Medicina Intensiva) OBRIGATÓRIO: ECG de base (caso não tenha sido realizado na urgência) e repetição de acordo com a terapêutica ** ponderar lopinavir/ritonavir até 28 dias, consoante evolução |
| Sintomas respiratórios e/ou Sintomas sistémicos moderados (MEWS 0-2) + Radiografia de tórax ou TC Torácica -Com evidência de Pneumonia não grave + Sat O2 ≥ 94% | Febre > 37,8ºC Tosse Mal-estar Mialgias Dispneia Prostração Astenia Sem critérios de gravidade laboratorial Sem sinais dificuldade respiratória grave (ex. tiragem, taquipneia) | Tratamento sintomático EM INTERNAMENTO NA ENFERMARIA + O2 suplementar se SatO2 < 92% (ar ambiente) com objetivo de SatO2 -90% a 94% (conforme controlo sintomático) | Hidroxicloroquina: 400 mg de 12/12h nas primeiras 24h, depois 200 mg de 12/12h durante mais 7-10 dias - conforme benefício terapêutico OU Fosfato de Cloroquina: 500 mg de 12/12h durante 7-10 dias - conforme benefício terapêutico + Lopinavir/ritonavir: 200/500 mg - 2 cp 12/12h (7-14 dias) ** E/OU Azitromicina: 500 mg/dia em D1, depois 250 mg/dia de D2-D5, PO/EV | Ponderar terapêutica antibiótica (empírica ou dirigida) e/ou antiviral (Oseltamivir) de acordo com quadro clínico, epidemiologia local e discussão Multidisciplinar (Medicina Interna, Pneumologia, Medicina Intensiva) OBRIGATÓRIO: ECG de base (caso não tenha sido reaizado na urgência) e repetição de acordo com a terapêutica ** ponderar lopinavir/ritonavir até 28 dias, consoante evolução |
| Sintomas respiratórios moderados, clinicamente instável, mas não crítico (MEWS 3-4) + Sat O2 < 94% | Dispneia moderada Frequência respiratória elevada SpO2 periférica baixa ou Alterações gasimétricas Doente ainda não crítico e sem sinais de alarme (falência respiratória grave, dificuldade respiratória grave, perturbação da consciência, hipotensão ou choque) | Tratamento sintomático e internamento em CUIDADOS INTERMÉDIOS (sempre que possível) + O2 suplementar se SatO2 < 92% (ar ambiente) com objetivo de SatO2 -90% a 94% (conforme controlo sintomático) | Idem ao estádio prévio - e de acordo com Protocolo da UCI | Idem ao estádio prévio Considerar corticoterapia sistémica (Metilprednisolona ev - 1 a 2 mg/kg/dia - 5 dias ou dexametasona 0,2-0,4 mg/kg/dia - 5 dias) quando broncospasmo marcado e em caso de ARDS, choque séptico, encefalite e síndrome hemofagocítica Ponderar Interferão β1b nos casos mais graves (0,25 mg SC de 48/48h - 14 dias) Necessidade de monitorização contínua Reavaliação clínica apertada - PaO2/FiO2 ≤ 250 - 300 -> Nível de cuidados superior - Transferência para Unidade de Cuidados Intermédios |
## Idade ≥ 65 anos, patologia cardiovascular crónica (hipertensão arterial, cardiopatia isquémica, insuficiência cardíaca, doença renal crónica, doença vascular cerebral, taquidisritmia), patologia respiratória crónica (doença pulmonar obstrutiva crónica, asma mal controlada, bronquiectasias), diabetes mellitus, neoplasia maligna ativa, obesidade (índice de massa corporal > 30 kg/cm2), imunossupressão
Na admissão, os sintomas mais referidos foram: tosse (24; 54,5%), febre (19; 43,2%), dispneia (11; 25%), mialgias (8; 18,2%), toracalgia (7; 15,9%), diarreia (4; 9%), cansaço (4; 9%) e odinofagia (4; 9%). O tempo médio de sintomas até ao diagnóstico foi de 7,43 dias (entre 1 e 15 dias) (Tabela 2).
O primeiro teste por RT-PCR para COVID-19 foi positivo em 26 doentes (59,1%), negativo em 15 doentes (34,1%) e indeterminado em 3 doentes (6,8%); 6 dos doentes inicialmente negativos vieram positivos num teste subsequente, perfazendo um total de 32 doentes (72,7%) cujo diagnóstico se confirmou laboratorialmente. E em média foram realizados 2,75 testes RT-PCR por doente (Tabela 2).
Todos os doentes suspeitos, mas não confirmados por teste RT-PCR, no momento da alta repetiram este teste PCR e realizaram serologias, havendo a confirmação adicional em um doente para COVID-19 por apresentar IgM e IgG positivos, aumentando para 33 (75%) o total de doentes com confirmação laboratorial (Tabela 2).12
Todos os doentes com clínica respiratória (35; 79,5%) realizaram tomografia computorizada torácica (TC-T) sendo encontrados diversos padrões imagiológicos já descritos na literatura como infiltrados em vidro despolido (32; 72,7%) com distribuição maioritariamente bilateral, periférica, posterior e nos lobos inferiores, alguns destes também com padrão “em mosaico”, bandas fibróticas e consolidação periférica. Em três doentes (6,8%), o padrão imagiológico da pneumopatia não era sugestivo, apesar de terem RT-PCR detetável para SARS-CoV-2.14-17
Realizaram-se eletrocardiogramas seriados para monitorizar o potencial efeito secundário cardíaco dos fármacos antimicrobianos adotados. Mediu-se o intervalo QTc no início e durante o período de administração destas terapêuticas, não tendo havido prolongamentos significativos do QT que obrigassem a suspender estes fármacos. O QTc médio inicial foi de 424 ms (variando entre 308 e 488) e, sob terapêutica, o QTc médio foi de 422 (variando entre 375 e 479).
O protocolo de intervenção terapêutica antimicrobiana dirigida incluiu hidroxicloroquina associada a azitromicina (HCQ+AZT) em 30 doentes (68,2%), hidroxicloroquina em monoterapia em dois doentes (4,5%) e hidroxicloroquina associada a lopinavir-ritonavir em um doente (2,3%). Não houve critérios para intervenção terapêutica em 11 doentes (25%).
O tempo médio de tratamento com HCQ foi de 7,1 dias, com AZT de 5,1 dias e com lopinavir-ritonavir de 5 dias.
Em três doentes (6,8%) introduziu-se corticoterapia sistémica e em 32 (72,7%) oxigénio suplementar.
A coinfeção respiratória ocorreu por vírus Influenza A num doente (2,3%) e presumivelmente por microrganismo bacteriano em 10 doentes (22,7%).
Houve agravamento clínico significativo em quatro doentes (9,1%), num deles ocorrendo o óbito e em três (6,8%) houve necessidade de escalar cuidados para uma Unidade de Cuidados Intensivos (UCI), dois no HCIS e um para hospital público. Estes doentes da UCI do HCIS necessitaram de ventilação mecânica invasiva com um tempo médio de 5 dias. O tempo médio de sintomas até este agravamento foi de 13,5 dias (Tabela 2).
Os diagnósticos secundários mais frequentes foram: insuficiência respiratória em 32 doentes (72,7%), com necessidade ventilação mecânica em 2 (4,5%); coinfeção respiratória bacteriana em 10 (22,7%); infeção do trato urinário (ITU) em 4 (9,1%) (Tabela 2).
A demora média de internamento foi de 10 dias. Dos doentes que sobreviveram, o destino na alta foi em 35 para o domicílio, cinco para residência sénior (local de proveniência) e três transferências para hospital público (perdendo-se o seguimento) (Tabela 2).
Não houve readmissões por COVID-19, mas ocorreu um reinternamento por patologia abdominal aguda num doente ainda com RT-PCR detetável.
Registou-se um óbito num doente do género feminino, correspondendo a uma mortalidade de 2,3% (Tabela 2).
Discussão
A casuística apresentada representa o primeiro grupo de doentes não críticos internados com infeção por SARS-CoV-2 na Rede CUF da Região de Lisboa (no HCIS).
A média de idades foi superior a 65 anos (sendo esta faixa etária a de pior prognóstico nesta doença), a maioria do género masculino. Apesar da hipertensão arterial ter sido o fator de risco mais prevalente, esta população apresentou muitos dos restantes fatores de risco para doença grave e mau prognóstico já identificados em estudos publicados.20-23
Ocorreram casos de doentes com RT-PCR não detetável em que a TC-T colocou a hipótese diagnóstica de COVID-19, alguns deles posteriormente confirmados por novos testes PCR e/ou serológicos, mantendo-se o diagnóstico presuntivo em 25%, na falta de testes laboratoriais com elevada especificidade e perante uma apresentação clínica e laboratorial sugestiva. A TC-T demonstrou-se crucial para o diagnóstico nesta população.
Em 75% dos doentes instituiu-se terapêutica antimicrobiana “antiviral” segundo o protocolo, com tolerância e aparente eficácia, embora não existisse um grupo controlo.
Dos três doentes transferidos para UCI, os 2 que permaneceram no HCIS necessitaram de VMI e regressaram ao IDNC, tendo posteriormente alta. O doente transferido para o hospital público perdeu-se para o seguimento.
A mortalidade intra-hospitalar foi baixa (2,3%) embora existisse um índice de comorbilidades de Charlson médio de 3,6 e se tratasse de uma população polimedicada.
O facto de a amostra ser pequena e se tratar de uma análise retrospetiva, condiciona a interpretação destes resultados.
Conclusão
Descreve-se a experiência vivida na abordagem da COVID-19, espelhando o imenso desafio que foi tratar uma doença até agora desconhecida para esta equipa médica.
Esta série de casos descreve as características da população de doentes não críticos com infeção pelo novo coronavírus, internados a cargo da Medicina Interna no HCIS na fase inicial do surto pandémico em Portugal.
Aplicaram-se os protocolos de avaliação e atuação especialmente criados para esta situação, pela equipa médica dedicada, à luz do conhecimento então existente.
A vigilância apertada destes doentes e a existência de uma equipa de Medicina dedicada (24 horas/7 dias por semana) capaz de detetar e adequar precocemente os cuidados, terá seguramente contribuído de forma decisiva para os bons resultados alcançados.
Perante as incertezas sobre a eficácia das atuais opções terapêuticas, mas sendo reconhecido que populações mais idosas e com multimorbilidade, como a apresentada, têm pior prognóstico, os resultados obtidos foram muito satisfatórios.