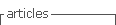Introdução
Em dezembro de 2019, foi identificado na China, nomeadamente na província de Hubei, um surto pelo novo coronavírus SARS-CoV-2. Desde então, vários milhões de casos surgiram por todo o Mundo. A precocidade do diagnóstico, isolamento e tratamento destes doentes é essencial para reduzir a transmissão humana, nomeadamente entre os contactos próximos e os profissionais de saúde, prevenindo a sua disseminação explosiva. Seguindo as recomendações para o diagnóstico e tratamento da pneumonia causada pelo novo coronavírus SARS-CoV-2, e de acordo com a prática clínica adquiria na província de Hubei, a análise por RT-PCR (reverse transcriptase polymerase chain reaction) das secreções respiratórias foi a usada para detetar o vírus. Contudo, alguns investigadores e médicos argumentaram que a imagiologia pulmonar por tomografia computorizada, serviu para identificar vários casos com infiltrados pulmonares múltiplos, bilaterais, periféricos e em vidro despolido, em doentes com resultados por RT-PCR negativos.1
Pelo Mundo inteiro verificou-se uma necessidade crescente em realizar testes diagnósticos para a COVID-19, com um encorajamento da Organização Mundial da Saúde em “testar, testar, testar”.
A identificação do genoma completo do vírus, precocemente na epidemia, facilitou o desenvolvimento de testes para detetar o seu RNA. Múltiplos ensaios com diferentes alvos genéticos foram desenvolvidos, usando a RT-PCR. Estes testes utilizam normalmente amostras obtidas do trato respiratório, através de zaragatoas nasofaríngeas. A testagem para a COVID-19, permite, para além da identificação dos indivíduos infetados e rastreamento dos seus contactos próximos, apurar as taxas de infeção regionais e nacionais, de forma a orientar as intervenções da Saúde pública. Contudo, permanecem várias questões de como aplicar corretamente o resultado destes testes, de modo a tomar as decisões mais adequadas para os doentes e população.2
Com este caso clínico pretendemos chamar a atenção para a problemática do diagnóstico e orientação clínica desta nova identidade COVID-19, que de forma exponencial e extremamente rápida invadiu a nossa prática clínica diária.
Caso clínico
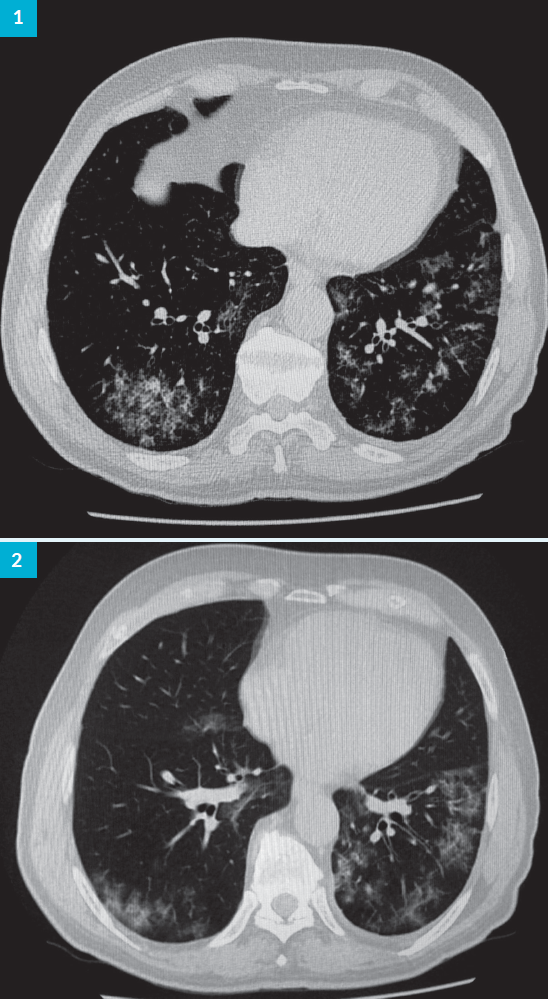
Doente do sexo masculino, 67 anos de idade, com história prévia de hipertensão arterial essencial e glaucoma, medicado em ambulatório com olmesartan/hidroclorotiazida e timolol/dorzolamida. Descreve quadro com dez dias de evolução caracterizado por febre, astenia e mialgias, tendo já efetuado ciclo de antibioterapia com azitromicina, por alegada pneumonia da comunidade. Recorreu ao Atendimento Permanente do Hospital CUF Torres Vedras, a 27/03/2020 por manutenção do quadro. Salientava-se, gasimetria bem ventilada e oxigenada, analiticamente com linfopénia de 1210/mm3, PCR 8,3 mg/dL, LDH 404 U/L, AST 90 U/L e ALT 73 U/L. Pesquisa de SARS-CoV-2 inconclusivo no exsudado faríngeo. Radiologicamente infiltrados subpleurais bilaterais. Reavaliado a 29/03/2020, apresentando hipoxemia discreta de 74 mmHg. Análises sobreponíveis com d-dímeros de 759,61 ng/mL. Pesquisa de SARS-CoV-2 negativo no exsudado faríngeo. Tomografia computorizada do tórax com áreas de densificação em vidro despolido, com envolvimento bilateral e distribuição preferencialmente periférica, enquadráveis num contexto de processo inflamatório/pneumonia atípica (Fig.s 1 e 2). Dada a elevada suspeição de pneumonia por SARS-CoV-2, foi transferido para o Hospital CUF Infante Santo. Iniciou protocolo terapêutico com hidroxicloroquina (400 mg bid no primeiro dia e posteriormente 200 mg bid) durante 7 dias e azitromicina (500 mg no primeiro dia e posteriormente 250 mg/dia) durante 5 dias. Repetiu pesquisa de SARS-CoV-2 no exsudado faríngeo, a 31/03/2020 que se revelou positivo. Evolução favorável, do ponto de vista clínico, com apirexia mantida, e analítico, tendo alta clínica ao sétimo dia de internamento.
Discussão
O teste mais frequentemente usado e confiável para o diagnóstico da COVID-19 tem sido a RT-PCR, realizado após colheita do exsudado nasofaríngeo, orofaríngeo, ou mais recentemente de saliva. Na maioria dos doentes sintomáticos, o RNA viral nasofaríngeo é detetável desde o primeiro dia dos sintomas, mas o seu pico surge a partir da primeira semana. No entanto, uma PCR “positiva” reflete apenas a deteção do RNA viral e não indica necessariamente a presença de vírus viáveis, podendo o teste manter-se positivo mesmo após a sexta semana pós-diagnóstico. Foram ainda relatados casos positivos após 2 testes negativos consecutivos, realizados com 24 horas de intervalo. Não está claro se é um erro do teste, reinfeção ou reativação. Num estudo com 205 doentes com infeção confirmada, a positividade da RT-PCR foi maior em amostras de lavado broncoalveolar (93%), seguidas de secreções brônquicas (72%), esfregaço nasal (63%) e esfregaço faríngeo (32%). Os falsos negativos ocorreram principalmente devido à análise precoce em relação com o início da doença e também por incorreta colheita de amostra, principalmente nas zaragatoas nasofaríngeas.
Os falsos positivos podem ocorrer, ocasionalmente, devido a erros técnicos, como a contaminação do reagente.3
Para além do tipo de amostra, a precisão do teste varia em função do estadio da doença, grau de replicação e de eliminação do vírus.2 É ainda mais sensível nos doentes com sintomatologia sugestiva de síndrome gripal, nomeadamente nos que apresentam febre.1
Recomenda-se que o diagnóstico microbiológico seja efetuado por PCR em tempo real nas amostras do trato respiratório superior (exsudado da nasofaringe e orofaringe, colhidos com zaragatoa), sempre que possível associada a amostra do trato respiratório inferior (secreções brônquicas colhidas por aspirado endotraqueal).4
Estimativas atuais, após várias revisões sistemáticas, apontam aproximadamente uma sensibilidade de 70% e uma especificidade de 95% para a RT-PCR. Neste contexto, um teste positivo tem maior peso do que um teste negativo, devido à sua alta especificidade. Um único teste negativo não deve ser usado como regra em doentes com sintomas sugestivos.2 Nos doentes com suspeita de COVID-19 e uma PCR inicial negativa, a repetição da RT-PCR revelou-se positiva em 23% dos casos. Nestas situações, sempre que possível, deve ser efetuada uma tomografia torácica.4 O padrão mais comum (76,4%) na tomografia torácica é a presença de opacidades em vidro despolido e infiltrados bilaterais.5
A infeção por SARS-CoV-2 também pode ser detetada indiretamente, medindo a resposta imunológica do hospedeiro. O diagnóstico serológico é especialmente importante nos casos leves a moderados com apresentação tardia, para além das duas primeiras semanas do início da doença. Pode ainda ter relevância na compreensão da disseminação da COVID-19 numa comunidade.
O marcador serológico mais sensível e mais precoce são os anticorpos totais, cujos níveis começam a aumentar a partir da segunda semana do início dos sintomas. Os testes aos anticorpos IgM e IgG por ELISA (enzyme-linked immunosorbent assay) têm mais de 95% de especificidade para o diagnóstico da COVID-19. A utilização conjunta da RT-PCR inicialmente, com os testes serológicos duas semanas depois, pode aumentar a precisão do diagnóstico.3 Apesar do enorme esforço para estudar as respostas imunológicas da COVID-19, até à data, ainda não há dados definitivos acerca da duração da presença dos anticorpos após infeções assintomáticas, leves e graves. Sublinha-se o perigo do uso destes testes para a avaliação do risco individual, mas destaca-se o seu potencial em termos epidemiológicos.6
Os testes rápidos utilizam um sistema qualitativo de deteção de IgG/IgM. Quando comparados com o teste RT-PCR (gold standard) apresentam baixa sensibilidade.
Neste contexto, são pouco úteis enquanto método de rastreio da comunidade tendo em conta o elevado número de falsos negativos.7
Conclusão
Este caso pretende ilustrar a complexidade do diagnóstico da COVID-19. Uma nova entidade que mantém a comunidade científica cheia de dúvidas e com muito poucas certezas. Diariamente vão surgindo novos estudos que mostram isso mesmo.
E a problemática vai para a além do diagnóstico, passando pela terapêutica de suporte, que tem levado à suspensão progressiva da hidroxicloroquina em vários países por questões de segurança, até à duração de imunidade dos indivíduos assintomáticos e sintomáticos, infetados pelo SARS-CoV-2, entre muitas outras.
O caminho releva-se longo e tortuoso, mas decerto sairemos dele mais enriquecidos em termos pessoais e profissionais, podendo contribuir para a história da humanidade.