Introdução
A síndrome das pernas inquietas (SPI) é uma doença do movimento que se caracteriza pela necessidade imperiosa de mover os membros, mais frequentemente os inferiores, ou outras partes do corpo, em resposta a disestesias. Normalmente apresenta agravamento durante a noite e em repouso e alívio momentâneo com o movimento.1)
Embora seja uma patologia subdiagnosticada, a literatura refere uma prevalência estimada de 5%-15%, com maior predomínio nos idosos e no sexo feminino.1-3
A fisiopatologia da SPI é ainda desconhecida, no entanto têm sido identificadas, nestes doentes, anomalias no sistema nervoso central (défice nas reservas de ferro e alteração no sistema dopaminérgico, no ritmo circadiano ou na função talâmica) e/ou periférico.4
Embora haja história familiar da doença em 40%-60% dos doentes com SPI, na maioria dos casos não é possível identificar um padrão genético característico. Nos doentes sem história familiar positiva, a SPI é classificada como primária (sem causa conhecida) ou secundária (se existirem comorbilidades que se associem a SPI). A SPI secundária pode ocorrer por anomalias na neutrotransmissão (diabetes, neuropatia periférica, doença de Parkinson) ou por alterações no metabolismo do ferro (gravidez, défice de ferro, insuficiência renal).5
O objetivo deste trabalho foi rever as manifestações clínicas, o diagnóstico, os fatores de agravamento e terapêutica desta síndrome.
Metodologia: Realizou-se, assim, uma revisão clássica da literatura com pesquisa de artigos de revisão nas principais bases de dados médicas (MEDLINE, Cochrane Library e National Institute for Health and Care Excellence (NICE) Evidence Search), utilizando o termo MeSH (Medical Subject Headings) “Restless Legs Syndrome”.
Resultados
Manifestações clínicas
O sintoma mais típico da SPI é uma necessidade imperiosa de movimento dos membros inferiores. Esta ocorre mais frequentemente nos períodos de inatividade, principalmente à noite, e alivia temporariamente com o movimento. Embora seja menos frequente, os membros superiores podem estar envolvidos, o que indica uma forma mais grave da doença. Raramente, as regiões perineal ou abdominal inferior também podem ser afetadas.6-7
Cerca de 80% dos casos de SPI estão associados a movimentos periódicos dos membros durante o sono, que tendem a ocorrer a cada 20-30 segundos, podendo causar insónia inicial, despertares noturnos, depressão, ansiedade e, consequentemente, diminuição do rendimento profissional e escolar e perda de qualidade de vida.
A SPI moderada ou de início precoce tende a remitir em 30%-60%.8-10 Os fatores que aumentam a probabilidade de se tornar persistente são a existência de história familiar e o diagnóstico em idade tardia.
Diagnóstico
O diagnóstico da SPI é clínico sendo necessário que os sintomas ocorram pelo menos 3 vezes por semana, durante um período de 3 ou mais meses, não sendo melhor explicados por outras patologias médicas ou psiquiátricas, ou pelo uso de fármacos ou substâncias psicoativas (Tabela 1).11
Tabela 1: Critérios de diagnóstico da síndrome das pernas inquietas segundo a quinta edição do Diagnostic and Statistical Manual of Mental Disorders (DSM-V).
Fatores de agravamento e abordagem terapêutica
A SPI apresenta, geralmente, uma boa resposta à terapêutica. A opção terapêutica depende de vários fatores como a gravidade da doença, a idade do doente, a existência de comorbilidades, os potenciais efeitos adversos e a preferência do doente. O objetivo da terapêutica é a redução ou eliminação dos sintomas da SPI com melhoria do sono e da qualidade de vida.
1. Correção da ferropénia
Uma vez que o défice de ferro está frequentemente associado à SPI, recomenda-se que a ferritina seja avaliada em todos os doentes com SPI antes de se iniciar terapêutica dirigida. Assim, para valores de ferritina iguais ou inferiores a 75 mcg/L (ou saturação da transferrina inferior a 20%) recomenda-se a administração de ferro. A via preferencial é a oral. A administração de ferro por via endovenosa, por ser menos cómoda e apresentar risco de anafilaxia, deve ser reservada para situações em que exista má absorção, intolerância ao ferro oral, persistência de sintomas mesmo após terapêutica com ferro oral ou necessidade de correção rápida devido à gravidade dos sintomas.12 A resposta à terapêutica oral é geralmente lenta, sendo necessários vários meses até ocorrer melhoria clínica. Por sua vez, a terapêutica endovenosa apresenta efeitos clínicos mais rápidos, podendo verificar-se melhoria sintomática após poucas semanas.13-14
Cerca de 3 meses após iniciar a terapêutica com ferro deve ser feito controlo analítico com hemograma e estudo do ferro. Caso não se obtenham os valores pretendidos, a avaliação analítica deve ser repetida a cada 3 a 6 meses até que a ferritina seja superior a 75 mcg/L e a saturação de transferrina seja superior a 20%.
Nos doentes em que não se verifique melhoria clínica, após normalização dos valores de ferro, deve ser considerada a realização de terapêutica dirigida para a SPI.
2. Terapêutica não farmacológica
A terapêutica não farmacológica deve ser aconselhada em todos os casos de SPI, podendo mesmo ser suficiente para a resolução dos sintomas em formas ligeiras a moderadas. As abordagens não farmacológicas incluem psicoeducação, a prática de exercício moderado, o alívio sintomático através de massagens ou aplicação de calor e evicção de terapêutica ou outros fatores de agravamento como o consumo de cafeína ou alguns fármacos.15-17 Existem vários fatores de agravamento da SPI que devem ser investigados, entre os quais se destaca a privação de sono, a síndrome de apneia obstrutiva do sono18 e a utilização de certos fármacos, nomeadamente os anti-histamínicos de primeira geração, os antagonistas dos recetores da dopamina (metoclopramida, clorpromazina) e antidepressivos (mirtazapina, antidepressivos tricíclicos, inibidores seletivos da recaptação da serotonina e inibidores da recaptação da serotonina-norepinefrina).19-20 Nos doentes a fazer antidepressivos das classes referidas, caso se considere pertinente um ajuste terapêutico, recomenda-se a troca para bupropiom, por ter menor probabilidade de agravar a SPI.21 Outra opção é manter a terapêutica antidepressiva e introduzir fármacos utilizados na terapêutica dirigida da SPI.
3. Terapêutica dirigida
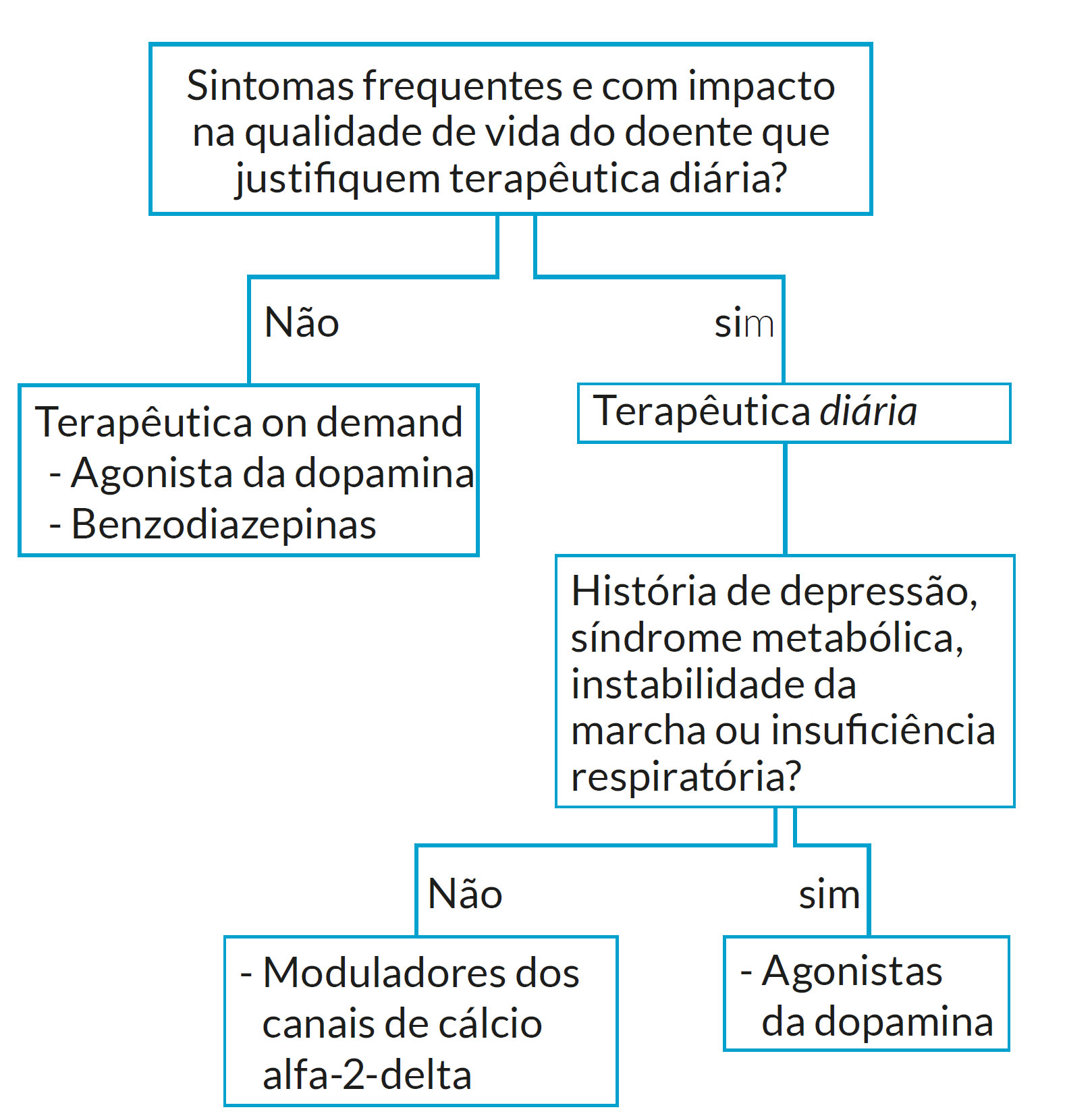
Quanto à terapêutica dirigida, deve optar-se por atuar de acordo com a gravidade da SPI.
SPI intermitente
A SPI intermitente caracteriza-se por sintomas pouco frequentes e imprevisíveis que não justificam uma terapêutica diária. No entanto, o facto de estes sintomas serem extremamente debilitantes e redutores de qualidade de vida, justificam a realização de terapêutica de forma pontual. O objetivo, neste caso, é uma terapêutica intermitente, principalmente se os sintomas surgem menos de uma a duas vezes por semana, ou preventiva, antes de condições previstas de imobilidade como procedimentos médicos ou viagens de carro ou avião.
Nesta síndrome intermitente usam-se frequentemente precursores da dopamina ou benzodiazepinas (Tabela 2).15 A escolha do fármaco deverá ter em conta o perfil de cada doente. O uso esporádico de levodopa é geralmente bem tolerado. Inclui efeitos adversos como náuseas, vertigens e sonolência que geralmente são moderados, mas que melhoram ao longo do tempo. (15,22 As benzodiazepinas também podem ser utilizadas nos casos moderados de SPI intermitente, sendo o clonazepam a benzodiazepina mais estudada para esta situação clínica.23-25
SPI crónica persistente
A SPI crónica persistente está associada a sintomas moderados a graves que ocorrem pelo menos duas vezes por semana, sendo necessária a realização de medicação diária.
A terapêutica de primeira linha são os moduladores dos canais de cálcio alfa-2-delta (gabapentina e pregabalina).(Tabela 3) 15 Estes fármacos apresentam alguns efeitos adversos, principalmente nos idosos, como vertigens, ganho de peso e edema dos membros inferiores. Estão ainda associados a aumento de risco de suicídio, pelo que os doentes medicados com estes fármacos deverão ser monitorizados ao longo do tempo.
Os agonistas da dopamina (rotigotina, pramipexol e ropinirol) são uma opção terapêutica de segunda linha devido ao possível efeito de aumentação. Este efeito secundário dos fármacos dopaminérgicos leva ao agravamento dos sintomas de SPI à medida que se aumentam as doses da medicação, com intensificação e aparecimento mais precoce dos sintomas (cerca de 2 horas antes do que era habitual), assim como extensão dos sintomas aos membros superiores ou outras partes do corpo.22) Isto implica que haja uma monitorização dos doentes medicados com estes fármacos a cada 6-12 meses para avaliar efeitos adversos ou complicações.15,23,24
Tabela 3: Terapêutica dirigida para a síndrome das pernas inquietas crónica persistente.
| Fármacos | Dose | Posologia | Efeitos adversos | |
|---|---|---|---|---|
| Moduladores dos canais de cálcio alfa-2-delta | Gabapentina enacarbil* | 600 mg | Dose única por volta das 17h | Sonolência e vertigem |
| Pregabalina | Iniciar com 50-75 mg e titular até 150-450 mg por dia | Sonolência, vertigem, fadiga, cefaleias, edemas periféricos e aumento de peso | ||
| Gabapentina | Iniciar com 100-300 mg e titular até 900-2400 mg por dia | Dose única 2h antes de deitar ou 1/3 da dose a meio do dia e 2/3 da dose ao deitar | Sonolência | |
| Agonistas de Dopamina | Pramipexole | 0,125 mg por dia Aumentar a cada 2-3 dias 0,125 mg (máximo 0,75 mg) até obter alívio sintomático | Dose única 2h antes do início dos sintomas de SPI | Náusea e fadiga |
| Ropinirol | 0,25 mg por dia Aumentar a cada 2-3 dias 0,25 mg (máximo 4 mg) até obter alívio sintomático | Dose única 2h antes do início dos sintomas de SPI | Náusea e fadiga | |
| Rotigotina | Iniciar com 1 mg até ao máximo de 3 mg | 1 penso transdérmico por dia | Reação na pele no local da colocação do penso transdérmico | |
*Terapêutica não disponível em Portugal
Contudo, em alguns casos, os agonistas da dopamina devem ser privilegiados em alguns doentes, nomeadamente quando existe história atual ou passada de perturbação depressiva moderada a grave, síndrome metabólico, patologia que induza instabilidade da marcha ou insuficiência respiratória (Tabela 4).15,23,24
Tabela 4: Seleção do grupo terapêutico na síndrome das pernas inquietas.
| Fatores que afetam a seleção da terapêutica | Terapêutica a escolher |
|---|---|
| Sintomas diurnos | Fármaco de longa ação |
| Insónia | Moduladores dos canais de cálcio alfa-2-delta |
| Gravidez | Evitar moduladores dos canais de cálcio alfa-2-delta e agonistas de dopamina; considerar uso de ferro |
| Risco aumentado de quedas | Agonistas de dopamina |
| Comorbilidade: Dor | Moduladores dos canais de cálcio alfa-2-delta |
| História de abuso de álcool ou substâncias | Moduladores dos canais de cálcio alfa-2-delta |
| História de perturbação de controlo de impulsos | Moduladores dos canais de cálcio alfa-2-delta |
| Sintomas severos de SPI | Agonistas de dopamina |
| Síndrome metabólico/Excesso de peso | Agonistas de dopamina |
| Menor custo do fármaco | Agonistas de dopamina |
| Comorbilidade: Depressão | Agonistas de dopamina |
| Comorbilidade: Ansiedade generalizada | Moduladores dos canais de cálcio alfa-2-delta |
SPI refratária
Na SPI refratária, na qual não há resposta ao uso de moduladores dos canais de cálcio alfa-2-delta nem de agonistas da dopamina,15 os opioides podem ser eficazes (Tabela 5). Embora se possam utilizar opioides mais fracos como o tramadol e a codeína, a maior parte destes doentes irão precisar de opioides mais potentes como a oxicodona e a metadona.26
Tabela 5: Terapêutica dirigida para a síndrome das pernas inquietas refratária.
| Fármacos | Dose | |
|---|---|---|
| Opioides de baixa potência | Codeína 30 mg | 60-180 mg |
| Tramadol 50 mg | 50-100 mg | |
| Tramadol 100 mg (libertação prolongada) | 100-200 mg | |
| Opioides de alta potência | Morfina 15 mg | 15-45 mg |
| Oxicodona 5 mg | 10-30 mg | |
| Hidrocodona* 10 mg | 20-45 mg | |
| Metadona 2,5 mg | 5-20 mg | |
*Terapêutica não disponível em Portugal
Os casos refratários devem ser referenciados para um especialista do sono.27
Algoritmo terapêutico da SPI
A síndrome das pernas inquietas é uma doença facilmente tratável e controlada, desde que se institua a terapêutica adequada ao doente. A seleção terapêutica deve seguir critérios que podem ser decididos de acordo com o algoritmo terapêutico da SPI (Tabela 6, Fig. 1).
Tabela 6: Algoritmo terapêutico na síndrome das pernas inquietas.
| Algoritmo terapêutico da SPI |
|---|
| 1. Instituir, em todos os doentes, medidas não farmacológicas que melhorem os sintomas |
| 2. Avaliar os níveis de ferritina em todos os doentes e iniciar suplementação com ferro oral ou endovenoso se indicado |
| 3. Realizar terapêutica dirigida consoante a gravidade das queixas |
Conclusão
A SPI é uma perturbação neuromotora com significativo impacto na qualidade de vida dos doentes, mas que se mantém infelizmente subdiagnosticada. Uma vez que o médico de família é frequentemente o primeiro contacto do doente é importante que esteja alerta para os sinais e sintomas que apontem para o diagnóstico desta patologia.
A ação do médico de família não se esgota no diagnóstico, sendo também essencial na introdução de uma terapêutica correta e no acompanhamento do doente. Tendo em conta a relação entre a SPI e alterações do padrão do sono, ansiedade e depressão, o acompanhamento destes doentes é de extrema importância. Salienta-se que melhorar e encorajar o apoio familiar promove melhor adesão aos planos de tratamento, cria um espaço terapêutico com comunicação e cooperação e permite ultrapassar os obstáculos e limites impostos pela nova doença diagnosticada.
Com este trabalho os autores pretendem alertar para esta patologia que, apesar do seu impacto negativo na qualidade de vida dos doentes, apresenta boa resposta à terapêutica, não devendo, por isso, ser uma entidade a descurar pelo médico de família.