Elevação das enzimas hepáticas, persistente e assintomática, como forma de apresentação da doença de Wilson em idade pediátrica
Persistently and asymptomatic raised liver enzymes as a form of presentation of Wilson's disease at pediatric age
Catarina MatosI; Sofia MartinsII; Idolinda QuintalIII; Lucília VieiraIII; Francisca CostaIV; Fernando PereiraI; Ermelinda Santos SilvaI
IS. Gastrenterologia Pediátrica, Departamento da Criança e do Adolescente, Centro Hospitalar do Porto. 4099-001 Porto, Portugal. E-mail: catarinamatos82@gmail.com; facpereira@sapo.pt; ermelinda.rss@gmail.com
IIS. Pediatria, Hospital de São Pedro Vila Real, Centro Hospitalar Trás-os-Montes e Alto Douro. 5000-508 Vila Real, Portugal. E-mail: sofia_moz@yahoo.com ]]>
IIIS. Pediatria, Hospital Padre Américo, Centro Hospitalar Tâmega e Sousa. 4564-007 Penafiel, Portugal. E-mail: ido@sapo.pt; luciliavieira2008@hotmail.com
IVS. Anatomia Patológica, Hospital de Santo António, Centro Hospitalar do Porto. 4099-001 Porto, Portugal. E-mail: kikareis_med@hotmail.com
RESUMO
Introdução: A doença de Wilson é uma doença rara, autossómica recessiva, caracterizada por uma alteração no transporte do cobre no fígado, com acumulação progressiva em vários órgãos (fígado, cérebro, rins e córneas). A expressão fenotípica é muito variável desde a elevação das enzimas hepáticas, esteatose ou litíase vesicular, em doentes assintomáticos, até à cirrose ou insuficiência hepática fulminante, ou doença neuropsiquiátrica incapacitante.
Objectivo: Caracterizar uma amostra de doentes com doença de Wilson.
Métodos: Estudo retrospectivo, incluindo as crianças diagnosticadas entre 2002 e 2011, segundo os critérios da European Association for the Study of the Liver (2012). Variáveis analisadas: antecedentes familiares; idade, dados clínicos, bioquímicos, imagiológicos e histológicos à data do diagnóstico; estudo genético; terapêutica e efeitos colaterais; seguimento e estado actual.
Resultados: Foram identificados cinco doentes, três com antecedentes familiares da doença. Todos se apresentavam assintomáticos e com elevação persistente das enzimas hepáticas. Em nenhum havia estigmas de doença hepática crónica. Uma doente tinha excesso de peso. Todos foram tratados com D-penicilamina, interrompida em dois por efeitos colaterais. Actualmente mantêm-se assintomáticos, sem evidência de progressão da doença hepática, com um seguimento mediano de 5 anos e 3 meses..
]]> Conclusões: A nossa série mostra que a doença de Wilson se pode apresentar com elevação das enzimas hepáticas em crianças assintomáticas. A doente com excesso de peso alerta-nos para a necessidade de rastrear a doença nos que têm excesso de peso/obesidade quando a elevação das enzimas hepáticas e/ou esteatose persistem por mais de seis meses após a perda de peso.Palavras-chave: doença de Wilson, D-penicilamina, elevação das enzimas hepáticas, esteatose hepática, idade pediátrica, metabolismo do cobre
ABSTRACT
Background: Wilson's disease is a rare autosomal recessive disorder characterized by a change in the transport of copper in the liver, with progressive accumulation in this and other organs such as brain, kidney and cornea. Phenotypic expression of the disease varies widely and can range from elevated liver enzymes, fatty liver or gallstones in asymptomatic patients, to cirrhosis and fulminant hepatic failure, or disabling neuropsychiatric disease.
Aim: To characterize a sample of patients with Wilson´s disease.
Patients and Methods: Retrospective survey including children diagnosed with Wilson´s disease between 2002 and 2011 according to the criteria of the European Association for the Study of the Liver (2012). We analyzed family history; age, clinical data, imaging and histology at the time of diagnosis; genetic analysis; treatment and side effects; follow-up and current status.
Results: We identified five patients. Three had a family history of disease. All were asymptomatic and had maintained raised liver enzymes. No patient had clinical stigmata of chronic liver disease. One female patient had overweight. All were treated with D-penicillamine, withdrawn in two patients because of side effects. Currently all patients remain asymptomatic, without evidence of progression of liver disease, with a median follow-up of 5 years and 3 months.
Discussion: Our series show that Wilson´s disease may be present with raised liver enzymes in asymptomatic children. The overweight patient alerts us to screen the disease in overweight/ obese patients with raised liver enzymes and/or steatosis persisting for more than six months after weight loss.
Keywords: Wilson´s disease, D-penicilamine, raised liver enzymes, fatty liver children, copper metabolism
]]>
INTRODUÇÃO
A doença de Wilson (DW) é uma doença metabólica rara (incidência 1/5000 a 1/30000), de transmissão autossómica recessiva, caracterizada por uma alteração no transporte do cobre a nível hepático.1 Foi descrita pela primeira vez em 1912, por Kinnear Wilson, como uma degeneração lenticular progressiva, letal e familiar, associada a doença hepática crónica com progressão para cirrose.
Em 1993 foi identificado o gene ATP7B, localizado no braço longo do cromossoma 13, que codifica uma ATPase tipo-P, expressa na região transmembranar dos hepatócitos, responsável pela excreção do cobre.2,3 Na DW, a ausência ou redução da função da ATPase leva à diminuição dos níveis séricos de cobre e de ceruloplasmina, ocorrendo uma acumulação hepática progressiva do cobre, e posterior deposição, via corrente sanguínea, noutros orgãos e tecidos como o cérebro, os rins e as córneas.2,3 A deposição de cobre no fígado provoca uma reacção inflamatória que progride, muitas vezes silenciosamente, para fibrose, cirrose, e insuficiência hepática.
A sintomatologia pode surgir em qualquer idade mas a maioria dos casos surge entre os cinco e os 35 anos. No entanto, já foi descrito o caso de uma criança de três anos com cirrose devido a DW.4 A suspeita clínica deve ser colocada perante qualquer criança com doença hepática (aguda ou crónica) inexplicada, associada ou não a doença neurológica ou psiquiátrica, anemia hemolítica, síndrome de Fanconi ou doença óssea.5-7
O diagnóstico deve ser baseado na integração de dados clínicos, bioquímicos, e estudo genético, uma vez que nenhum exame por si só o pode confirmar ou excluir.5-7 O diagnóstico pode ser particularmente difícil em alguns doentes, sobretudo naqueles em idade pediátrica.8
O tratamento consiste na administração de quelantes do cobre que permitem um aumento da sua excreção (Dpenicilamina ou trientina), e/ou sais de zinco (sulfato ou acetato) que actuam diminuindo a sua absorção, e numa dieta pobre em cobre, reduzindo a sua ingestão (evicção de alimentos como o chocolate, fígado, avelãs, marisco).7 Os doentes tratados com D-penicilamina devem ser suplementados em vitamina B6, dado que o quelante é um anti-metabolito desta vitamina1.
O prognóstico da DW depende da precocidade do diagnóstico e início do tratamento, bem como da resposta individual ao mesmo. A instituíção precoce de terapêutica nos indivíduos assintomáticos previne a expressão clínica da doença.8,9
Descrevemos uma série de cinco casos de DW diagnosticados em idade pediátrica.
]]> MÉTODOS
Análise retrospectiva, transversal e descritiva de cinco doentes (entre os nove e os doze anos de idade, três do sexo masculino (M) e dois do sexo feminino (F) com doença de Wilson.
O diagnóstico foi efectuado entre 2002 e 2011, e foram aplicados os critérios da European Association for the Study of the Liver (EASL) de 2012.7 Foram analisadas e comparadas as seguintes variáveis: antecedentes familiares de DW; idade, dados clínicos, bioquímicos, imagiológicos, e histológicos no momento do diagnóstico; estudo genético; terapêutica e efeitos colaterais; seguimento e evolução.
RESULTADOS
Caso 1 Doente de sexo feminino, admitida aos dez anos de idade por enzimas hepáticas persistentemente elevadas, com um ano de evolução, observadas em análises efetuadas por queixas de náuseas e dores abdominais difusas (Quadro 1). O diagnóstico de DW foi efectuado por critérios bioquímicos e a histologia hepática mostrou lesões de esteatohepatite (Quadro 2). A doente foi inicial- mente tratada com dieta pobre em cobre, D-penicilamina e vitamina B6. Seis meses depois as enzimas hepáticas normalizaram, e a ecografia revelava a presença de fígado de dimensões e ecoestrutura normais. Esta doente tem 12 anos de seguimento, e a sua evolução foi marcada pela necessidade de mudanças terapêuticas, condicionadas
pela ocorrência de efeitos colaterais e/ou má adesão (Quadro 3). Sob Dpenicilamina teve hematúria microscópica e proteinúria. Com o sulfato de zinco, observou-se a normalização do sedimento urinário, mas viria a experimen- tar dispepsia, que predispunha à má adesão terapêutica.
Com o acetato de zinco não houve melhoria significativa das queixas dispépticas. Cinco anos após o diagnóstico, as transaminases voltaram a subir (cerca de 2x/N), e a ecografia sugeria novamente a presença de esteatose. Nesta altura registava-se um excesso de peso (índice de massa corporal no P85-90). Foi decidido suspender os sais de zinco e reiniciar a D-penicilamina. Desta vez não ocorreram efeitos colaterais e a resposta terapêutica voltou a ser favorável, com normalização das transaminases e resolução da esteatose. Actualmente mantém-se assintomática, com enzimas hepáticas normais, e fígado com dimensões e ecoestrutura normais. Medicação actual: Dpenicilamina 300 mg 1x/dia.
Caso 2 Sexo masculino, admitido aos nove anos de idade, assintomático. O rastreio analítico efectuado após ter sido diagnosticada doença de Wilson ao irmão de 16 anos (apresentação neuropsiquiátrica) revelou enzimas hepáticas elevadas (Quadro 1). O diagnóstico de DW foi efectuado por critérios bioquímicos (Quadro 2), e confirmado posteriormente por estudo molecular, que mostrou uma mutação em dupla heterozigotia no gene ATP7B [alelo1: mutação c.2795C>A (p.Ser932X) exão 12; alelo2: mutação c.3694A>C (p.Thr1232Pro) exão 17].
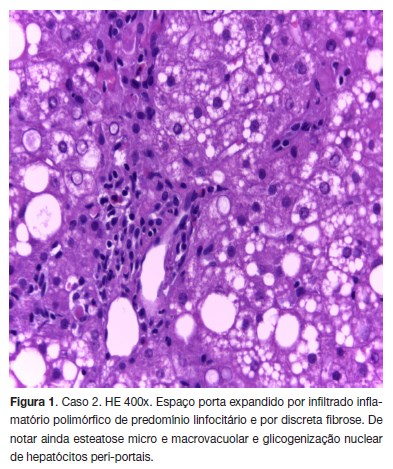
A histologia hepática evidenciou a presença de esteatohepatite (Figura 1). Foi iniciada dieta pobre em cobre, e terapêutica com D-penicilamina e vitamina B6. Uma semana após o início do tratamento observou-se uma reacção de hipersensibilidade à Dpenicilamina, com febre, exantema maculopapular, tosse e pieira, que reverteu após suspensão da terapêutica (Quadro 3). Iniciou terapêutica alternativa com trientina e sulfato de zinco, com boa tolerância. Observou-se uma diminuição progressiva das enzimas hepáticas, sem se atingir a normalização completa. A histologia hepática três anos após o início do tratamento não revelou progressão da doença, e o cobre hepático tinha diminuído, embora de forma não inteiramente satisfatória, tendo-se aumentado a dose do quelante (Quadro 3). Após 5 anos e 8 meses de seguimento, mantém-se assintomático, com enzimas hepáticas ainda ligeiramente elevadas. Além dos exames neurológico e oftalmológico, a ressonância magnética cerebral também foi normal neste doente. Medicação actual: trientina 600 mg 2x/dia.
]]>

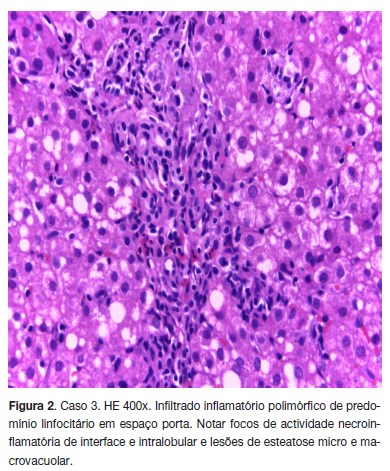
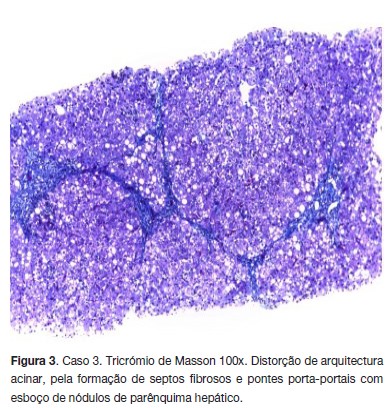
Casos 3 e 4 Irmãos gémeos monozigóticos, do sexo masculino, filhos de pais consanguíneos, admitidos aos sete anos de idade, assintomáticos. Observada elevação das enzimas hepáticas em análises de rotina. Havia referência a DW em um primo em 3ºgrau (Quadro 1). O diagnóstico de DW foi efectuado por critérios bioquímicos (Quadro 2) e posteriormente confirmado por estudo molecular que revelou em ambos a presença de uma mutação em homozigotia no gene ATP7B [alelos 1 e 2: mutação c.2123T>C (p.Leu708Pro) exão 8]. Nos dois irmãos a alfa1-antitripsina sérica estava diminuída, e o fenótipo era SZ. A histologia hepática, idêntica nos dois irmãos, revelou esteatohepatite, fibrose portal importante com formação de septos e pontes e esboço de nódulos, e ausência de grânulos alfa-1-antitripsina (Figuras 2 e 3). Foi iniciada dieta pobre em cobre e terapêutica com D-penicilamina, e vitamina B6, com boa resposta. Foram medicados também com ácido ursodesoxicólico 20 mg/kg/dia, em 2 tomas. Foi registada uma reacção urticariforme ligeira (exantema maculopapular prurigi- noso), transitória, num dos irmãos, 22 dias após o início da terapêutica com D-penicilamina (Quadro 3). Observou-se uma diminuição progressiva das enzimas hepáticas (1,5-2x/N), mas sem se atingir a normalização completa. A histologia hepática, cerca de 2,5 anos após o início do tratamento, não revelou progressão da doença, e o cobre hepático tinha diminuído de forma significativa. A partir de Julho 2013 foi suspenso o ácido ursodesoxicólico. Actualmente, após 5 anos e 3 meses de follow-up, encontram-se assintomáticos, com elevação ligeira/ moderada (cerca de 2-3xN) das enzimas hepáticas. Medicação actual: Dpenicilamina 500 mg 2x/dia.
]]>
Caso 5 Doente de sexo feminino, admitida aos 11 anos de idade, com hipertransaminasemia e hepatomegalia ligeira com esteatose, observadas em estudo analítico e ecográ- fico realizado na altura do diagnóstico de apendicite aguda (Quadro 1). Nesta altura apresentava excesso de peso (IMC no percentil 90) tendo iniciado regime dietético e exercício físico para perder peso. Seis meses após ter atingido o peso adequado (IMC no percentil 75) mantinha transaminases elevadas pelo que se prosseguiu a investigação. O diagnóstico de DW foi efectuado por critérios bioquímicos (Quadro 2), e posteriormente confirmado por estudo molecular que evidenciou uma mutação em dupla heterozigotia do gene ATP7B [alelo1: mutação c.1285+5G>T intrão2; alelo2: mutação c.2123T>C (p.Leu708Pro) Exão 8]. A histologia hepática mostrou aspectos sugestivos de esteatohepatite (Quadro 2). Foi iniciada dieta pobre em cobre, e terapêutica com D-penicilamina e vitamina B6, com boa resposta e sem efeitos colaterais. Observou-se progressiva redução dos valores das transaminases e depleção do cobre sistémico. Foi efectuado rastreio da doença de Wilson ao irmão, de cinco anos de idade, por estudo molecular, revelando-se portador de uma mutação em heterozigotia no gene ATP7B [alelo1: sem mutações; alelo2: mutação c.1285+5G>T intrão2] (Quadro 3). Após 3 anos e 9 meses de seguimento, encontra-se assintomática e com enzimas hepáticas normais. Medicação atual: D-penicilamina 150 mg 1x/dia.
DISCUSSÃO
O diagnóstico precoce da DW e o seu tratamento em fase pré-sintomática aumentam as expectativas de impedir a progressão para lesões graves nos órgãos-alvo.
A DW deve ser rastreada em qualquer criança com idade superior a 3 anos que apresente: 1) alterações hepáticas de etiologia desconhecida associadas ou não a patologia neurológica e/ou psiquiátrica; 2) esteatose ou esteatohepatite não alcoólica (Non-Alcoolic Steato-Hepatitis, NASH); 3) quadro clínico de hepatite auto-imune; 4) insuficiência hepática associada a hemólise intravascular Coombs negativa, elevação ligeira das transaminases ou fosfatase alcalina sérica baixa, e relação fosfatase alcalina/bilirrubina < 2; ou 5) seja familiar em 1ºgrau de um doente com DW. No entanto, a idade por si só não deve servir de base para eliminar um diagnóstico de DW.6,7
Na nossa série, o caso 2 foi diagnosticado após rastreio familiar, dado que tinha um irmão falecido aos 16 anos com DW de apresentação neuropsiquiátrica. No caso 5, a doente com excesso de peso, foi estudada por ter uma NASH que não regrediu após redução do índice de massa corporal para o p75. A NASH é actualmente a causa mais frequente de transaminases elevadas em idade pediátrica nos países ocidentais.10,11 No entanto, numa criança com excesso de peso ou obesidade que apresente elevação das enzimas hepáticas e/ou esteatose que persistem por mais de seis meses após a perda de peso, torna-se necessário rastrear outra doença subjacente, incluindo a DW. Os outros três doentes foram investigados após constatação ocasional de enzimas hepáticas elevadas, que persistiram por mais de seis meses.10-13
O diagnóstico de DW pode revelar-se particularmente difícil, sobretudo em doentes em idade pediátrica.8 Nenhum exame de per si confirma ou exclui o diagnóstico. Por este motivo, ao longo dos anos, os peritos foram elaborando recomendações com o objectivo de facilitar o diagnóstico, destacando-se as recomendações da American Association for the Study of Liver Diseases (AASLD) e da European Association for the Study of the Liver (EASL).5-7
]]> As primeiras recomendações da AASLD5 revelaram limitações na sua aplicabilidade à população pediátrica, na qual raramente estão presentes manifestações típicas da doença como os anéis de KF. Por outro lado, do ponto de vista bioquímico, muitos doentes pediátricos (com doença hepática sem envolvimento neurológico) apresentam excreção do cobre urinário de 24h e após teste com D-penicilamina e cobre hepático inferiores aos critérios referidos nestas recomendações. Além disto, estes critérios não incluíam a análise genética.As recomendações mais recentes da AASLD e da EASL consideram valores inferiores para a excreção do cobre urinário de 24h (basal > 40 µg, após teste de D-penicilamina > 1000 µg), e para o cobre hepático (> 50 µg/g tecido hepático), e incluem a análise genética, aumentando assim a sensibilidade e a especificidade para o diagnóstico de DW na idade pediátrica.6,7,14,15 As recomendações da EASL adoptam a utilização de um score baseado numa combinação de aspectos clínicos, bioquímicos, e genéticos, proposto pelo Grupo de Trabalho da 8ª Reunião Internacional sobre Doença de Wilson de Leipzig 2001, e baseado neste score é proposto um algoritmo de diagnóstico.
Os cinco doentes desta série apresentavam critérios de diagnóstico segundo as recomendações da AASLD e da EASL.5-7 Em nenhum dos nossos doentes foi observado atingimento neurológico ou anéis de Kaiser-Fleischer (KF), o que não surpreende dada a idade dos doentes à data do diagnóstico. Todos apresentavam ceruloplasmina sérica <10 mg/dl, mas no caso 2 a excreção urinária de cobre nas 24h (basal) era inferior ao considerado nas recomendações da AASLD, e o caso 5 encontrava-se no limite do considerado nas recomendações da EASL.6,7 No entanto em ambos o valor do cobre hepático permitiu confirmar o diagnóstico. Nos 4 doentes em que a análise genética foi efectuada foi possível identificar mutações em ambos os alelos, exame que teria sido decisivo para o diagnóstico caso os testes bioquímicos tivessem sido equívocos.
Na admissão as transaminases estavam elevadas em todos os doentes, sendo esta uma forma comum de apresentação da DW na idade pediátrica, mas nenhum dos doentes apresentava estigmas clínicos de doença hepática crónica.13,14 No entanto, nos casos 3 e 4 a histologia hepática mostrava já a presença de fibrose portal importante com formação de septos, pontes e esboço de nódulos. Sendo estes doentes também portadores de défice de alfa-1-antitripsina (fenótipo SZ), é impossível determinar se a extensão da doença hepática se deve exclusivamente à doença de Wilson, ou se existe uma sobreposição de morbilidades, eventualmente com potenciação mútua. A prescrição de ácido ursodesoxicólico a estes dois doentes foi uma tentativa de intervenção sobre as eventuais lesões provocadas pelo défice de -1-antitripsina.16
A D-penicilamina, outrora a única opção para o tratamento da doença de Wilson, é bastante dispendiosa e tóxica (reacções de hipersensibilidade, deficiência de zinco, anemia aplástica ou nefrose em 10-20% dos casos), e muitas vezes nos doentes com manifestações neurológicas provoca uma deterioração da sua situação clínica. Outros quelantes do cobre, como a trientina, são menos potentes, mas podem ser melhor tolerados. Alguns autores demonstraram que mesmo os casos de doença hepática crónica severamente descompensada podem ser tratados com quelantes.17
Entretanto, os sais de zinco (sulfato e acetato), surgiram como alternativa terapêutica eficaz, segura e económica, e podem ser uma opção para a 1ª linha de tratamento dos doentes pré-sintomáticos, e para os doentes com sintomas neurológicos.6,7 No que diz respeito aos doentes sintomáticos, embora alguns autores assegurem que os sais de zinco são tão eficazes como os quelantes do cobre, outros afirmam o contrário, sobretudo no que diz respeito aos doentes com manifestações hepáticas.18-20 Por outro lado, a ideia inicial de que os sais de zinco eram muito seguros e bem tolerados tem vindo a desvanecer-se, já que têm sido reportados vários efeitos colaterais, com destaque para os sintomas gastrointestinais (até 40% dos doentes), que podem favorecer a má adesão ou mesmo o abandono do tratamento, com a consequente ineficácia do mesmo.21 Em qualquer caso, se os sais de zinco forem a opção terapêutica está recomendado efectuar uma monitorização cuidadosa das transaminases, e se estas aumentarem dever-se-á passar para um quelante.7
Todos os doentes da nossa série foram medicados inicialmente com D-penicilamina, interrompida em dois (~40%) por efeitos colaterais: um caso por reacção de hipersensibilidade, outro por hematúria microscópica associada a proteinúria. No primeiro a terapêutica foi substituída por trientina e sulfato de zinco, com boa tolerância e eficácia. No segundo foi substituída por sais de zinco, mas registaram-se efeitos colaterais gastrointestinais (dispepsia) condicionando uma má adesão, e ausência de eficácia terapêutica, tendo sido retomada a D-penicilamina, sem novas intercorrências. Os efeitos colaterais da D-penicilamina podem fazer ponderar a escolha da trientina como fármaco de 1ª linha. No entanto, a trientina tem acção quelante menos potente, também não é isenta de efeitos colaterais, e por vezes existe alguma dificuldade de acesso ao fármaco.
Após um período de seguimento mediano de 5 anos e 3 meses (de 3 anos e 9 meses a 12 anos) não houve progressão clínica da doença em nenhum doente. Também não houve progressão histológica nos três doentes que repetiram a biópsia hepática. Nestes a biópsia foi repetida para avaliar o cobre hepático, por não ter ainda ocorrido a normalização completa das enzimas hepáticas após mais de 2 anos de terapêutica que- lante, em doses consideradas adequadas e aparentemente com bom cumprimento (nos casos 3 e 4 observou-se uma diminuição significativa do cobre hepático, mas no caso do doente sob trientina a diminuição foi proporcionalmente bastante menor, tendo-lhe sido aumentada a dose do quelante).
Estes resultados reflectem os benefícios da precocidade do diagnóstico e do início da terapêutica nestas crianças, afectadas por uma patologia rara, mas que tem tratamento seguro e eficaz, e que quando iniciado em fase pré-sintomática pode prevenir a progressão para doença hepática terminal com necessidade de transplante hepático, bem como o aparecimento de manifestações neurológicas irreversíveis.
Em nossa opinião, tendo em consideração a evolução silenciosa da doença e a escassez de sinais clínicos até fases muito avançadas da mesma, pode justificar-se a realização de um doseamento de transaminases a todas as crianças, pelos 10 anos de idade, altura em que alguns autores recomendam o rastreio universal das dislipidemias.22 Os custos associados a um doseamento de transaminases serão previsivelmente baixos quando comparados com os custos do diagnóstico e tratamento da DW em estadios mais avançados.
]]>REFERÊNCIAS BIBLIOGRÁFICAS
1. Scheinberg IH, Sternlieb I. Wilsons disease. In: Smith Jr LH, editor. Major problems in internal medicine, vol. 23. Philadelphia, PA: WB Saunders;1984. p. 25-35. [ Links ]
2. Tao TY, Gitlin JD. Hepatic copper metabolism: insights from genetic disease. Hepatology 2003;37:1241-7. [ Links ]
3. Lutsenko S, Petris MJ. Function and regulation of the mammalian coppertransporting ATPases: insights from biochemical and cell biological approaches. J Membr Biol 2003;191:1-12. [ Links ]
4. Wilson DC, Phillips MJ, Cox DW, Roberts EA. Severe hepatic Wilsons disease in preschool-aged children. J Pediatr 2000;137:719-22. [ Links ]
]]>5. Roberts EA, Schilsky ML. A practice guideline on Wilson disease. Hepatology 2003;37:1475-92. [ Links ]
6. Roberts EA, Schilsky ML. Diagnosis and Treatment of Wilson Disease: An Update. Hepatology 2008; 47 (6): 2090-105. [ Links ]
7. Ferenci P, Czlonkowska A, Stremmel W, Houwen R, Rosenberg W, Schilsky M, et al. European Association for the Study of the Liver. EASL Clinical Practice Guidelines: Wilsons disease. Journal of Hepatology 2012; 56: 671-85. [ Links ]
8. Sánchez-Albisua I, Garde T, Hierro L, Camarena C, Frauca E, de la Vega A, Díaz MC, Larrauri J, Jara P. A high index of suspicion: the key to an early diagnosis of Wilsons disease in childhood. J Pediatr Gastroenterol Nutr. 1999; 28 (2): 186-90. [ Links ]
9. Benhamla T, Tirouche YD, Abaoub-Germain A, Theodore F. The onset of psychiatric disorders and Wilsons disease. Encephale. 2007; 33 (6): 924-32. [ Links ]
]]>10. Nanda K. Non-alcoholic steatohepatitis in children. Pediatr Transplant. 2004;8 (6): 613-8. [ Links ]
11. Bramlage KS, Bansal V, Xanthakos SA, Kohli R. Fatty Liver Disease in Children-What Should One Do? Indian J Pediatr. 2012. [ Links ]
12. Pena-Quintana L, García-Luzardo M, García-Villarreal L, Arias-Santos M et al. Manifestations and Evolution of Wilson Disease in Pediatric Patients Carrying ATP7B Mutation L708P. JPGN 2012; 54 (1):48-54. [ Links ]
13. Iorio R, DAmbrosi M, Marcellini M, Barbera C, Maggiore G et al. Serum Transaminases in Children with Wilsons Disease. J Pediatr Gastroenterol Nutr. 2004; 39 (4): 331-6. [ Links ]
14. Manolaki N, Nikolopoulou G, Daikos GL, Panagiotakaki E, Tzetis M. Wilson disease in children: analysis of 57 cases. J Pediatr Gastroenterol Nutr. 2009; 48(1): 72-7. [ Links ]
]]>15. Koppikar S, Dhawan A. Evaluation of the scoring system for the diagnosis of Wilsons disease in children. Liver Int 2005;25:680-1. [ Links ]
16. Lykavieris P, Ducot B, Lachaux A, Dabadie A, Broue P, Sarles J,et al. Liver disease associated with ZZ a1-antitrypsin deficiency and ursodeoxycholic acid therapy in children. J Pediatr Gastroenterol Nutr 2008; 47 (5): 623-9. [ Links ]
17. Santos Silva E, Sarles J, Buts JP, Sokal EM. Successful medical treatment of severely decompensated Wilson disease. J Pediatr. 1996; 128:285-7. [ Links ]
18. Członkowska A, Litwin T, Karliński M, Dziezyc K, Chabik G, Czerska M.D-penicillamine versus zinc sulfate as first-line therapy for Wilson's disease. Eur J Neurol. 2014 Jan 21. doi: 10.1111/ene.12348. [Epub ahead of print]. [ Links ]
19. S, Taly AB. Withdrawal of penicillamine from zinc sulphate- penicillamine maintenance therapy in Wilson's disease: promising, safe and cheap. J Neurological Sciences 2008; 264 (1): 129-32. [ Links ]
]]>20. Weiss KH, Gotthardt DN, Klemm D, Merle U, FerenciFoerster D, Schaefer M, et al. Zinc monotherapy is not as effective as chelating agents in treatment of Wilson disease. Gastroenterology. 2011 Apr;140(4):1189-1198.e1. doi:10.1053/j.gastro.2010.12.034. Epub2010 Dec 24. [ Links ]
21. Wiernicka A, Jańczyk W, Dądalski M, Avsar Y, Schmidt H, Socha P. Gastrointestinal side effects in children with Wilson's disease treated with zinc sulphate. World J Gastroenterol 2013; 19(27): 4356-62. [ Links ]
22. Ritchie SK, Murphy E, Ice C, Cottrell LA, Minor V, Elliot E, et al. Universal Versus Targeted Blood Cholesterol Screening Among Youth: The CARDIAC Project. Pediatrics 2010; 126 (2): 260-5. [ Links ]
Endereço para correspondência
Ermelinda Santos Silva
S. Gastrenterologia Pediátrica, ]]>
Departamento da Criança e do Adolescente,
Centro Hospitalar do Porto
Largo Prof. Abel Salazar,
4099-001 Porto.
e-mail: ermelinda.dca@chporto.min-saude.pt
telefone: 222 077 500
Recebido a 24.03.2014 | Aceite a 10.12.2014
]]>