Teresa Moreira*, Jorge Areias*
INTRODUÇÃO
A hepatite B crónica constitui um importante problema de saúde pública a nível mundial. Estima-se que existam cerca de 2 mil milhões de infectados pelo vírus da hepatite B (VHB) e cerca de 400 milhões de pessoas com hepatite B crónica em todo o mundo.
Cerca de 15-40% dos portadores do vírus irão desenvolver complicações graves ao longo da vida. Este vírus é responsável por 0,5-1,2 milhões de mortes por cirrose hepática e hepatocarcinoma, anualmente.
A prevalência do AgHBs varia muito a nível geográfico e os países podem ser definidos como tendo prevalência elevada (≥ 8%),
]]> intermédia (2-7%) ou baixa (<2%). Nos países desenvolvidos a prevalência é mais elevada entre os imigrantes de países de prevalência elevada ou intermédia e naqueles com factores de risco. A história natural da hepatite B crónica é complexa e causa um espectro clínico da doença variado.O risco de desenvolver infecção crónica pelo VHB após a exposição aguda varia de cerca de 90% nos recém-nascidos de mães AgHBe +, a 25-30% em crianças de idades < 5 anos até < 5% em adultos. O risco é também superior em indivíduos imunocomprometidos.
DEFINIÇÕES
Hepatite crónica B
Doença necro-inflamatória do fígado, causada pela infecção persistente com o VHB. Pode ser dividida em AgHBe (+) ou AgHBe (-)
1. AgHBs (+) > 6 meses
2. DNA VHB > 20.000 IU/L (105 cópias/ml)
Valores entre 2.000 e 20.000 IU/L (104-105 cópias/ml) são habitualmente observados na hepatite crónica B AgHBe (-)
3. Elevação persistente ou intermitente da ALT/AST
]]> 4. Histologia: hepatite crónica com infiltrado necroinflamatório moderado a severo (score necroinflamatório ≥ 4)
Estado de portador inactivo
Infecção persistente do fígado pelo VHB, sem doença necroinflamatória significativa.
1. AgHBs (+) 6 meses
2. AgHBe (-), Anti-HBe (+)
3. DNA VHB 2.000 IU/L (104/cópias/ml) < 20.000 IU/L (105 cópias/ml) segundo alguns autores
4. ALT/AST persistentemente normal (implica um seguimento longitudinal)
5. Histologia confirma a ausência de hepatite significativa (score necroinflamatório < 4)
]]> Hepatite B resolvida
Infecção pelo VHB passada, sem evidência de infecção activa virulógica, bioquímica ou histológica ou doença.
1. História prévia conhecida de hepatite B aguda ou crónica, ou a presença de anti-HBc +/- anti-HBs
2. AgHBs (-)
3. Níveis de DNA VHB indetectáveis
4. ALT normal
Definições e termos utilizados
- Exacerbação aguda ou flare de hepatite B
- Reactivação
]]> - Eliminação AgHBe- Seroconversão AgHBe
- Reversão AgHBe
HISTÓRIA NATURAL
O início da hepatite B crónica é marcado pela persistência do AgHBs, níveis elevados de virémia e presença de AgHBe. Na infecção adquirida na fase perinatal, os doentes tendem a apresentar níveis normais de transaminases, com DNA do VHB elevado e persistência de AgHBe (fase imunotolerante). Embora a biopsia hepática não seja habitualmente realizada nesta fase, existem estudos que demonstram actividade inflamatória ou fibrose mínimas ou inexistentes. Na infecção adquirida na vida adulta, a fase inicial da infecção acompanha-se por marcada actividade da doença, com transaminases elevadas, numa tentativa de clearence dos hepatócitos infectados (fase imunoactiva). A histologia demonstra marcada actividade necroinflamatória, com graus variados de fibrose. Durante esta fase pode ocorrer a seroconversão AgHBe (perda do AgHBe e aquisição do anticorpo anti-HBe) que ocorre a uma taxa de 8-12% ao ano; acompanha-se normalmente de uma queda do DNA VHB para níveis inferiores a 20.000U/l, e representa a transição para fase de portador inactivo (fase de imuno-control). Alguns doentes também perdem o AgHBs, tratando-se de uma resolução espontânea da hepatite crónica B. A perda do AgHBs ocorre espontaneamente a uma taxa de 0,5%/ano.

Alguns doentes nos quais ocorre seroconversão AgHBe apresentam novamente níveis elevados de DNA do VHB e transaminases elevadas. Estes doentes apresentam uma forma mutante do VHB, com mutação nas regiões do precore ou promotor do core, que impede ou down-regulates a produção de AgHBe (fase de imuno-escape). Esta forma de hepatite é chamada de hepatite crónica B AgHBe negativo e cursa com níveis de DNA mais baixos que a Hepatite B AgHBe (+). Estes doentes são habitualmente mais velhos e apresentam doença hepática mais avançada, uma vez que a Hepatite B AgHBe (-) representa uma fase mais tardia da infecção. A distinção entre o estado de portador inactivo e hepatite crónicaB AgHBe (-) requer um seguimento/avaliação longitudinal, devido à flutuação dos valores de transaminases e DNA.
]]>OBJECTIVOS DO TRATAMENTO
Objectivos a longo prazo:
1. Prevenir e atrasar o desenvolvimento de complicações: cirrose e hepatocarcinoma.
Objectivos imediatos:
1. Supressão vírica (DNA VHB < 2.000 IU/L)
2. Normalização da ALT
3. Melhoria histológica
4. Seroconversão AgHBe (apenas na Hepatite cónica B AgHBe+)
]]> 5. Perda do AgHBs
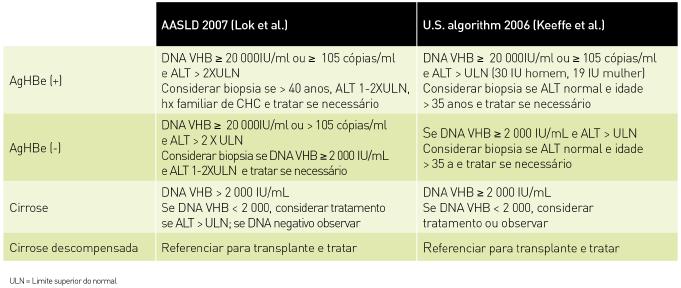
INDICAÇÕES PARA O TRATAMENTO
É importante definir o ponto da história natural em que cada doente se encontra. Esta categorização é feita com base: presença ou ausência de AgHBe, replicação vírica (DNA VHB), valor de ALT e histologia hepática. Esta avaliação permite definir o perfil de cada doente de forma a determinar a melhor estratégia de tratamento.
Caracterização da Doença
AgHBe positivo ou negativo
Replicação vírica (DNA VHB)
ALT elevada ou normal
Histologia hepática (fibrose)
]]>FÁRMACOS DISPONÍVEIS
Peginterferão alfa-2a (Pegasys) - 180 mcg/semana 48 semanas
Vantagens
- Duração de tratamento definida (48 semanas)
- Taxa de resposta sustentada elevada
- Elevada taxa de seroconversão HBe 27%
- Elevada taxa de supressão DNA VHB 25%
- Elevada taxa de seroconversão HBs
- Ausência de resistências
]]> Desvantagens
- Via de administração: injectável
- Efeitos laterais frequentes
- Contra-indicado na cirrose descompensada
- Custo
Peg IFN - O doente ideal
Idade jovem
ALT elevada (> 5 x ULN)
]]> DNA VHB baixo (< 200,000 IU/mL) Raça negra
Sem contra-indicações para o seu uso
Genotipo A (melhor que D) ou B (melhor que C)?
Análogos dos núcleos(t)ideos:
1. Lamivudina (Epivir-HBV®): 100 mg/dia, via oral (aprovado pela FDA em 1998)
Vantagens
- Bem tolerada; via de administração oral
- Excelente perfil de segurança
]]> - Baixo custo
Desvantagens
- Elevada taxa de resistências (YMDD) e resistências cruzadas com outros análogos nucleosídeos.
- Taxas modestas de seroconversão AgHBe: ~ 20% no 1º ano, que aumenta com a duração do tratamento
- Seroconversão AgHBs rara
Quando usar a Lamivudina?
Não deverá ser de 1ª linha
Tratamentos de curta duração (p.ex. prevenção de reactivação durante QT, Imunossupressão).
]]> Segurança: Durante a gravidez. Custo: Hepatite Crónica B nos países em desenvolvimento ou sub-desenvolvidos.
2. Adefovir dipivoxil (Hepsera®): 10 mg/dia, via oral (aprovado pela FDA em 2002)
Vantagens
- Bem tolerado; via de administração oral
- Baixa incidência de resistências, especialmente nos 1º e 2º anos
- Eficaz contra VHB resistente à lamivudina
Desvantagens
]]> - Reposta lenta e taxa elevada de não-respondedores- Taxas de seroconversão de AgHBe modestas: ~ 12% no 1º ano, que aumenta com a duração do tratamento
- Seroconversão AgHBs rara
- Potencial de toxicidade renal? (ajuste de dose se TFG<50 ml/min).
- Custo superior ao tenofovir
3. Entecavir (ETC) (Baraclude®): 0.5 mg/dia (doentes naive); 1.0 mg/dia (doentes resistentes à lamivudina), via oral
(aprovado pela FDA em 2005)
Vantagens
- Bem tolerado; via de administração oral
]]> - Elevada potência anti-vírica- Baixa incidência de resistências em doentes naive (1% aos 5 anos)
- Eficaz no VHB resistente à lamivudina, mas necessárias doses superiores e elevado risco de resistências (51% aos 5 anos)
- Excelente fármaco de primeira linha
Desvantagens
- Taxas de seroconversão AgHBe modestas (21% a 1 ano, mas aumenta com a duração do tratamento)
- Seroconversão AgHBs rara
- Dados sobre eficácia e segurança a longo prazo ainda escassos
]]> 4. Tenofovir (TDF) (Viread®): 300 mg/dia, via oral (aprovado pela FDA em 2008)
Recentemente aprovado para o tratamento da Hepatite crónica B, é um fármaco estruturalmente relacionado com o adefovir, mas com potência anti-vírica muito superior (supressão vírica DNA < 400 cópias/mL: 76% vs 13%). Bem tolerado. Sem evidência de toxicidade renal significativa. Sem resistências conhecidas até à data (0%). Por estes motivos, constitui um excelente fármaco de primeira linha. Ausência de dados sobre segurança e tolerabilidade a longo prazo.
5. Telbivudina (LdT) (Tyzeka®, Sebivo®): 600 mg/dia, via oral (aprovado pela FDA em 2006) L-Nucleosídeo, com potente actividade anti-vírica, mais potente que a lamivudina na supressão da replicação do VHB. Contudo está associada a elevada taxa de resistências (até cerca de 25% aos 2 anos), com resistências cruzadas com a lamivudina (YMDD). Bem tolerada, com perfil de segurança sobreponível ao da lamivudina. Ainda não disponível para uso no nosso país.
DURAÇÃO DO TRATAMENTO COM OS ANÁLOGOS?
Hepatite B AgHBe (+)
- Tratar até à seroconversão AgHBe + 6 meses após (tratamento de consolidação)
- Monitorizar após a suspensão do tratamento (risco de recidiva)
Hepatite B AgHBe (-)
]]> - Tipicamente necessitam de terapêutica de longa duração- Suspender se houver clearance do AgHBs
- Supressão vírica sustentada associa-se a melhoria histológica e do prognóstico (cirrose, CHC)
Cirrose Compensada: Tratamento de longa duração
Cirrose descompensada: Tratamento de longa duração (de preferência combinado LAM+ADV).
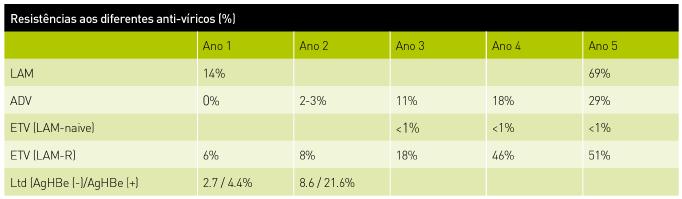
RESISTÊNCIAS
Consequências das Resistências
↑↑ HBV DNA
↑↑ ALT
]]> Agravamento da histologia Possível descompensação clínica (mau prognóstico em doentes cirróticos).
NOMENCLATURA
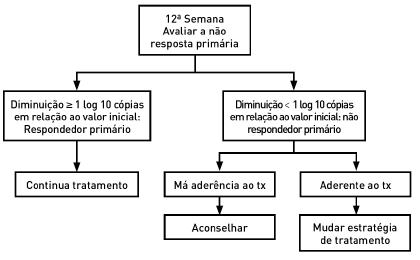
Não reposta (primary treatment failure)
Diminuição <1 log10 IU/ml do DNA do VHB após 3 meses de tratamento. Habitualmente relacionada com a má adesão à terapêutica.
Resistência genotípica: Mutação no genoma do VHB que se desenvolve durante o tratamento anti-vírico e que confere resistência (e diminuição da eficácia) ao agente anti-vírico.
Breakthrough virulógico: Rebound do DNA do VHB (> 1 log10 IU/ml) durante o tratamento após o desenvolvimento de resistências genotípica.
Breakthrough clínico e bioquímico: Elevação da ALT. Coincide frequentemente com uma elevação da carga viral e pode resultar num flare de hepatite e mais raramente em descompensação hepática.
]]>
ESTRATÉGIAS DE PREVENÇÃO DE RESISTÊNCIAS
Prevenção
Maximizar o tratamento anti-vírico: Evitar tratamentos desnecessários; Seleccionar o regime antivírico mais eficaz, com a mais baixa taxa de resistências.
Maximizar as barreiras géneticas às resistências: Evitar monoterapia sequencial; evitar interrupções de tratamento; Escolher fármacos que requerem múltiplas mutações para a resistência.
Aumentar as barreiras farmacológicas: Assegurar a adesão do doente ao tratamento.
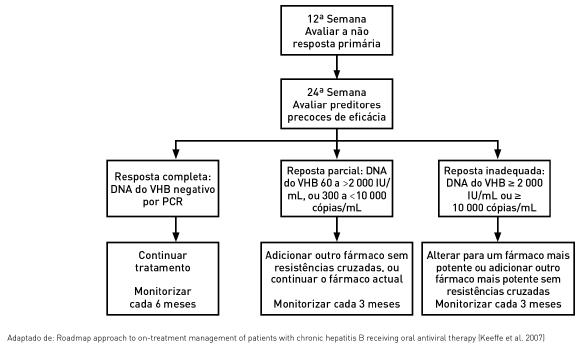
Monitorização
Modificação precoce da estratégia de tratamento (antes da elevação da carga viral).
]]>Tratamento das resistências
Lamivudina-R: Adicionar tenofovir ou adefovir
Adefovir-R: Adicionar lamivudina; Alterar ou adicionar entecavir
Entecavir-R: Alterar ou adicionar tenofovir ou adefovir
Telbivudina-R: Alterar ou adicionar tenofovir ou adefovir.
*Sociedade Portuguesa de Gastrenterologia
Data de elaboração: Junho de 2008
]]>