Regeneração do menisco humano por engenharia de tecidos. Nova abordagem celular e acelular
Hélder PereiraI, II, III, IV; Joana Silva-CorreiaI, II; Ana Margarida FriasI, II; Joaquim Miguel OliveiraI, II; José Mesquita MontesIV; Rui Luis ReisI, II; João Espregueira-MendesI, II, III
I. Clínica Espregueira-Mendes. Porto. Portugal.
II. Grupo de Investigação 3B's - Biomateriais, Biodegradáveis e Biomiméticos. Universidade do Minho - Sede do Instituto Europeu de Excelência em Engenharia de Tecidos e Medicina Regenerativa. Guimarães. Portugal.
III. Departamento de Ortopedia do Centro Hospitalar Póvoa de Varzim - Vila do Conde. Póvoa do Varzim. Portugal.
IV. Laboratório Associado ICVS/3B?s. Braga. Portugal.
RESUMO
]]> A meniscectomia (total ou parcial) tem sido a abordagem clínica mais frequente no que respeita ao tratamento da maioria das lesões do menisco. A reparação meniscal representa uma tendência recente, uma vez que a importância funcional destas estruturas na articulação do joelho e as consequências a longo prazo da sua remoção são agora melhor compreendidas. Contudo, as suas indicações são ainda limitadas e, apesar de garantir melhores resultados funcionais e radiológicos a longo prazo, as técnicas de reparação apresentam ainda uma taxa muito elevada de falência e reintervenção.As lesões destas estruturas continuam a estar entre as mais frequentes patologias que motivam intervenção cirúrgica em Ortopedia e têm um importante impacto sócio-económico.
Verificamos um interesse crescente da comunidade médica nos aspetos da biologia do menisco humano mas continuam a existir poucos estudos relacionados com este tema. Um dos objetivos desde grupo de investigação é acrescentar conhecimento relevante sobre este tecido com o objetivo de facilitar aplicações clínicas futuras, nomeadamente pelo conhecimento das propriedades biomecânicas do menisco a fresco (sem processo de congelamento) e da sua biologia celular. Da análise mecânica dinâmica (DMA) dos segmentos do menisco humano a fresco observamos a seguinte tendência decrescente de rigidez: segmento anterior MI (0,25 MPa a 1Hz)
Efetuamos a primeira revisão sistemática da literatura sobre aplicações da Engenharia de Tecidos e Medicina Regenerativa aplicadas às lesões meniscais para aferir o estado da arte.
Existem poucos biomateriais em aplicação clínica atualmente com esta finalidade. Diferentes opções têm sido testadas como estruturas tridimensionais porosas (scaffolds) viáveis (derivados do colagénio, poliuretano ou poliglicerol, enxertos de submucosa, hidrogéis acelulares) mas muitas questões permanecem por responder apesar de, nos ensaios pré-clínicos e poucos ensaios clínicos publicados, serem apresentadas perspetivas promissoras. Matrizes derivadas de colagénio e de poliuretano estão já comercialmente disponíveis para substituição parcial de menisco mas existem algumas preocupações relativas à sua estabilidade, taxa de degradação, e biocompatibilidade. Por outro lado, poucos estudos combinam estratégias de regeneração baseadas em abordagens acelulares e celulares existindo aí uma diferença marcada nas abordagens por estudos clínicos e pré-clínicos.
Para cumprir o objetivo de regeneração deste tecido existe um longo caminho a percorrer na descoberta da melhor forma de aplicar a tríada da Engenharia de Tecidos (matrizes, células, fatores de crescimento ou substâncias bioativas) ou mesmo abordagens mais complexas por Medicina Regenerativa (manipulação de células estaminais, genética, nanotecnologia) para responder à recuperação deste tecido concreto e adequado aos vários mecanismos de lesão estabelecidos.
Foi testada a viabilidade de um novo biomaterial derivado de solução aquosa de elevada concentração de fibroína de seda desenvolvida na nossa instituição, e que permite combinar propriedades mecânicas e biológicas promissoras para uso como estrutura tridimensional porosa em zonas articulares de carga. Esta nova scaffold apresenta vantagens por comparação aos materiais existentes considerando os dados adquiridos na nossa caracterização do menisco a fresco.
A nossa hipótese é que estes biomateriais processados como scaffolds e combinados com células (isoladas do tecido nativo ou diferenciadas previamente de células estaminais, e.g. tecido adiposo abdominal ou bolsa de Hoffa), permitirão desenvolver estratégias regenerativas, capazes de ultrapassar algumas limitações e preocupações associadas às práticas que estão já em uso clínico.
Um segundo objetivo será completar esta abordagem reconhecendo e controlando o processo de neovascularização/inervação adversa. A nossa hipótese será que é positivo incrementar a neovascularização na zona periférica (facilitando a adesão e integração) e inibi-la na área mais central do menisco aí preservando o fenótipo dos meniscócitos (responsáveis pela manutenção das propriedades biomecânicas) e inibindo desenvolvimento de nocireceptores em zonas de carga. Pelo uso de um outro biomaterial original do nosso grupo (Goma gelana metacrilada) foi conseguido, pelo ensaio de angiogénese na membrana corioalantóica do embrião de galinha demonstrar pela primeira vez a possibilidade de manipular a neovascularização em tecido de menisco humano.
Com base nos resultados obtidos foi possível construir uma nova hipótese para abordagem por Medicina Regenerativa aos defeitos do menisco implicando o uso de células, fatores de crescimento e novos biomateriais desenvolvidos no nosso Grupo (fibroína de seda e goma gelana). Decorre ainda dos mesmos um modelo original de diferenciação para regeneração do menisco considerando a assimetria do tecido nativo, respeitando a distribuição determinada pelas áreas defi nidas pelo grau de vascularização do menisco humano adulto.
Concluída a fase de estudo in vitro, está já em curso a subsequente análise in vivo incluindo modelo em ovelha pois tem sido largamente estudada como modelo de artrose do joelho humano por partilhar vários aspetos da biomecânica e biologia desta articulação.
]]> Palavras chave: menisco, células, factores de crescimento, implantes, engenharia de tecidos, medicina regenerativa.
1. INTRODUÇÃO DA DESCOBERTA DAS FUNÇÕES DO MENISCO À REPARAÇÃO E REGENERAÇÃO
As lesões do menisco são das mais comuns da articulação do joelho [1]. Mais de 450.000 meniscectomias artroscópicas são realizadas a cada ano nos Estados Unidos[1], continuando a ser um dos procedimentos cirúrgicos ortopédicos mais frequentes2. O resultado clínico correlaciona-se com o estado da cartilagem, estabilidade articular, alterações degenerativas articulares e quantidade de tecido removido[3,4].
A primeira descrição de uma meniscectomia pertence a Broadhurst[5], em 1866, em Londres. A que se seguiu, curiosamente num curto espaço de tempo, a primeira descrição de reparação meniscal por Thomas Annandale[6] em 1883.
Apesar dos relatos de King[7] em 1936 e Fairbanks[8] em 1948, que descreveram os efeitos deletérios da meniscectomia total, até aos anos setenta os meniscos foram consideradas como restos evolutivos, sem função, dos músculos da perna que poderiam ser extirpados sem consequências relevantes para a articulação[9]. Ghormley[10] aconselhava mesmo a excisão completa de qualquer menisco lesado afirmando que a meniscectomia parcial acarretava maior risco de danos na superfície articular. Nos anos cinquenta, Albert Trillat destacou o papel da preservação do muro meniscal e descreveu os benefícios da meniscectomia intramural[11]. Até 1970, Smillie[9] ainda recomendava a excisão total como tratamento de lesões meniscais, baseando-se na convicção que este seria o caminho para a sua regeneração - “When the entire meniscus is excised a new one grows in from the parietal synovial membrane”. McGinity em 1977[12] alertou sobre as poucas evidências científicas que sustentavam estas alegações uma vez que as descrições de Smillie de regeneração de um menisco similar ao original após a excisão total estavam em contradição direta com as observações de seu grupo de estudo. Em cerca de 800 artroscopias de second-look, nunca observaram regeneração de muro meniscal superior a cinco milímetros. Pela avaliação retrospetiva de 136 joelhos com mais de cinco anos de seguimento concluiu que a meniscectomia parcial acarretaria um maior respeito pela anatomia, menor morbilidade pós-operatória e mais rápida reabilitação funcional em comparação com a excisão total. Isto representou um virar de página histórico ao ditar uma nova direção no tratamento das lesões meniscais: preservação.
É impossível separar a cirurgia do menisco da história da Artroscopia. Em 1918, Kenji Takagi em Tóquio, realizou o primeiro procedimento artroscópico pelo exame de joelhos de cadáver com um citoscópio em meio gasoso[13]. No entanto, a primeira meniscectomia parcial artroscópica é geralmente atribuída a Masaki Watanabe (discípulo de Takagi) em 1962[14]. Seria ele o “pai” do primeiro artroscópio viável, produzido em série, capaz de realizar exploração intra-articular eficaz: o artroscópio número 21 de Watanabe. No entanto, a artroscopia começou a assumir maior importância na cirurgia do joelho, após os relatos de Robert Jackson[15,16] a partir de Toronto, que reintroduziu o entusiasmo por esta técnica no mundo ocidental. Nos anos oitenta, múltiplos estudos e autores reportaram vantagens na cirurgia artroscópica em detrimento da meniscectomia parcial a “céu aberto”[17-20].
Estudos de biomecânica confirmaram a importância dos meniscos na transferência de carga. Kurosawa et al[21] demonstraram que a meniscectomia total reduz a área total de contacto entre um terço e metade no joelho totalmente estendido. Eles transmitem cerca de 50% do peso corporal em extensão e cerca de 85% durante a flexão em carga do joelho. Em ensaios in vitro foi demonstrado que a transmissão da carga através dos meniscos é de cerca de 70% no compartimento lateral e 50% no compartimento medial[22]. A descrição da macro-anatomia dos meniscos está fora dos propósitos deste trabalho mas temos de considerar que os meniscos não estão firmemente ancorados na tíbia e acompanham, em alguma extensão, a translação articular no sentido anteroposterior durante o movimento. Devido a razões anatómicas o menisco interno (MI) é menos móvel. No joelho estável (pivot central íntegro) o MI tem um papel pouco importante na oposição à translação anterior da tíbia pois o ligamento cruzado anterior (LCA) sustém esse movimento antes de ocorrer um conflito significativo entre o corno posterior do MI e prato tibial com o côndilo femoral interno. Contudo em movimentos extremos, ou perante lesão do LCA, funciona como restritor secundário à translação anterior da tíbia (o que está associado a alguns mecanismos de lesão)[23]. Outro aspeto fundamental é a assimetria dos compartimentos femurotibiais. Podemos descrever, o prato tibial externo como convexo por oposição à forma mais côncava do prato interno. Por este motivo, a perda do menisco externo (ME) tem uma implicação comparativamente maior na perda de congruência femurotibial. Walker et al[24] concluíram que o ME transmite a maior parte da carga do compartimento externo enquanto no interno essa transmissão de força é mais dividida entre as superfícies cartilagíneas envolvidas e o respetivo menisco[25].
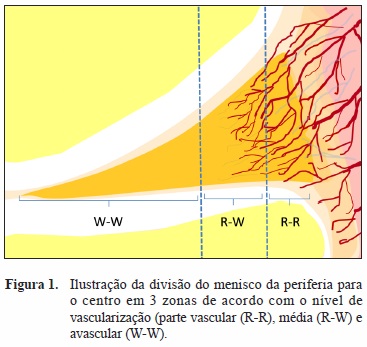
Arnoczky et al[21] descreveram a anatomia microvascular do menisco humano[26] e os processos de resposta a lesão a partir de modelo de cão[27] no início dos anos oitenta. A periferia do menisco é vascularizada e preserva alguma capacidade de reparação por oposição à parte central que é avascular e recebe nutrição pelo líquido sinovial. Com base nestes estudo continua a ser usada uma divisão do menisco da periferia para o centro em 3 zonas de acordocom o nível de vascularização (zonas: red-red; red-white e white-white (Figura 1).
]]>

A cirurgia aberta de reparação meniscal teve DeHaven[28] como o seu principal impulsionador nos EUA, suportado na Europa por Beaufils e Cassard[29]. Tem havido um esforço crescente no estabelecimento das indicações, melhoria das técnicas e materiais de sutura até aos dispositivos de sutura all-inside de última geração[30]. Contudo, apesar de garantir melhores resultados funcionais e radiológicos a longo prazo a reparação está ainda limitada nas suas indicações (maioria dos autores limita a reparação a lesões em zona vascularizada, ruturas agudas/subagudas, excluindo ruturas radiais ou horizontais). Por outro lado, apesar das melhorias muito significativas introduzidas continua a estar associada a uma taxa de falência e necessidade de revisão cirúrgica elevadas[30].
Kohn et al[31] e Milachowski et al[32] introduziram o transplante de menisco no algoritmo de tratamento do joelho com múltiplas lesões/lesões complexas reconhecendo o seu papel na estabilidade e proteção da cartilagem como determinante na reabilitação articular.
Outros desenvolveram esta técnica até ser considerada atualmente uma terapia fiável em doentes selecionados[33-35] com bons resultados, em alguns casos com mais de vinte e cinco anos de seguimento[36]. Contudo, existem limitações importantes a considerar nomeadamente quanto à disponibilidade de dadores, investimento e problemas logísticos do processo de recolha e armazenamento, transmissão de doenças, ou diminuição da viabilidade do tecido causadas pela criopreservação ou congelamento a fresco.
A aplicação de scaffolds acelulares para substituição parcial de defeitos de menisco está já em fase embrionária de prática clínica com resultados promissores mas limitações igualmente reconhecidas entre os autores nomeadamente quanto à estabilidade, biomecânica e biocompatibilidade.
Citando René Verdonk[37] - "Nothing has changed so much in knee treatment and surgery as meniscal treatment algorithms" – Esta afirmação sumariza claramente a revolução que ocorreu recentemente na abordagem das lesões meniscais.
Os novos desafios visam melhorar as técnicas de reparação alargando a sua aplicação, nomeadamente às lesões em área avascular, e diminuir a sua taxa de falência. Em relação aos casos de perda irreparável de tecido, o objetivo maior seria o recurso a Técnicas de Engenharia de Tecidos e Medicina Regenerativa para criar uma fonte virtualmente inesgotável de tecido cumprindo todas as exigências de segurança capazes de reparar com qualidade o defeito ou mesmo ser usado como substituição total do menisco.
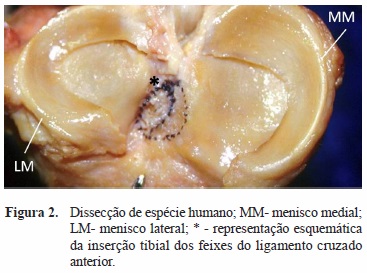
Hoje é consensual assumir que o menisco humano (Figura 2) tem um papel fundamental na homeostasia do joelho com funções na transmissão de carga, absorção de impacto, nutrição e lubrificação, aumento da congruência articular e propriocepção.
]]>
Este trabalho visa contribuir para a prossecução desse objetivo de preservação, reparação e substituição, apresentando novas opções de biomateriais e novas estratégias de Medicina Regenerativa com aplicação ao tratamento do menisco.
2. ESTADO ATUAL DAS APLICAÇÕES DE ENGENHARIA DE TECIDOS E MEDICINA REGENERATIVA: REVISÃO SISTEMÁTICA DA LITERATURA (INVESTIGAÇÃO ORIGINAL)
INTRODUÇÃO
O advento da Engenharia de Tecidos (ET) promete revolucionar a Medicina proporcionando estratégias que mimetizam os mecanismos normais de reparação e regeneração que ocorrem na natureza
Tal como descrito por Langer e Vacanti[38], a ET é o campo do conhecimento que recorre aos princípios quer da Engenharia quer das Ciências da Vida visando o desenvolvimento de substitutos biológicos para reparar, manter ou melhorar a função dos tecidos.
]]> As abordagens de ET, por definição, recorrem a três variáveis principais (tríada da ET), i.e., matrizes (scaffolds), células (diferenciadas ou indiferenciadas) e agentes bioativos incluindo fatores de crescimento (FCs), que podem ser implantados no local da lesão de forma isolada ou combinada.Por outro lado a Medicina Regenerativa é um conceito mais abrangente e além de abranger o uso de moléculas solúveis e células estaminais ou duferenciadas, aplica igualmente estratégias terapêuticas recorrendo a ET e terapia génica para estabelecer ou reparar o funcionamento normal de células/tecidos/órgãos.
Depois do reconhecimento da importância dos meniscos em manter a homeostasia do joelho tem vindo a ser tentado o desenvolvimento de tratamentos regenerativos como alternativa ou complemento dos procedimentos tradicionais de reparação ou meniscectomia.
Esta necessidade de reparação/regeneração meniscal tem vindo a merecer interesse crescente dos clínicos com sucessivos apelos para a preservação do menisco - "Save the Meniscus"[39]. E quando a preservação ou reparação deixam de ser viáveis, o caminho que tem vindo a ser proposto como mais adequado é o da substituição[40], com experiência e consenso crescentes relativos à transplantação meniscal com aloenxerto em casos selecionados.
Se considerarmos o significativo impacto socioeconómico desta lesão (pela sua frequência e por atingir muitas vezes uma população jovem no pico da sua capacidade produtiva), e atendermos à escassez de soluções clínicas até ao momento, parece evidente a necessidade de desenvolvimento de novas opções[8] para responder às necessidades e expectativas dos pacientes.
A comunidade clínica em geral (incluindo ortopedistas) tem vindo a reconhecer a importância crescente da investigação em ciências básicas, Engenharia de Tecidos e Medicina Regenerativa[41] (ETMR) no aparecimento de uma nova linguagem e um novo mundo de opções e perspetivas para lidar com problemas clínicos. O Multicenter Orthopedic Outcomes Network (MOON), de um cohort prospetivo de jovens submetidos a reparação do ligamento cruzado anterior concluiu que existe um “mercado” potencial importante para aplicações de ETMR às lesões do menisco quer através do desenvolvimento de scaffolds, quer alargando a possibilidade de reparação à zona avascular, quer desenvolvendo formas de reparação inteiramente biológicas sem recurso a implantes[42].
Sendo a reparação/regeneração meniscal um tema quente em Ortopedia, e mais recentemente sendo-o também em ETMR reconhecemos a necessidade de reunir e organizar os avanços mais recentes nesta área.
O propósito desta revisão sistemática da literatura é sumariar e hierarquizar os estudos publicados de estratégias de ETMR aplicadas ao menisco, proporcionando igualmente uma narrativa sistemática que permita aos clínicos/especialistas familiarizaremse com os avanços mais recentes neste campo.
Assim, é aqui organizada toda a informação relevante relacionada com: (i) aplicações clínicas, indicações, resultados e complicações; e (ii) principais correntes de investigação no campo da reparação/ regeneração meniscal aferida pela análise dos estudos pré-clínicos (in vivo) publicados.
Além de estabelecer um estado da arte das aplicações clínicas neste tópico visamos igualmente apresentar a informação relevante perto da clinica para facilitar o passo fi nal de transição do conhecimento do laboratório para a cabeceira dos doentes num futuro próximo, e ajudar o recentemente reconhecido "clínico ortopedista-cientista"[43] a conceber e efetivar projetos válidos de investigação.
]]> MATERIAL E MÉTODOSTrês investigadores independentes realizaram uma pesquisa usando a base eletrónica PubMed de todos os trabalhos originais publicados de 2006 a março de 2011 usando o termo "Meniscus" combinado com qualquer dos seguintes: "Scaffolds", "Constructs", "Cells", "Growth factors", "Implant", "Tissue engineering" e "Regenerative Medicine". Um segundo período (2000 a 2005) foi considerado de forma a aferir a evolução do interesse neste tópico refletido no número de publicações.
Os critérios de inclusão foram: artigos em língua inglesa, ensaios clínicos originais (nível I a IV[44]), e estudos pré-clínicos (in vivo) implicando estratégias TERM aplicadas às lesões dos meniscos. O score Metodológico de Coleman Modificado[45] (MCM) foi usado para aferir qualitativamente os ensaios clínicos selecionados.
Todos os artigos identificados foram analisados e discutidos entre os investigadores e tomada a decisão final de inclusão ou exclusão. Até julho de 2011 (pré-publicação), além das referências bibliográficas as bases eletrónicas dos jornais identificados foram verificadas em busca de artigos relevantes não identificados na pesquisa original. Perante ausência de acordo a decisão final foi tomada por um dos autores (R.L.R.).
RESULTADOS E DISCUSSÃO
Pelo método descrito foram identificados no período de 2000 a 2005, 161 artigos enquanto de 2006 a março de 2011 este número aumentou para 285 (Quadro I).

]]> Destes (n=285), 102 foram excluídos por terem sido classificados como não relacionados com o tópico, 9 por não estarem escritos em língua inglesa e 19 por serem estudos de nível V.
Não foi encontrada nenhuma revisão sistemática da literatura relativa a este tema.
Foram ainda excluídos 118 estudos in vitro incluindo estudos de cultura celular, ensaios biomecânicos ou de citotoxicidade de biomateriais.
Uma (n=1) referência foi identificada pela pesquisa da lista de referências. Considerando os critérios definidos foram identificadas 38 referências para análise[46-83]. Duas outras referências (n=2) foram incluídas pela pesquisa pré-publicação[84,85].
Estudos clínicos de aplicações de Engenharia de Tecidos para regeneração meniscal
Dos estudos clínicos um corresponde ao nível de evidência I68, dois ao nível II61,79 , e seis ao nível IV[48,52,22,78,83,84]. A Quadro II sumariza a experiência clínica de estratégias de ET para tratamento do menisco lesado ou degenerado. A média do score MCM de todos os estudos foi de 48,0 (S.D.=15,7).
]]> Na sua maioria, 8/9 estudos referem-se a implantação de scaffold acelular para reparação de defeitos parciais do menisco (sete referem-se a matrizes baseadas em colagénio e em um estudo baseada em poliuretano). Apenas um estudo se refere à possibilidade de aplicação de coágulo de fibrina (abordagem por scaffold-fatores de crescimento) como potenciador da reparação de ruturas horizontais na zona avascular.
Os sete estudos publicados relacionados com aplicação do Collagen Meniscus Implant (CMI, atualmente conhecido por Menaflex®, ReGen Biologics, USA) envolveram 565 pacientes dos quais 487 foram avaliados e 304 receberam implantes CMI. Todos aplicados em defeitos do menisco interno. O score MCM médio dos ensaios com CMI foi 50,6 (S.D.=12,6). Um estudo comparou resultados de osteotomia tibial de valgização isolada (OTV) com a combinação de OTV e CMI61; dois usaram a meniscectomia parcial como grupo de controlo[68,79] e os restantes são séries de casos sem controlo. Os controlos incluíram 167 meniscectomias parciais e 16 OTV. A idade media reportada para aplicação de CMI variou entre 29,2[68,84] e 41,8 anos[61]. Um dos estudos não fornece informação relativa ao género[61] mas dos restantes 223 são homens e 61 mulheres. O seguimento médio variou de 24[61] até 133 meses[79, 84]. Um estudo refere apenas seguimento até 24 meses[52] as não fornece nenhum valor numérico de medida de tendência central.
As cirurgias concomitantes à aplicação do CMI incluíram 96 reparações do ligamento cruzado anterior (LCA)[48,52,68,79,82,84], 26 OTV[48,52,61], e 7 microfracturas[48,52,78,79,84] e 2 transplantes autólogos de condrócitos[52] para tratamento de lesões condrais de grau III.
Cinco ensaios dividiram os candidatos em dois grupos: (i) lesões meniscais agudas irreparáveis e (ii) grupo de lesões crónicas com perda prévia de tecido[48,52,68,78,79]. Apenas dois forneceram alguma informação sobre a classificação (tipo) de lesões meniscais[48,84]. Pouca informação é fornecida sobre o tipo e o tempo decorrido entre as cirurgias prévias e a cirurgia de implantação[68,78,84]. No estudo que considera a aplicação do CMI em pacientes candidatos a OTV nenhuma informação sobre o alinhamento no plano frontal pré- ou pós-operatório foi fornecida nem para os casos nem para os controlos[61]. O intervalo do tempo decorrido desde a lesão, o início dos sintomas ou a meniscetomia prévia foi pobremente ou não definido de todo.
Vários scores clínicos diferentes foram usados. Em ordem decrescente de frequência: Lysholm score (n=5) [48,61,68,79,84], escala subjetiva visual analógica (VAS) da dor (n=5)[61,68,78,79,84], Tegner activity level score (n=3) [48,68,79], International Knee Documentation Committee (IKDC) avaliação objetiva (n=2)78,79 e subjetiva (n=1) [61], Cincinnati knee rating scale (CKRS; n=1)[78] e SF-36 score (n=1)[79]. O Tegner score pré-operatório foi baseado na memória dos pacientes em dois estudos[68,79]. Um estudo desenhado para avaliação por ressonância magnética (RM) não apresenta resultados cínicos[52]. Apesar desta diversidade, poucos dados numéricos de estatística descritiva e resultados clínicos são apresentados (incluindo escassez ou mesmo ausência de medidas de dispersão) limitando a análise global dos resultados fornecidos.
Quatro estudos apresentam avaliação radiológica independente[48,78,79,84]. Um usou o Kellgren-Lawrence score[48], e outro[79] comparou a diminuição da interlinha articular entre o joelho operado e o contralateral (saudável), Monllau et al[84] usou a classificação de Ahlbäck e nenhum método específico é referido no quarto[78].
A avaliação por RM é apresentada em cinco estudos[48,52,78,79,84]. Genovese et al[52] descreveu um score de RM de 1 a 3 graus em que um score mais alto corresponde a uma maior aproximação ao menisco normal quanto a características morfológicas ou de sinal. Este método foi usado em três estudos subsequentes[48,79,84]. Genovese et al[52] propôs avaliação por artro-RM para melhor aferição das lesões condrais (em dois casos a RM convencional falhou na deteção de lesões condrais que só foram detetadas na artro-RM) o que foi também considerado pelo grupo de Bulgheroni[48].
Quatro ensaios[48,52,61,78] apresentaram resultados de artroscopias subsequentes (second look arthroscopies) num total de 187 pacientes.
O comprimento médio do CMI aplicado foi apresentado em três estudos[48,79,84] e variou entre 3,6 e 4,8 cm. Um aumento da área total de tecido considerando o muro meniscal existente na cirurgia de implantação e o novo tecido formado registado na artroscopia de second look foi também descrito[68]. Foram efetuadas biópsias em 149 doentes de dois ensaios[48,68]. Nenhum método específi co de avaliação ou classificação histológica objetiva reprodutível foi usado. Os resultados referidos baseiam-se em estimativas visuais ou descrições histológicas genéricas.
Considerando como falência a impossibilidade de identificar o implante na RM, 7 casos foram descritos[52,78,79,84]. Um deles foi reoperado para remoção de restos do implante, e a artroscopia de second-look confi rmou o diagnóstico[52]. Nenhuma outra consideração foi referida para os restantes. Além deste, 6 outros foram removidos, num total de 7: um por desorganização[84]; um por desorganização e luxação[61]; dois por falência precoce de fi xação[48,68] (um dos pacientes não cumpriu indicações pósoperatórias[48]); um por infeção[68] e um outro por causa não especificada[68].
]]> Derrame e/ou dor, rigidez, bloqueio ou sensação de instabilidade determinaram necessidade de reoperação em 8 doentes[68,79,84]. As reintervenções relacionadas com o método de implantação do CMI incluíram ainda um caso de compressão de um ramo infrapatelar do nervo safeno que necessitou de neurolise[48] perfazendo um total de 15/282 pacientes reoperados por complicações consideradas como possivelmente relacionados com o método.Os procedimentos de reintervenção incluíram desbridamento/lavagem artroscópica isolada ou combinada[48,52,61,68,78,79], OTV[68,79,84], reconstrução do LCA[68], meniscectomia parcial[68] e transplante de menisco de cadáver[84]. Uma redução na dimensão do implante foi referida em todos os estudos, registada por RM ou second look. Contudo, a incidência exata desta ocorrência não pode ser apresentada uma vez que o problema não foi especificamente abordado e nem a sua magnitude nem a implicação no resultado clínico foi estudada.
Não foi registado nenhum dado clinicamente relevante quanto a inflamação ou resposta imune significativa ao CMI nas biópsias efetuadas.
Apenas um estudo multicêntrico de nível de evidência IV[83] com 52 pacientes se refere à experiência clínica com o implante baseado em poliuretano (Actifit®, Orteq Ltd, London, United Kingdom). Destes, 39 são homens e 13 mulheres com idade média de 30,8 (S.D. = 9,4) anos, 34 por lesão do menisco interno e 18 do externo com comprimento médio de 47,1 mm.
Não foram apresentados resultados clínicos, os autores propuseram-se aferir a segurança e crescimento de novo tecido recorrendo a análise independente por RM (cega para dados clínicos) incluindo imagens de RM potenciada por injeção dinâmica de contraste (DCE-MRI; método para aferir vascularização do tecido). Análise histológica qualitativa é apresentada para 44/52 casos. Foi registado um caso de não integração da scaffold ao menisco nativo aos 12 meses. As complicações registadas aos 12 meses de seguimento incluem: um paciente que desenvolveu infeção (1 semana após cirurgia o implante foi removido); um paciente submetido a prótese total do joelho 4 meses após implantação (considerado pelos autores um erro de inclusão por artrose severa desde o início); e um caso de enfarte do miocárdio. Todos estes casos foram considerados como não relacionados com o implante.
Um único ensaio[56] propôs uma estratégia para expandir a indicação de reparação às ruturas horizontais em zona avascular pelo recurso ao coágulo de fibrina. O defeito é preenchido com coágulo de fibrina antes de ajustar as suturas num efeito tipo “sandwich”. Esta série inicialmente refere aplicação em 3 meniscos internos e 6 externos. Conclusões genéricas de melhoria nos scores funcionais são descritas mas apenas o score de Lysholm está acessível e para um único doente.
Estudos pré-clínicos de aplicações de Engenharia de Tecidos para regeneração meniscal
Para sistematizar os dados desta análise os ensaios pré-clínicos (n=31) foram agrupados de acordo com o modelo animal usado, i.e., pequenos ou grandes animais. As correntes de investigação apresentadas incluem: estratégias de potências reparação por sutura; substituição parcial ou total; e terapias percutâneas para aumentar reparação tecidular ou diminuir a sua taxa de degradação. Dos trinta e ensaios pré-clínicos onze usaram modelos de grandes animais incluindo porco, ovelha e cabra. Da análise concluímos que quatro se focam na aplicação de scaffolds acelulares[49,62,82,85], seis estudos combinam scaffolds com células quer alogénicas[73,74] quer autólogas[59,63,73] ou combinam scaffolds com fatores de crescimento (VEGF)[60,66]. Uma abordagem por terapia génica é apresentada em um estudo pela combinação de um gel de alginato injetável com células humanas da medula óssea transfectadas com IGF-1[81].
Vinte estudos usaram modelos de pequenos animais como camundongo, rato, coelho e cão salientando-se que estão centrados essencialmente no estudo de scaffolds acelulares ou combinação de células com scaffolds (conhecidos por constructs).
Na realidade, combinando todos os ensaios préclínicos constatamos que onze se focam em abordagens por scaffolds acelulares[49-51,53,62,67,71,72,76,82,85], nove testaram scaffolds semeadas com células[47,57,59,63,69,73-75,77], dois testaram a combinação de células-scaffold-FCs[58,81] (FCs - fatores de crescimento) associada ainda a terapia génica num deles[81]. Adicionalmente um estudo comparou scaffold associada a células com scaffold associada a FCs[80] e um outro testou in vivo a imunocompatibilidade de uma scaffold (menisco de porco descelularizado) mas com intenção de aplicação numa abordagem por construct[70]. Três estudos testaram a combinação scaffold-FCs[55,60,66], três apresentam terapia injetável com células estaminais (MSCs)[46,54,64] e um apresenta terapia génica isolada[65]. A figura 3 ilustra a heterogeneidade e frequência das diferentes abordagens testadas em ensaios clínicos e pré-clínicos.
]]>
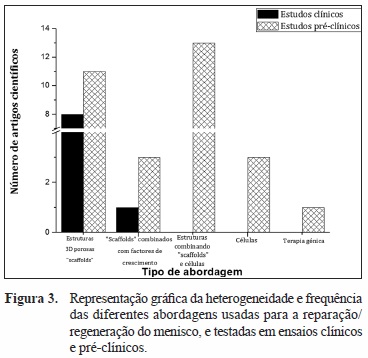
Enquanto a maioria dos ensaios clínicos reporta à implantação de scaffolds acelulares para substituição de um defeito irreparável do menisco (8 de 9 estudos), a mesma tendência não se verifica na investigação em fase pré-clínica. Nesta última, a maioria dos estudos relacionados com o uso de scaffolds (n=27) favorecem o seu uso combinada com células (constructs) e/ou com fatores de crescimento (16/27).
A maioria dos pacientes dos ensaios clínicos avaliados encontram-se na sua terceira a quinta décadas de vida. Considerando ainda que as lesões do menisco permanecem como a causa mais frequente de lesão dos joelhos que implicam tratamento cirúrgico[7], podemos extrapolar consequências relevantes do absentismo laboral e impacto socioeconómico decorrentes desta entidade patológica. Nesta população jovem podemos esperar genericamente um razoável estado da cartilagem em joelhos estáveis (ou estabilizados) com lesões dos meniscos, constituindo o alvo ideal para defender a função dos meniscos visando proteger a degeneração articular precoce. Por todos estes factos sublinha-se a importância clínica deste tópico e o significativo impacto socioeconómico do desenvolvimento de novas possibilidades terapêuticas eficazes nesta área. Seguramente que a prossecução deste objetivo requer o domínio pelos clínicos desta nova área do conhecimento com a sua linguagem específica e o esforço combinado de várias áreas de ciência incluindo Ortopedia, Veterinária, Bioquímica, Biologia, Engenharia de Tecidos ou Medicina Regenerativa. Contudo o acesso a estudos de ciência básica nem sempre é fácil para clínicos pelo que o papel do ortopedista clínico-cientista[43] terá um papel fundamental no desenvolvimento de novos horizontes e no levantar de um novo tipo de soluções para alguns "velhos" problemas clínicos.
Nos oito estudos clínicos reportando ao uso de scaffolds encontramos consenso quanto às suas indicações independentemente do material aplicado que podemos resumir: (i) perda irreparável traumática ou degenerativa de tecido meniscal preservando as inserções anterior e posterior do menisco além de um muro meniscal residual; (ii) doentes biologicamente jovens; (iii) joelhos estáveis ou estabilizados cirurgicamente. Da mesma forma quanto aos critérios de exclusão: (i) insuficiência do pivot central; (ii) alterações degenerativas marcadas do compartimento afetado ou global; (iii) desvio axial major no plano frontal não corrigido; (iv) artrite inflamatória ou patologia autoimune; (v) infeção ativa ou patologia neurológica que impeçam o cumprimento das indicações pós-operatórias.
Nos estudos comparativos[61,68,79] os controlos submetidos a meniscectomia parcial cumpriram um plano de reabilitação diferente do dos doentes que receberam implantes e este facto não foi esclarecido para os doentes submetidos a osteotomia tibial de valgização (OTV)[61]. Este facto pode influenciar os resultados a curto prazo mas temos de concordar que será provavelmente irrelevante para um tempo de seguimento mais longo[79]. Da nossa análise não foi possível concluir qual o tipo de controlo mais adequado para avaliar estratégias de substituição parcial, i.e., meniscectomia parcial ou OTV.
A variedade de scores clínicos usados e a escassez de dados numéricos fornecidos limita a aferição global e conjugada dos resultados e este facto deve ser considerado em ensaios futuros.
Todos os estudos que usaram o Menafllex®/CMI apresentaram algum grau de melhoria clínica por comparação ao estado pré-operatório[48,52,61,68,78,79,84]. Comparando com OTV isolada, Linke et al[61] não encontrou diferenças significativas. Zaffagnini et al[79] e Rodkey et al[68]usando como controlos meniscectomia parciais não conseguiram estabelecer diferenças significativas no score de Lysholm. Considerando o parâmetro dor para os casos com CMI, um não conseguiu encontrar diferenças[68] mas resultados signifi cativamente melhores foram descritos pelo outro[79].
]]> Uma nova ferramenta para aferir resultados foi proposta por Rodkey et al[68] (e usada num estudo subsequente[79]), o index Tegner (IT) que tenta avaliar a percentagem de nível de atividade perdida que foi recuperada como resultado do tratamento. É calculada pela subtração do score Tegner pré-operatório pelo score obtido na última avaliação e depois divide-se a diferença obtida pelo resultado da subtração do score prévio à lesão pelo score obtido imediatamente antes da cirurgia.Na série de Zaffagnini et al[79] e no ramo crónico da série de Rodkey verificou-se uma melhoria significativa do IT que não se verificou no ramo das lesões agudas deste último[68]. Além destes dois[68,79] trabalhos não conseguimos identificar nenhum outro trabalho validando o IT como ferramenta de medição da quantidade de perda de atividade que é recuperada após a cirurgia. Além disso, nestes trabalhos o score Tegner pré-operatório foi calculado com base namemória dos pacientes pelo que se deve considerar a fonte de viés daí inerente.
O score de RM descrito por Genovese et al[52] tem sido usado subsequentemente o que facilita a análise deste parâmetro. Alguma maturação de tecido parece ocorrer com o tempo, contudo características básicas da sua constituição e características volumétricas constituem aspetos críticos do sucesso e permanecem mal defi nidas.
As biopsias têm sido descritas com base em estimativas genéricas. Seria útil a definição de parâmetros histológicos objetivos a serem reproduzidos pelos vários ensaios. O novo tecido obtido tem sido descrito como sendo não fibrocartilagem pura mas um tecido híbrido com algumas semelhanças[68].
Apesar de infrequentes têm sido descritas falências precoces por deslocação ou reabsorção do implante. Uma diminuição do tamanho do implante em alguma magnitude tem sido frequentemente descrito apesar de não ter sido ainda possível estabelecer uma relação entre este facto e os resultados clínicos. Algumas preocupações quanto às pobres propriedades biomecânicas iniciais foi também referida[45].
Um dado consistente em todos os estudos é a ausência de respostas inflamatórias ou imunológicas específicas do implante clinicamente relevantes.
O único studo relativo à aplicação do implante baseado em poliuretano (Actifit®, Orteq Ltd, London, United Kingdom) foi desenhado para testar o perfil do implante quanto a ser biocompatível, biomimético e biodegradável além do seu perfil de segurança[83]. Decorrentes desse facto não foram fornecidos dados relativos aos resultados clínicos. As dimensões e características dos defeitos tratados foram similares às descritas nos estudos com CMI. A inclusão da RM potenciada por injeção dinâmica de contraste (DCEMRI) permitiu a aquisição de dados importantes e poderia ser usada no futuro para comparação com o CMI em termos de tempo e qualidade de integração. Foi apresentada análise histológica qualitativa para 84,6% dos casos com resultados descritivos relativamente a vascularização, celularidade e matriz extracelular. Foi descrita uma distribuição do neotecido que inclui uma cápsula fibrosa vascularizada e três camadas distintas. Este método deve ser considerado em trabalhos futuros. Foi descrito um caso de falência precoce mas, tal como para o CMI, não foi descrita nenhuma resposta inflamatória ou imunológica clinicamente relevante relacionada com o implante. Apesar dos resultados positivos na avaliação por RM e histologia são necessários resultados clínicos de ensaios prospetivos controlados e "randomizados" antes de se poder concluir as vantagens da disseminação do método.
Além disto, existindo duas propostas de implantes tão diferentes com os mesmos objetivos seria vantajosa a realização de estudos clínicos comparativos entre ambos.
Deve ainda ser considerado que estamos na fase inicial da experiência com uma nova tecnologia e a possibilidade de ocorrer um viés de publicação[86,87] (tendência dos investigadores e editores de lidarem com os dados "positivos", i.e. significativos, obtidos na investigação de forma diferente da que lidam com os resultados "negativos", i.e., a favor da hipótese nula, ou inconclusivos) deve ser considerada.
Numa proposta completamente diferente, Kamimura et al[56] descreve experiência clínica com um método que visa ampliar a possibilidade de reparação meniscal às lesões horizontais em zona avascular. Apesar da inerente inovação do método, de encontrar algum suporte nos estudos de ciência básica, e de ter sido inicialmente classificado como estudo de nível de evidência IV, a escassez de dados clínicos objetivos fornecidos (refletida no MCM score de 19) aconselharia a sua classificação como estudo com nível de evidência V.
]]> Relativamente aos ensaios pré-clínicos verifica-se que existem propostas de novas abordagens por ETMR que ainda não passaram à fase de ensaios clínicos como terapia génica ou terapias percutâneas com células estaminais.Nos ensaios visando modelos de substituição parcial ou total do menisco a maioria dos autores favorece a amplificação de scaffolds por combinação a fatores bioativos e/ou células por comparação a abordagens acelulares.
CONCLUSÕES
Concluímos deste estudo um interesse crescente nas aplicações da Engenharia de Tecidos e Medicina Regenerativa aplicadas ao menisco mas esta é a primeira revisão sistemática da literatura neste tópico com inclusão da experiência clínica e in vivo. A substituição parcial por scaffolds acelulares baseadas em colagénio ou poliuretano em pacientes selecionados com lesões irreparáveis do menisco pode ser considerada segura e apresenta resultados promissores. Contudo, devem ser assinaladas algumas preocupações relacionadas com a fixação inicial e estabilidade dos biomateriais.
Deve ainda salientar-se que a maioria dos estudos pré-clínicos aponta possíveis vantagens das abordagens que combinem as scaffolds com células de origem diversa e/ou fatores de crescimento.
Novas e diferentes abordagens por ETMR continuam a surgir visando melhorar os processos de reparação, diminuir a taxa de degeneração ou terapias de substituição dos tecidos e estão em análise préclínica podendo, no futuro, abrir novos horizontes à prática clínica.
3. ULTRA-ESTRUTURA E BIOMECÂNICA: DESCOBRIR AS BASES PARA A REGENERAÇÃO MENISCAL (INVESTIGAÇÃO ORIGINAL)
]]> INTRODUÇÃO
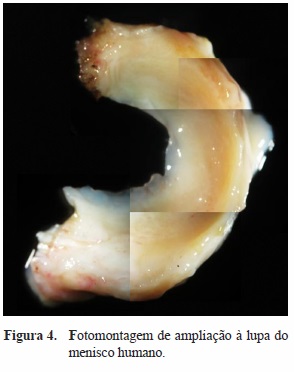
Existem muitos aspetos por explorar relativamente à caracterização biológica do menisco humano (Figura 4), mas o tema tem merecido um grande interesse nos últimos anos. Podemos afirmar que se tem prestado maior atenção ao estudo das diferentes populações celulares que o constituem, à investigação da sua ultraestrutura[88], densidade celular e distribuição da matriz extracelular, propriedades biomecânicas, e interações biológicas ou mecanismos de resposta a uma lesão.
Devido essencialmente às limitações inerentes ao estudo de tecidos humanos, a maioria dos estudos da biologia do menisco tem sido efetuado a partir de modelos animais ou, em menor número, a partir do tecido congelado de espécimes cadavéricos.
Apesar de algum possível viés da caracterização do menisco no joelho com algumas alterações degenerativas quando comparado com o menisco do jovem saudável, podemos encontrar suporte na literatura de que, em meniscos morfologicamente intactos, as alterações que se podem encontrar no que respeita à sua estrutura[89] ou às populações celulares[90] serão pouco relevantes.
Assim sendo, dada a maior possibilidade de acesso, e desde que estabelecidos critérios rígidos de inclusão, esta pode constituir uma fonte de tecido para estabelecer padrões mínimos das propriedades deste tecido[91,92] e ajudar a contribuir para o desenvolvimento de estratégias de engenharia de tecidos para aplicação clínica futura[91,92].
]]> MATERIAL E MÉTODOS
Amostras de tecido humano foram obtidas cirurgicamente nos hospitais locais, de acordo com as orientações éticas das respetivas comissões. Usamos dadores vivos respeitando todos os critérios bioéticos inerentes aos estudos de tecido humano conforme o Comité de Ética da Universidade do Minho. A população principal é constituída por dadores entre os cinquenta e setenta anos de vida com gonartrose unicompartimental. Neste estudo foram avaliados 26 meniscos externos (ME) e 23 meniscos internos (MI) obtidos de 41 dadores (10 masculinos e 31 femininos). Apenas meniscos morfologicamente intactos, sem antecedentes cirúrgicos foram incluídos e foram excluídos meniscos de compartimentos classificados radiologicamente como grau IV de Kellgren-Lawrence[93,94]. Cada menisco foi dividido em segmentos anterior, médio e posterior antes da avaliação mecânica, biológica ou histológica. Foi usada uma amostra humana de paciente com dezoito anos de idade com rutura aguda irreparável do menisco externo para controlo do fenótipo dos meniscócitos (i.e. células de articulação não artrósica).
Propriedades biomecânicas por segmentos do menisco humano em tecido fresco.
As propriedades viscoelásticas do menisco foram determinadas recorrendo ao equipamento TRITEC8000B DMA (Triton Technology, Reino Unido, Figura 5). Todas as análises foram realizadas a 37ºC. Antes de cada análise, diferentes porções do menisco foram obtidas como descrito na Figura 6. Assim, o menisco foi seccionado em três regiões: anterior, médio e posterior. Dentro da região de interesse, as amostras foram cortadas de forma a obter porções cilíndricas com cerca de 4 mm de diâmetro e 4 mm de espessura usando uma trefina de biópsia. Procedeu-se à uniformização do tamanho e geometria das amostras a serem testadas. De seguida, as amostras foram armazenadas em solução de PBS até ao momento da análise. Todos os ensaios foram realizados com as porções de menisco imersas em PBS, num reservatório deTeflon®. Depois de atingir o equilíbrio a 37ºC, as análises foram realizadas a uma frequência compreendida entre 0,1 e 10 Hz. Os ensaios foram também realizados sob amplitude de deformação constante (50 mm). Uma pequena pré-carga foi aplicada em cada amostra para garantir que a superfície das porções de menisco estavam em contacto com as placas de compressão, antes do teste.
Isolamento de subpopulações, avaliação do potencial condrogénico e caracterização da distribuição celular em 2D e 3D (em curso)
Diferentes populações celulares isoladas de meniscos humanos foram preparadas para análise por citometria de fluxo. As células, das diferentes populações, após tripsinização, foram marcadadas com anticorpos (CD31, CD34, CD44, CD45, CD73, CD90, CD105) ligados a diferentes fluorocromos (FITC - Isotiocianato de fluoresceína, PE - ficoeritrina, e APC - aloficocianina). Em resumo, as células foram incubadas durante 15 minutos, protegidas da luz, e à temperatura ambiente. Após este passo de incubação, as amostras foram lavadas, em PBS, por centrifugação e fixadas com formaldeído (1%). De seguida, os dados foram adquiridos num citómetro FACSCalibur e analisados utilizando o software CellQuest.
Tendo em conta a utilização a que nos propomos, na regeneração parcial ou total de menisco, estamos presentemente a avaliar celularidade e também o potencial condrogénico das células isoladas, recorrendo a meios de cultura já amplamente descritos na literatura, e disponíveis comercialmente, o que nos permite a padronização dos métodos utilizados em cultura celular, tendo sempre em mente a aplicabilidade clínica. Após 28 dias de cultura na presença de suplementos condrogénicos, e com a utilização de cultura em micromassa, avaliaremos a extensão da diferenciação com recurso a técnicas histológicas, como colorações (hematoxilina/eosina, safranina O, azul de toluidina) e técnicas de imunocitoquímica utilizando anticorpos anticolagénio tipo I e II, e agrecano. Estes resultados serão complementados através da quantificação dos glucosaminoglicanos sulfatados, e recorrendo a técnicas de PCR para a expressão de genes específicos de cartilagem (e.g., colagénio, proteína oligomérica da matriz da cartilagem (COMP) e agrecano).
Neste trabalho, temos também como objetivo (em curso) isolar células de tecido adiposo humano, tecido este obtido por liposucção em abdomenoplastias ou da bolsa de Hoffa, após consentimento informado de acordo com a legislação em vigor referente à proteção de dados. As células serão obtidas através de um processo de digestão enzimática com colagenase, e centrifugação, e em seguida o sedimento será plaqueado, e por adesão ao frasco de cultura, propriedade das células estaminais mesenquimais, como as presentes no tecido adiposo, obteremos a população inicial para estudo. Diferentes sobpopulações serão isoladas a partir da primeira fração recorrendo a métodos de seleção magnética. As células serão caracterizadas quanto à expressão de marcadores de superfície, referenciados para células estaminais mesenquimais. Serão efetuados ensaios de proliferação e viabilidade celular através da quantificação de ADN, e ATP.
No final desta tarefa, os resultados esperados são: (i) caracterização da celularidade das diferentes regiões que constituem o menisco, (ii) isolamento de células estaminais mesenquimais derivadas de tecido adiposo colhido de abdomenoplastias ou da bolsa de Hoffa; (iii) Caracterização das subpopulações isoladas; (iv) Avaliação do potencial condrogénico das células mesenquimais derivadas do tecido adiposo.
RESULTADOS E DISCUSSÃO
O presente estudo tem como principal objetivo a caracterização das propriedades mecânicas e celularidade das diferentes regiões que constituem o menisco, i.e. parte anterior, média e posterior (Figura 7). Estes resultados serão usados como padrão para futura diferenciação condrogénica de células estaminais obtidas da gordura humana (abdominal ou gordura de Hoffa) para estabelecer duas possíveis fontes celulares para uso terapêutico (células de tecido nativo ou células estaminais autólogas após diferenciação in vitro).
]]>
Da análise mecânica dinâmica (DMA) dos diferentes segmentos do menisco humano a fresco observamos (Figura 8) a seguinte tendência de crescente de rigidez: segmento anterior MI (0,25 MPa a 1Hz) <anterior ME< médio ME<posterior MI< posterior ME< médio MI (0,9 MPa a 1 Hz).
A análise de micro-CT do menisco liofilizado revelou uma porosidade média de 53%, espessura média das trabéculas igual a 80 µm e um tamanho de poros em média de 85 µm. A figura 9 mostra as imagem 2D de raios X do menisco liofilizado e a distribuição da espessura das trabéculas e tamanho de poros.
]]>
As células isoladas (Figura 10) das diferentes amostras incluem fibrocondrócitos (meniscócitos) e células estaminais mesenquimais.
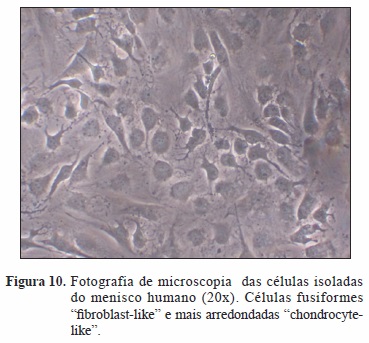
Foram analisadas diferentes populações celulares utilizando citometria de fluxo. A análise indica que as células expressam de forma heterogénea, i.e., intensidade de fluorescência média a alta, os seguintes marcadores: CD44, CD73, CD90, CD105. Quando analisada a percentagem de células positivas para os quatro marcadores referidos, os valores são superiores a 97,0%±1,5% (média ± erro padrão da média). As mesmas populações foram ainda analisadas para a expressão de CD31, CD34 e CD45, tendo os valores obtidos sido 1,8%±0,8%, 3,2%±1,0% e 0,2%±0,1%, respetivamente. Em duas das populações isoladas, foram analisadas duas passagens diferentes (P2 e P7), tendo-se verificado a manutenção dos marcadores analisados e respetivas percentagens de expressão. A figura 11 é uma representação dos resultados obtidos para as populações em estudo.
]]>
Este ensaio foi repetido com uma amostra de célula obtidas de um dador vivo com 18 anos de idade que sofreu rutura traumática complexa e irreparável do corpo e corno do menisco externo, operado 4 semanas após a lesão. Neste caso a articulação não apresentava qualquer alteração artrósica no plano clínico, radiológico, ressonância magnética ou avaliação artroscópica intraoperatória. Os resultados obtidos até nas análises efetuadas até ao momento foram sobreponíveis aos descritos para a população em estudo.
Por sua vez, a caracterização da distribuição celular em 2D e 3D, dos diferentes segmentos e regiões que constituem o menisco está neste momento a decorrer. Para tal, a celularidade (Figura 12) é determinada usando um método semiquantitaivo, e recorrendo a análise histológica do menisco (coloração H&E). Este estudo contempla um universo de 25 pacientes (18 meniscos externos e 7 meniscos internos). Sendo que destes uma parte foi avaliada apenas em 2D (n=15) e outra em 3D (n=10).
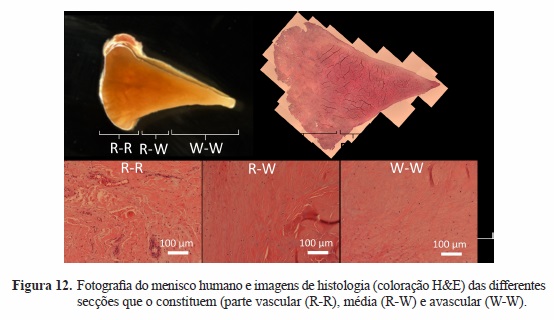
O uso de dadores com mais de cinquenta anos, com artrose em algum compartimento do joelho pode constituir uma fonte de viés. Contudo, existe suporte na literatura determinando que não existem alterações relevantes quer no respeitante a células[90], quer relacionados com a estrutura[89] de meniscos morfologicamente intactos obtidos desta fonte.
]]> Alguma diminuição da densidade celular é espectável com a idade[95] e não se exclui igualmente alguma alteração da biomecânica. Contudo, este estudo tem o mérito de avaliar, pela primeira vez, as propriedades biomecânicas em tecido humano fresco, obviando o viés inerente ao uso de material congelado[96,97] que altera significativamente as propriedades físicas do menisco[96-98].Foi possível obter neste modelo, de forma repetida e consistente, células viáveis e funcionantes com características de tecido meniscal normal semelhantes ao descrito na literatura[88,90]. As células de controlo obtidas de lesão aguda em paciente jovem confirmaram a preservação fenotípica da população principal tal como previamente descrito.
CONCLUSÕES
Este estudo contribuiu para um conhecimento mais profundo do menisco humano nomeadamente no que respeita às propriedades biomecânicas dos vários segmentos do menisco (sem processo de congelamento) e da sua biologia celular. Da análise mecânica dinâmica (DMA) dos diferentes segmentos do menisco humano observamos a seguinte tendência decrescente de rigidez: segmento anterior MI (0,25 MPa a 1Hz) <anterior ME< médio ME<posterior MI< posterior ME< médio MI (0,9 MPa a 1 Hz). As células isoladas das diferentes amostras incluem fibrocondrócitos e células estaminais mesenquimais (positivas para CD105, CD73 e CD90; negativas para CD34 e CD45). A densidade celular decresce da periferia (R-R) para o centro (W-W). Observou-se uma assimetria na celularidade entre os diferentes segmentos avaliados.
O modelo usado na manipulação das populações celulares permitiu obter de forma fiável e reprodutível células viáveis para aplicações em engenharia de tecidos.
Estes dados acrescentam desde já conhecimento relevante sobre este tecido com o objetivo de desenvolver novas e mais eficazes abordagens visando a regeneração parcial/total do menisco mas os trabalhos em curso neste capítulo poderão abrir ainda novas perspetivas.
4. NOVA MATRIZ TRIDIMENSIONAL POROSA PARA ABORDAGEM CELULAR E ACELULAR EM ENGENHARIA DE TECIDOS DO MENISCO: ENSAIO IN VITRO (INVESTIGAÇÃO ORIGINAL)
]]> INTRODUÇÃO
Reconhecendo algumas das limitações descritas para as scaffolds em aplicação clínica e mesmo préclínica com base na revisão sistemática da literatura efetuada (falência precoce de integração, diminuição progressiva do volume, tecido final diferente de fibrocartilagem - capítulo 2), e considerando os parâmetros mínimos do ponto de vista biomecânico e biológico resultantes do trabalho descrito no capítulo 3, avançamos no desenvolvimento de uma nova opção com um novo biomaterial que pudesse estabelecer vantagens do ponto de vista da estabilidade, propriedades mecânicas e biocompatibilidade.
A fibroína de seda obtida do bicho da seda tem vindo a ser explorada como biomaterial para a produção de scaffolds. A arquitetura e as propriedades mecânicas de uma matriz tridimensional porosa são variáveis determinantes no controlo da formação/regeneração de tecido[99], tal como o são a disponibilidade de meio adequado (incluindo fatores de crescimento) e a pressão hidrostática[100,101] particularmente se estamos a lidar com cartilagem (o que justifica o papel dos bioreactores nos estudos in vitro)[102].
Por esse motivo, considerando as características físicas do tecido humano previamente descritas e os resultados dos nossos estudos proposemo-nos testar scaffolds de fibroína da seda (produzida pelo bicho da seda Bombyx mori) a 10 e 12% para aplicação em abordagens de Engenharia de tecidos de menisco (Figura 13).
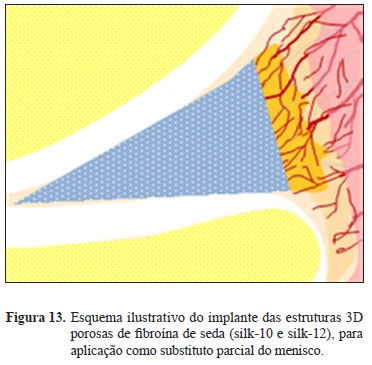
MATERIAL E MÉTODOS
]]> Produção e caracterização das estruturas tridimensional (3D) porosas baseada em seda para reparação parcial/total de defeitos meniscaisAs estruturas 3D porosas (scaffolds) foram produzidas utilizando como matéria-prima a seda, com diferentes concentrações. As estruturas tridimensionais porosas foram obtidas recorrendo ao método de processamento através da mistura e lixiviação de sais (cloreto de sódio). A fibroína de seda será preparada conforme descrito anteriormente por Leping Yan et al.103 A solução de fi broína de seda será diluída para obtermos as soluções com as seguintes concentrações: 10% e 12% (% em massa). As estruturas foram moldadas utilizando um tubo de silicone, e secas à temperatura ambiente durante 48 horas. Os tubos foram depois imersos em água destilada e o sais de cloreto de sódio extraídos por vários dias. As estruturas foram posteriormente congeladas a -80°C e liofilizadas.
A estabilidade das estruturas (% perda de massa) produzidas foi avaliada, in vitro. Este estudo foi realizado ao longo de trinta dias, por imersão dos suportes em tampão salino (PBS), a pH fisiológico (7,4). A morfologia da superfície e propriedades mecânicas das estruturas após cada tempo de imersão foram analisadas.
As estruturas produzidas foram caracterizadas utilizando testes de compressão dinâmica (DMA) em condições húmidas (PBS, pH 7,4) e testes de compressão em estado seco, utilizando para estes últimos ensaios uma máquina de ensaios universal (Instron 4505) com célula de carga 1 kN à temperatura ambiente. Para além dos testes referidos, foram utilizadas outras técnicas de cracterização complementares como seja a microtomografia de raios-X (micro-CT) e microscopia eletrónica de varrimento (SEM).
Avaliação da toxicidade e cultura de células de menisco humano na matriz tridimensional de seda (in vitro)
Os estudos de biocompatibilidade correspondem a uma das etapas da caracterização das estruturas porosas tridimensionais, independentemente da sua micro ou macro-porosidade, e consequentemente, determinar a adequação ao uso pretendido, ou seja, irá determinar se as scaffolds devem seguir para as próximas fases de teste (em ensaios in vivo, e préclinicos) ou se é necessário voltar atrás e otimizar alguns parâmetros. Procedeu-se à cultura e expansão das células do menisco em frascos de cultura até atingiram 70-80% de confluência, e nessa altura foram então transferidas para as estruturas 3D produzidas, e a cultura continuada, quer em condições de expansão quer em condições de diferenciação condrogénica. A proliferação celular e vialibidade foram testadas recorrendo a testes padronizados. A caracterização das estruturas híbridas (scaffold com células) foi caracterizada recorrendo ao ensaio calceína-AM e será também realizada utilizando espectroscopia (SEM). A diferenciação condrogénica (estudo a decorrer) será avaliada com a quantificação de glicosaminoglicanos (GAGs), técnicas histológicas para a imunolocalização de colagénio tipo I e II. Sendo a caracterização complementada pela determinação da expressão de genes específicos para cartilagem como Sox9, colagénio tipo I, II e X, COMP e agrecano utilizando técnicas de PCR.
RESULTADOS E DISCUSSÃO
Foram avaliadas as propriedades mecânicas, arquitetura e performance biológica das scaffolds de fibroína de seda (Figura 14) produzidas a partir de diferentes concentrações iniciais de seda (10% e 12% em massa).
]]>

Quanto à análise de DMA constatamos um aumento do módulo com o aumento da concentração de fibroína de seda. Durante os testes, observou-se uma variação dos módulos de 37,6 ± 1,7-77,9 ± 4,4 kPa e 158,0 ± 16,8-264,1 ± 26,8 kPa, para silk-10 e silk-12, respetivamente (Figura 15). Comparando os módulos do menisco humano 250-900 kPa, (capítulo 3) pode afirmar-se que as scaffolds são adequadas para aplicação em abordagens de engenharia de tecidos de menisco.
As imagens de microscopia eletrónica de varrimento revelaram que as estruturas desenvolvidas são altamente porosas e interconectivas (Figura 16), apresentando também macro- e micro-poros.
]]>
A porosidade total, interconectividade e tamanho de poros das scaffolds foram determinadas através da técnica micro-CT. Com o aumento da concentração fibroína de seda de 10% para 12%, verificou-se uma diminuição da porosidade média de 89% para 87% (Figura 17). Por outro lado verificou-se que a interconectividade também diminuiu de ~97% para 95%. No entanto, a espessura das trabéculas e tamanho de poros não variou significativamente, i.e., 60 µm para silk-12 e 58 µm para silk-10, sendo que o tamanho médio de poros está compreendido entre 200 e 300 µm, o que é favorável para a cultura e proliferação celular.104
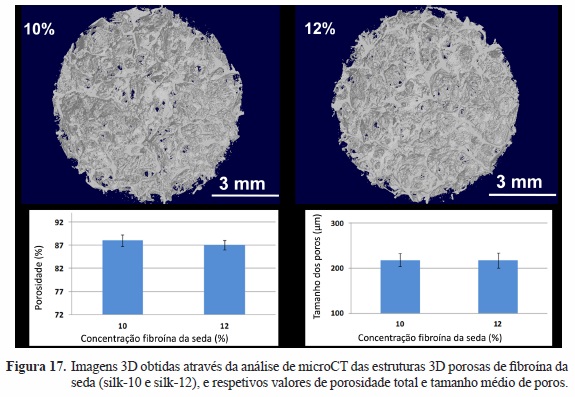
Os ensaios de degradação realizados numa solução tampão salina de fosfato (pH 7,4 e T=37ºC) revelaram que as scaffolds apresentam uma estabilidade favorável, i.e., a sua estrutura, morfologia e propriedades mecânicas foram mantidas após 30 dias (Figura 18).
]]>
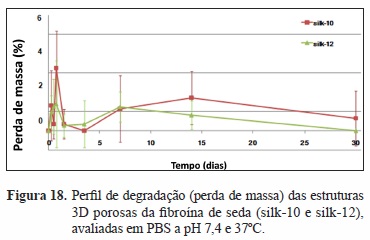
A avaliação da performance biológica das scaffolds propostas para a engenharia de tecidos de menisco foi estudada in vitro. Fibroblastos de pulmão de ratinho (células L929) foram cultivadas na presença das substâncias lixiviáveis libertadas das scaffolds produzidas (10 e 12%). O ensaio MTS foi realizado após 1, 3 e 7 dias de cultura (Figura 19).
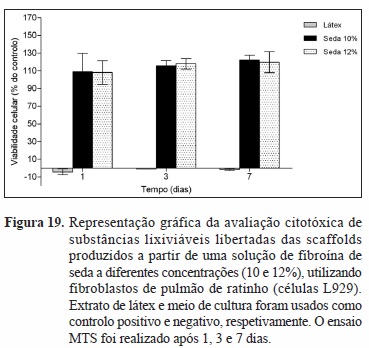
Os resultados mostraram que as scaffolds não apresentam qualquer efeito citotóxico.
Por sua vez, a viabilidade celular foi investigadacultivando células isoladas do menisco humano na superficie das scaffolds e realizando um ensaio de calceína-AM (Figura 20).
]]>
O ensaio revelou um aumento de fluorescência com o aumento do tempo de cultura, o que demonstra a capacidade das scaffolds em suportar a adesão e proliferação das células do menisco.
CONCLUSÕES
O presente estudo descreve a caracterização físico-química das estruturas 3D de fibroína de seda produzidas a partir de concentrações elevadas de diferentes soluções aquosas de fibroína de seda. A macro- e micro-porosidade das estruturas foi obtida recorrendo aos métodos de lixiviação de sal e liofilização. O estudo da arquitetura 3D das scaffolds de fibroína de seda mostrou que estas estruturas possuem elevada porosidade e interconectividade, diminuindo a sua percentagem com o aumento da concentração de fibroína de seda. Os ensaios de compressão e análise de DMA revelaram que as propriedades mecânicas das estruturas aumentaram drasticamente com o aumento da concentração de fibroína de seda. Por outro lado, os ensaios de degradação in vitro também mostraram que as scaffolds mantêm a sua estrutura e morfologia, bem como suas propriedades mecânicas originais, após 30 dias de imersão. Os ensaios de caracterização biológica provaram que as scaffolds não apresentam qualquer efeito citotóxico e suportam a adesão e viabilidade de células do menisco, in vitro. É possível desenvolver estruturas com propriedades mecânicas mais elevadas (módulo 399,2±19,6-630,3±49,8 kPa) usando soluções de fibroína de seda até 16%. Portanto, as scaffolds de fibroína de seda propostas são boas candidatas para encontrarem aplicações em abordagens de engenharia de tecidos do menisco.
5. IMPORTÂNCIA DA NEOVASCULARIZAÇÃO/INERVAÇÃO: APLICAÇÃO DO HIDROGEL DE GOMA GELANA METACRILADA NA MATRIZ DE FIBROÍNA DE SEDA COMO UMA NOVA ABORDAGEM PARA PREVENIR NEOVASCULARIZAÇÃO/INERVAÇÃO E DEFENDER AS PROPRIEDADES BIOMECÂNICAS PELA PRESERVAÇÃO DO FENÓTIPO DOS FIBROCONDRÓCITOS (INVESTIGAÇÃO ORIGINAL)
]]>INTRODUÇÃO
Considerando a especificidade e características biológicas e funções do tecido em apreço, propusemos uma nova abordagem por Engenharia de Tecidos na substituição do menisco.
Nos estudos publicados estão registados casos de falência precoce de integração, diminuição do volume do tecido final ou desintegração. Além disso, o tecido obtido não é fibrocartilagem mas um híbrido com algumas semelhanças.
Assim sendo a hipótese é de que se pudermos, sem prejudicar a estabilidade do implante, favorecer a neovascularização na zona periférica da scaffold de fibroína de seda poderemos facilitar a adesão e integração inicial do implante (Figura 21). Na mesma perspetiva seria vantajoso inibi-la nas zonas mais centrais, onde se privilegia a preservação fenotípica dos meniscócitos que produzem a matriz extracelular responsável pelas propriedades mecânicas, eventualmente aproximando o tecido final à fibrocartilagem característica do menisco. Além disso, apesar de não estar cabalmente demonstrado é verosímil que a invasão vascular das zonas mais centrais possa ter efeito nocivo nas propriedades mecânicas e que seja acompanhada por proliferação de nocireceptores.
Recentemente descrevemos um hidrogel à base de goma gelana com propriedades barreira e nãoangiogénico, o qual permite inibir a infiltração de células endoteliais e de vasos sanguíneos. Na mesma perspetiva seria vantajoso combinar o hidrogel de goma gelana com a nossa scaffold, por forma a ser possível prevenir a neovascularização nas zonas mais centrais, e desta forma mimetizar o tecido final à estrutura do menisco. Considerando as propriedades mecânicas das scaffolds desenvolvidas (capítulo 4), foi seleccionda a scaffolds de fi broína de seda 12% (silk- 12) como a mais promissora, e como tal a ser avaliada no presente estudo.
]]> Ao contrário de outros modelos desenvolvidos para o estudo da angiogénese in vivo, o ensaio da membrana corio-alantoide (CAM) de ovos de galinha é um teste simples e viável para testes envolvendo um grande número de amostras. Além disso, não requer um biotério, e portanto, não é caro. Este método tem sido também aplicado no estudo da resposta angiogénica e infl amatória de biomateriais. Assim, o presente estudo consiste na avaliação das propriedades de barreira do hidrogel de goma gelana quando combinada com a scaffold de fibroína de seda 12%, recorrendo ao ensaio CAM.
MATERIAL E MÉTODOS
Ensaio da membrana corio-alantoide (CAM) de ovos de galinha
Ovos férteis de galinha (n=90-120; Pintobar, Portugal) foram incubados a 37ºC (Laboratory Incubator Series 8000; Termaks, Norway) durante 3 dias. Após este período foi criado uma pequena abertura na extremidade pontiaguda do ovo, com o objetivo de permitir a dissociação da CAM da membrana da casca do ovo. Foi igualmente cortada uma janela circular na casca (com um máximo de 15 mm de diâmetro) a fim de avaliar a viabilidade do embrião e permitir o acesso à CAM (Figura 22). Este processo foi realizado numa câmara de fluxo laminar para minimizar o risco de contaminação. A abertura na casca foi selada com fita adesiva transparente (aproximadamente 50×30 mm; BTK, Portugal) para evitar a desidratação e os ovos foram novamente incubados a 37ºC até o dia 10 do desenvolvimento embrionário.
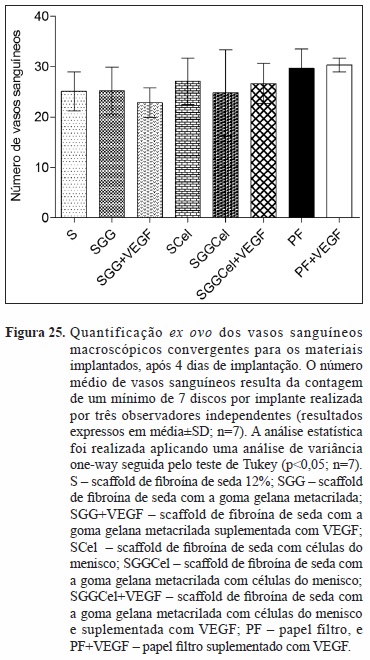
Discos estéreis (n=7) com um diâmetro de 4 mm e altura de 3 mm foram implantados na CAM ao 10º dia de desenvolvimento embrionário em condições estéreis. Seis grupos experimentais foram testados: discos de 1) seda a 12% (S), 2) seda a 12%+iGGMA (SGG), 3) seda a 12%+iGG-MA+VEGF (SGG+VEGF), 4) seda a 12%+células do menisco (SCel), 5) seda a 12%+iGG-MA+células do menisco (SGGCel) e 6) seda a 12%+iGG-MA+células do menisco+VEGF (SGGCel+VEGF). Foram igualmente preparados discos de papel de filtro (PF) com um diâmetro de 4 mm, esterilizados em autoclave e implantados na CAM ao 10º dia de desenvolvimento embrionário (n=7). O papel de filtro estéril foi colocado diretamente sobre a CAM e serviu como controlo, com ou sem a adição de 100 ng de VEGF (PF+VEGF e PF). A abertura na casca foi protegida com fita adesiva transparente e os ovos novamente incubados a 37ºC até ao 14º dia de desenvolvimento embrionário. Após dois dias foi adicionado 100 ng de VEGF ao grupo controlo PF+VEGF e aos restantes grupos experimentais contendo VEGF, emcondições estéreis. As imagens dos implantes na CAM foram obtidas in ovo no final do ensaio utilizando uma câmara digital Olympus DP71 (Olympus, EUA) conectada ao software básico de imagem CellB (Olympus, EUA) acoplada a um microscópio estereoscópico Olympus SZX16 (Olympus, EUA). Os embriões e respetivas membranas foram então fixados in ovo por adição de um pequeno volume de uma solução fresca de paraformaldeído (PFA; Merck, Alemanha) a 4% (v/v), seguida de incubação a -80°C durante 10 minutos. Os materiais implantados e as porções da CAM imediatamente subjacentes foram dissecadas e transferidas para placas de 12 poços contendo solução de PFA a 4% (v/v). As imagens ex ovo foram então capturadas para cada implante na CAM. As membranas excisadas foram transferidas para cassetes histológicas, incluídas em parafina e seccionadas (Rotary Microtome HM 325; Microm, Alemanha) para análise imuno-histoquímica.
]]> Quantificação de vasos sanguíneos convergentesA avaliação macroscópica da resposta angiogénica foi efetuada utilizando um método semiquantitativo, por análise da convergência de vasos sanguíneos para os discos implantados, in ovo e ex ovo, de acordo com o descrito por Ribatti et al[105] As imagens in ovo e ex ovo obtidas ao 14º dia de desenvolvimento embrionário foram processadas utilizando o software WCIF ImageJ (EUA National Institutes of Health, EUA) para facilitar a contagem do número total de vasos sanguíneos que convergiam para o disco implantado. Para efeitos de quantificação, a ampliação das imagens estereomicroscópicas foi mantida constante (7x), bem como a área da imagem processada (1000 x 1000 pixels). O número total de micro-vasos macroscópicos que convergiam para o implante foi quantificado para cada ovo por três observadores independentes.
Coloração de hematoxilina-eosina
Secções da CAM com 3 µm de espessura foram coradas com H&E. Os cortes histológicos sagitais das amostras foram observados por microscopia através de um microscópio ótico Axio Imager.Z1m (Zeiss, Alemanha) associado a uma câmara digital AxioCam MRC5 (Zeiss, Alemanha) conectada ao software de processamento de imagem AxioVision (Zeiss,Alemanha).
Análise imuno-histoquímica
A análise imuno-histoquímica foi efetuada em secções representativas (de espessura 3 µm) da CAM contendo o material implantado, com base no sistema estreptavidina-biotina-peroxidase (UltraVision Large Volume Detection System Anti-Polyvalent, HRP; LabVision Corporation, EUA). Resumidamente, a parafina foi removida dos cortes da CAM e as lâminas re-hidratadas foram submetidas ao calor para induzir a recuperação antigénica em tampão citrato 10 mM (pH 6,0; Merck, Alemanha) durante 20 minutos e a 98ºC. De forma a inativar as peroxidases endógenas, as lâminas foram incubadas numa solução de peróxido de hidrogénio a 3% (v/v) (PanreacQuímica SAU, Espanha) durante 10 minutos, e seguidamente imersas em PBS. As secções da CAM foram então submetidas a um período de incubação em solução bloqueadora de proteína por 10 minutos, seguido de incubação com o anticorpo primário específico para a lectina (SNA, EBL), durante 1 hora e à temperatura ambiente. Finalmente, os cortes foram lavados sequencialmente com PBS e incubadas com o complexo estreptavidinaperoxidase durante 10 minutos. A reação imunológica foi visualizada utilizando 3,3’-Diaminobenzidina (DAB; Thermo Scientific, EUA) como cromógeno. A contracoloração foi efetuado com solução de hematoxilina de Gill-2 (Merck, Alemanha) em todos os cortes. Para preparar o controlo negativo foi omitido o anticorpo primário, enquanto que para o controlo positivo foi utilizada apenas a membrana corio-alantoide. As imagens das secções histológicas da CAM foram obtidas utilizando uma câmara digital AxioCam MRc5 (Zeiss, Alemanha) conectada ao software de processamento de imagem AxioVision (Zeiss, Alemanha) acoplada a um microscópio ótico AxioImager.Z1m (Zeiss, Alemanha).
Análise estatística
A análise estatística foi realizada aplicando uma análise de variância one-way seguida pelo teste de comparação múltipla de Tukey (p<0,05; n=7) usando o software GraphPadPrism (GraphPad Software Inc., EUA). O critério de significância estatística utilizado foi um valor de p<0,05 para um intervalo de confiança de 95% (*** p<0,001; ** p<0,01; * p<0,05).
RESULTADOS E DISCUSSÃO
]]> A figura 23 mostra as fotografias (in ovo) de estereomicroscopia da secção da CAM correspondente aos diferentes materiais implantados, após 4 dias de implantação. A partir da figura é possível observar que as scaffolds foram parcialmente encapsuladas. No entanto, não se observou qualquer indício macroscópico de degradação ou absorção do material. Também não foi observada a formação de tecido de granulação, o que é uma indicação de que os materiais não despoletaram uma reação inflamatória.
Por sua vez, a figura 24 mostra as fotografias (ex ovo) de estereomicroscopia da secção da CAM correspondente aos diferentes materiais implantados, após 4 dias de implantação. Estas imagens foram processadas para determinar o número de vasos sanguíneos macroscópicos convergentes para os implantes.
]]> A figura 25 mostra a quantificação de vasos sanguíneos (ex ovo) macroscópicos. Três diferentes observadores procederam á análise das imagens. É possível observar que não há diferenças significativas na formação de vasos sanguíneos macroscópicos induzida pelos implantes quando comparado com o controlo positivo de angiogénese (Papel filtro, PF).
A figura 26 mostra as imagens de microscopia ótica das secções sagitais da CAM excisada após coloração com hematoxilina e eosina (H&E) correspondentes aos materiais implantados. A figura 6.6A e D corresponde aos implantes de fibroína de seda 12%, com e sem células do menisco. A partir das imagens é possível observar uma infiltração celular massiva da CAM, ocupando os poros da scaffold, da periferia para o centro. Por sua vez, a figura 6.6B, C, E e F corresponde aos implantes de seda (12%) modificados com o hidrogel goma gelana metacrilada (iGG-MA). As figuras mostram que o hidrogel inibiu a infiltração celular a partir da CAM.
]]> A figura 27 corresponde às imagens de microscopia ótica da coloração imuno-histoquímica (Lectina- SNA, especifica para as células endoteliais), das secções sagitais da CAM excisada correspondentes aos materiais implantados. Foi possível verificar que a adição de VEGF às scaffolds promove quer a migração de células endoteliais (setas) para a CAM quer a formação do microcapilares. Por sua vez, estes resultados mostraram que a adição da goma gelana modificada (com e sem células do menisco humano) às scaffolds de fi broína de seda inibiu a infiltração de células endoteliais e de vasos sanguíneos para o interior das scaffolds a partir da CAM.
Estes resultados demonstram que o hidrogel de goma gelana modificada é capaz de prevenir, pelo menos durante o período de implantação, ambas infiltração celular e de vasos sanguíneos para o interior da scaffold. Esta abordagem na engenharia de tecidos do menisco é uma estratégia inovadora para o controlo da neovascularização na scaffold, i.e., permite a neovascularização na zona periférica da scaffold de fibroína de seda e promove a sua inibição nas zonas mais centrais.
CONCLUSÕES
O estudo in vivo, demonstro que o desenvolvimento de uma scaffold de fibroína de seda combinada com um hidrogel de goma gelana modificada permite-nos controlar a neovascularização na zona periférica da scaffold e promover a sua inibição nas zonas mais centrais. Apesar disso, será necessário a realização de mais estudos, de forma a ser possível avaliar a performance biológica destas scaffolds, no que respeita à manutenção do fenótipo dos meniscócitos, tanto in vitro como in vivo. Apesar disso, esta é uma abordagem pioneira e que nos possibilitará desenvolver implantes “inteligentes” por forma a mimetizar o tecido final regenerado à fibrocartilagem característica do menisco.
]]> 6. ENSAIOS IN VIVO: TRABALHO FUTURO (DESENHO DE ESTUDO)
INTRODUÇÃO
Diferentes modelos animais têm sido propostos para avaliar o potencial de reparação do tecido meniscal[106]. Estes compreendem abordagens que vão desde a regeneração de um defeito com perda mínima de tecido (por exemplo, suturas, colas biológicas) ou após perda de uma grande parte do tecido a integração de suportes concebidos para substituição de tecidos. Tais modelos devem reproduzir não só o ambiente biológico em estudo, mas também a terapêutica necessária e as condições cirúrgicas. A escolha do modelo animal para a situação em estudo depende de diversos fatores: (1) a biologia e anatomia do modelo animal, (2) a idade do modelo animal, o que afeta o seu metabolismo, e (3) o potencial de regeneração espontânea do modelo em estudo.
MATERIAL E MÉTODOS
Implantação subcutânea no rato Fischer 344
Esta etapa do trabalho tem por objetivo a avaliação da biocompatibilidade e biodegradação das diferentes scaffolds de fibroína da seda num modelo de rato Fischer 344(implantação subcutânea). Após 1, 4 e 8 semanas, secções dos implantes serão preparadas para análise histológica (coloração H&E e imunohistoquimica) visando avaliar: (i) reação inflamatória (presença de células polimorfonucleares, mononucleares e células multinucleadas será investigada através da técnica de imunofluorescência: ED1; Serotec, Oxford, Reino Unido), (ii) formação de tecido de granulação e fibrose, (iii) infiltração celular e formação de vasos sanguíneos. A caracterização da microestrutura e evidências de degradação dos materiais será avaliada através da microscopia eletrónica de varrimento (SEM). As propriedades mecânicas das scaffolds serão determinadas recorrendo à análise mecânica dinâmica (DMA).
Modelo de regeneração de defeito parcial em modelo de grande animal (ovelha)
Há evidências de que as principais características estruturais que influenciam a regeneração do menisco humano são bem reproduzidas em animais da raça bovina, lagomórfica, ovina e caprina[49,106,107]. A raça ovina/caprina permite a utilização de técnicas de correção cirúrgica artroscópica semelhantes aos utilizados rotineiramente em humanos. Considerando todos os fatores optamos por um modelo utilizando ovinos adultos. Neste estudo, o defeito de menisco, em estudo, será artificialmente induzido com um procedimento cirúrgico que consiste na remoção mecânica, artroscópica, do menisco (deixando parte dos ligamentos do corno anterior e posterior). Uma comparação lado-a-lado será usada para superar avaliações condicionadas.
]]> Diferentes abordagens terapêuticas serão aplicadas nos joelhos direitos traseiros de diferentes indivíduos. Três condições serão estudadas: (i) defeito induzido (DI) sem qualquer intervenção no joelho, que serve de controlo como defeito vazio às outras condições, e que pretende a avaliar a possibilidade remota de regeneração espontânea; (ii) reparação do DI por substituição do menisco por uma estrutura acelular com suturas; (iii) a regeneração do DI utilizando uma estrutura híbrida (células-scaffolds) para comparar com os scaffolds acelulares previamente implantados em ii). Apenas um dos joelhos é intervencionado para garantir o bem-estar dos animais e sucesso do modelo proposto. No final do estudo, e de acordo com a legislação em vigor, todos os animais serão eutanasiados. As diferentes abordagens serão avaliadas depois de 3, 6 e 12 meses da cirurgia:1. Defeito induzido (DI) (Figura 28) sem qualquer outra atitude complementar no joelho direito – aferir possibilidade de regeneração espontânea e colher células de menisco para aplicação na scaffold in vitro.
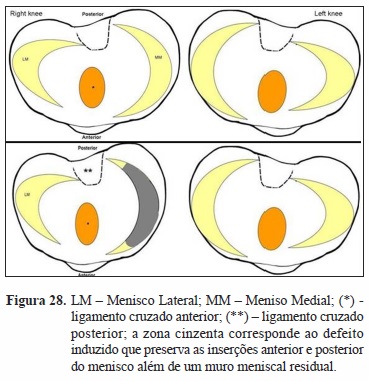
2. Comparação entre evolução crónica (e.g., 3 meses) da reparação do DI por scaffold acelular suturada in situ, e evolução no mesmo tempo do DI não reparado (Figura 29).
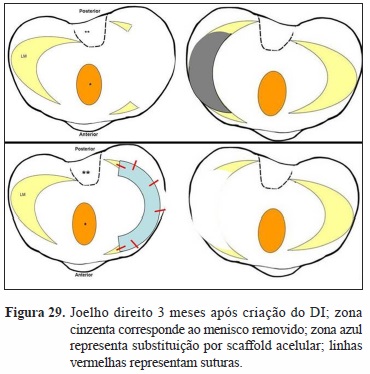
3. Comparação entre os resultados obtidos com scaffolds acelulares e scaffolds associadas a células (estaminais e/ou meniscócitos)
O comportamento de biocompatibilidade das estruturas 3D porosas com ou sem células serão avaliadas por radiografia, micro-CT, imagens de ressonância magnética e histologia. As estruturas implantadas, tanto a híbrida como a acelular, serão avaliadas utilizando procedimentos padrão para coloração histológica (hematoxilina/eosina, safranina-O, tricromo de Masson).
Os membros da equipa realizarão todos os ensaios de acordo com a legislação em vigor, no que se refere ao bem-estar animal, e são certificados pela Direção Geral de Veterinária para realizarem experimentação animal.
No final desta tarefa, esperamos demonstrar o desempenho das estruturas 3D porosas, in vivo, quer numa abordagem celular quer numa abordagem acelular para a regeneração parcial ou total de menisco e está já estabelecida a sua realização em colaboração com a Faculdade de Veterinária da Universidade de Trás-os-Montes e Alto Douro; Universidade Claude Bernard Lyon 1 (França); e Universidade Autonoma de Barcelona (Espanha), durante o ano civil de 2012.
CONCLUSÕES DO TRABALHO PRODUZIDO
Apesar dos resultados obtidos e dos avanços deles inerentes, o trabalho aqui apresentado, muito mais do que um objetivo alcançado, representa o início de um percurso.
Do reconhecimento do problema clínico e das dificuldades diárias no seu tratamento resultou uma necessidade de uma nova abordagem à luz da tríada básica da Engenharia de Tecidos (i.e., células, scaffolds e sinais moduladores da função celular como fatores de crescimento ou agentes externos - Figura 30).
]]>
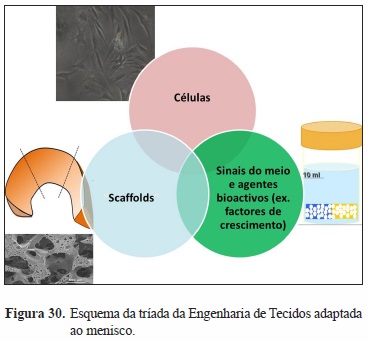
O investimento na investigação na área da Engenharia de Tecidos e Medicina Regenerativa (ETMR) aplicados ao modelo de reparação do menisco humano obriga ao conhecimento do estado da arte (capítulo 2). Durante essa pesquisa ficou inequivocamente comprovado que existe um consenso crescente na comunidade científica que apenas com a aproximação dos Ortopedistas a áreas do conhecimento geralmente descritas como Ciências Básicas (sendo que o epíteto de básico só se aceita como “fundamento”) é legítimo esperar a implementação futura de novas abordagens terapêuticas válidas. Por outro lado estas novas áreas do conhecimento prometem influenciar decisivamente a forma de praticar Medicina no futuro.
Ficou ainda estabelecido que os modelos de ETMR já testados clinicamente no tratamento dos defeitos do menisco estão desde já em discrepância com os modelos de investigação in vivo, em que se vêm testando novas possibilidades. Apesar dos esforços mais recentes existem ainda muitos aspetos da Biologia do menisco humano por esclarecer o que esteve na génese dos trabalhos efetuados (ou ainda em curso) apresentados no capítulo 3. Por outro lado, foi sentida a necessidade de testar a efetiva capacidade de, com os recursos disponíveis, montar e testar um “modelo” reprodutível de recolha de células e induzir a sua proliferação numa nova matriz tridimensional porosa com características adequadas.
Esse aspeto foi alcançado como demonstram os resultados aqui reproduzidos. Conseguimos montar um modelo viável e reprodutível com uma nova scaffold adaptada às propriedades físicas do menisco e em que as células de menisco humano permanecem viáveis.
Neste processo as células têm de preservar a capacidade de produzir a matriz extracelular que confere as características mecânicas essenciais do menisco e também esta capacidade tem de ser "afinada" e controlada.
Por outro lado este tecido não é homogéneo, tem variações da periferia para o centro e entre os diferentes segmentos (como estabelecido na literatura e reforçado pelos resultados apresentados). Assim, dificilmente poderá ser eficazmente replicado com recurso a um processo de "simples" substituição por uma matriz homogénea que não considera todas as variáveis da ETMR.
Este facto, conjugado com as descrições de que o tecido final resultante dos efeitos do processo de regeneração no ser humano sobre uma matriz acelular (colagénio ou poliuretano) não segue os mesmos parâmetros do tecido normal, levou-nos ao desenvolvimento da seguinte hipótese: se formos capazes de influenciar a neovascularização durante este processo podemos contribuir decisivamente para a melhoria do tecido final.
Desde já conseguimos demonstrar que é possível controlar in vitro a separação no construct (scaffold com células) entre áreas em que a revascularização é possível e facilitada, de outras em que é limitada ou impedida favorecendo aí a proliferação apenas dos meniscócitos. Decorre igualmente deste facto a possível influência no processo de adesão e integração do construct à área do defeito. Estas novas hipóteses serão testadas nos ensaios in vivo.
]]> Considerando todos estes aspetos, podemos resumir este trabalho da seguinte forma: (i) reconhecemos a relevância do problema; (ii) reunimos e hierarquizamos o conhecimento científico existente e reconhecemos limitações das estratégias em desenvolvimento; (iii) estudamos o tecido alvo para conhecermos as características a replicar e testar se seríamos capazes de manipular as suas células; (iv) construímos, com base no conhecimento adquirido, um novo modelo (novos biomateriais e nova possibilidade de regeneração heterogénea do tecido controlando a neovascularização); (v) reunimos conhecimento suficiente para testar a nossa hipótese num modelo animal; (vi) algumas fases do estudo estão ainda em curso e refletem as novas necessidades que emergem do trabalho efetuado e dos resultados entretanto obtidos.
REFERÊNCIAS BIBLIOGRÁFICAS
1. Hall MJ, Lawrence L. Ambulatory Surgery in the United States, 1996. Vital and Health Statistics of the Centers for Disease Control and Prevention/National Center for Health Statistics. 1998. p. 1-16. [ Links ]
2. Garrett WE Jr, Swiontkowski MF, Weinstein JN. American Board of Orthopaedic Surgery Practice of the Orthopaedic Surgeon: Part-II, certification examination case mix. J Bone Joint Surg Am. 2006; 88: 660-667 [ Links ]
3. Ait Si Selmi T, Fithian D, Neyret P. The evolution of osteoarthritis in 103 patients with ACL reconstruction at 17 years follow-up. Knee. 2006; 13: 353-358 [ Links ]
4. Fayard JM, Pereira H, Servien E, Lustig S, Neyret P. Meniscectomy Global results-Complications. Berlin, Heidelberg: Springer-Verlag; 2010. [ Links ]
5. Bolano LE, Grana WA. Isolated arthroscopic partial meniscectomy. Functional radiographic evaluation at five years. Am J Sports Med. 1993; 21: 432-437 [ Links ]
6. Annandale T. An Operation for Displaced Semilunar Cartilage. Br Med J. 1885; 1: 779 [ Links ]
7. King D. The function of semilunar cartilages. Journal of Bone and Joint Surgery American. 1936; 18: 1069-1076 [ Links ]
8. Fairbank TJ. Knee joint changes after meniscectomy. J Bone Joint Surg Br. 1948; 30B: 664-670 [ Links ]
9. Smillie IS. Injuries of the knee joint. 4th. Edinburgh: Churcill Livingstone; 1972. [ Links ]
10. Ghormley RK. Late joint changes as a result of internal derangements of the knee. Am J Surg. 1948; 76: 496-501 [ Links ]
11. Neyret P, Walch G, Dejour H. [Intramural internal meniscectomy using the Trillat technic. Long-term results of 258 operations]. Rev Chir Orthop Reparatrice Appar Mot. 1988; 74: 637-646 [ Links ]
12. McGinity JB, Geuss LF, Marvin RA. Partial or total meniscectomy: a comparative analysis. J Bone Joint Surg Am. 1977; 59: 763-766 [ Links ]
13. Takagi K. Practical experience using Takagi?s arthroscope. J Jpn Orthop Assoc. 1933; 8: 132 [ Links ]
14. Watanabe M. Arthroscopy: the present state. Orthop Clin North Am. 1979; 10: 505-522 [ Links ]
15. Jackson RW, Abe I. The role of arthroscopy in the management of disorders of the knee. An analysis of 200 consecutive examinations. J Bone Joint Surg Br. 1972; 54: 310-322 [ Links ]
16. Jackson RW, Rouse DW. The results of partial arthroscopic meniscectomy in patients over 40 years of age. J Bone Joint Surg Br. 1982; 64: 481-485 [ Links ]
17. Bergstrom R, Hamberg P, Lysholm J, Gillquist J. Comparison of open and endoscopic meniscectomy. Clin Orthop Relat Res. 1984; 133-136 [ Links ]
18. Northmore-Ball MD, Dandy DJ, Jackson RW. Arthroscopic, open partial, and total meniscectomy. A comparative study. J Bone Joint Surg Br. 1983; 65: 400-404 [ Links ]
19. Simpson DA, Thomas NP, Aichroth PM. Open and closed meniscectomy. A comparative analysis. J Bone Joint Surg Br. 1986; 68: 301-304 [ Links ]
20. Tregonning RJ. Closed partial meniscectomy. Early results for simple tears with mechanical symptoms. J Bone Joint Surg Br. 1983; 65: 378-382 [ Links ]
21. Kurosawa H, Fukubayashi T, Nakajima H. Load-bearing mode of the knee joint: physical behavior of the knee joint with or without menisci. Clin Orthop Relat Res. 1980; 283-290 [ Links ]
22. McDermott ID, Amis AA. The consequences of meniscectomy. J Bone Joint Surg Br. 2006; 88: 1549-1556 [ Links ]
23. Levy IM, Torzilli PA, Warren RF. The effect of medial meniscectomy on anterior-posterior motion of the knee. J Bone Joint Surg Am. 1982; 64: 883-888 [ Links ]
24. Walker PS, Hajek JV. The load-bearing area in the knee joint. J Biomech. 1972; 5: 581-589 [ Links ]
25. Bourne RB, Finlay JB, Papadopoulos P, Andreae P. The effect of medial meniscectomy on strain distribution in the proximal part of the tibia. J Bone Joint Surg Am. 1984; 66: 1431-1437 [ Links ]
26. Arnoczky SP, Warren RF. Microvasculature of the human meniscus. Am J Sports Med. 1982; 10: 90-95 [ Links ]
27. Arnoczky SP, Warren RF. The microvasculature of the meniscus and its response to injury. An experimental study in the dog. Am J Sports Med. 1983; 11: 131-141 [ Links ]
28. DeHaven KE, Black KP, Griffiths HJ. Open meniscus repair. Technique and two to nine year results. Am J Sports Med. 1989; 17: 788-795 [ Links ]
29. Cassard X, Verdonk R, Almqvist KF. [Meniscal repair]. Rev Chir Orthop Reparatrice Appar Mot. 2004; 90 (3): 49-75 [ Links ]
30. Paxton ES, Stock MV, Brophy RH. Meniscal repair versus partial meniscectomy: a systematic review comparing reoperation rates and clinical outcomes. Arthroscopy. 2011; 27: 1275-1288 [ Links ]
31. Kohn D, Milachowski K, C W. Meniskus-transplantation. Hefte Unfallheilkd. 1988; 199: 61-67 [ Links ]
32. Milachowski KA, Weismeier K, Wirth CJ. Homologous meniscus transplantation. Experimental and clinical results. Int Orthop. 1989; 13: 1-11 [ Links ]
33. Hergan D, Thut D, Sherman O, Day MS. Meniscal allograft transplantation. Arthroscopy. 2011; 27: 101-112 [ Links ]
34. Monllau JC, Gonzalez-Lucena G, Gelber P, Pelfort X. Allograft Meniscus Transplantation: A Current Review. Techniques in Knee Surgery. 2010; 9: 107-113 [ Links ]
35. Harris JD, Cavo M, Brophy R, Siston R, Flanigan D. Biological knee reconstruction: a systematic review of combined meniscal allograft transplantation and cartilage repair or restoration. Arthroscopy. 2011; 27: 409-418 [ Links ]
36. Verdonk PC, Demurie A, Almqvist KF, Veys EM, Verbruggen G, Verdonk R. Transplantation of viable meniscal allograft. Survivorship analysis and clinical outcome of one hundred cases. J Bone Joint Surg Am. 2005; 87: 715-724 [ Links ]
37. Verdonk R. The meniscus: past, present and future. Knee Surg Sports Traumatol Arthrosc. 2011; 19: 145-146 [ Links ]
38. Langer R, Vacanti J. Tissue Engineering. Science. 1993; 260: 920-926 [ Links ]
39. Lubowitz JH, Poehling GG. Save the meniscus. Arthroscopy. 2011; 27: 301-302 [ Links ]
40. Elattar M, Dhollander A, Verdonk R, Almqvist KF, Verdonk P. Twenty-six years of meniscal allograft transplantation: is it still experimental? A meta-analysis of 44 trials. Knee Surg Sports Traumatol Arthrosc. 2011; 19: 147-157 [ Links ]
41. Lubowitz JH, Poehling GG. Tissue Engineering: A Call for Manuscripts. Arthroscopy. 2008; 24: 623-624 [ Links ]
42. Fetzer GB, Spindler KP, Amendola A. Potential market for new meniscus repair strategies: evaluation of the MOON cohort. J Knee Surg. 2009; 22: 180-186 [ Links ]
43. Jackson DW. The orthopaedic clinician-scientist. J Bone Joint Surg Am. 2001; 83-A: 131-135 [ Links ]
44. Wright JG, Swiontkowski MF, Heckman JD. Introducing levels of evidence to the journal. J Bone Joint Surg Am. 2003; 85-A: 1-3 [ Links ]
45. Kon E, Verdonk P, Condello V. Matrix-assisted autologous chondrocyte transplantation for the repair of cartilage defects of the knee: systematic clinical data review and study quality analysis. Am J Sports Med. 2009; 37 (1): 156-166 [ Links ]
46. Agung M, Ochi M, Yanada S. Mobilization of bone marrow-derived mesenchymal stem cells into the injured tissues after intraarticular injection and their contribution to tissue regeneration. Knee Surg Sports Traumatol Arthrosc. 2006; 14: 1307-1314 [ Links ]
47. Angele P, Johnstone B, Kujat R. Stem cell based tissue engineering for meniscus repair. J Biomed Mater Res. 2008; 85: 445-455 [ Links ]
48. Bulgheroni P, Murena L, Ratti C, Bulgheroni E, Ronga M, Cherubino P. Follow-up of collagen meniscus implant patients: clinical, radiological, and magnetic resonance imaging results at 5 years. Knee. 2010; 17: 224-229 [ Links ]
49. Chiari C, Koller U, Dorotka R. A tissue engineering approach to meniscus regeneration in a sheep model. Osteoarthritis Cartilage. 2006; 14: 1056-1065 [ Links ]
50. Cook JL, Fox DB. A novel bioabsorbable conduit augments healing of avascular meniscal tears in a dog model. Am J Sports Med. 2007; 35: 1877-1887 [ Links ]
51. Cook JL, Fox DB, Malaviya P. Long-term outcome for large meniscal defects treated with small intestinal submucosa in a dog model. Am J Sports Med. 2006; 34: 32-42 [ Links ]
52. Genovese E, Angeretti MG, Ronga M. Followup of collagen meniscus implants by MRI. Radiol Med. 2007; 112: 1036-1048 [ Links ]
53. Hannink G, van Tienen TG, Schouten AJ, Buma P. Changes in articular cartilage after meniscectomy and meniscus replacement using a biodegradable porous polymer implant. Knee Surg Sports Traumatol Arthrosc. 2011; 19: 441-451 [ Links ]
54. Horie M, Sekiya I, Muneta T. Intra-articular Injected synovial stem cells differentiate into meniscal cells directly and promote meniscal regeneration without mobilization to distant organs in rat massive meniscal defect. Stem Cells. 2009; 27: 878-887 [ Links ]
55. Ishida K, Kuroda R, Miwa M. The regenerative effects of platelet-rich plasma on meniscal cells in vitro and its in vivo application with biodegradable gelatin hydrogel. Tissue Eng. 2007; 13: 1103-1112 [ Links ]
56. Kamimura T, Kimura M. Repair of horizontal meniscal cleavage tears with exogenous fibrin clots. Knee Surg Sports Traumatol Arthrosc. 2011; [ Links ]
57. Kang SW, Son SM, Lee JS. Regeneration of whole meniscus using meniscal cells and polymer scaffolds in a rabbit total meniscectomy model. J Biomed Mater Res A. 2006; 78: 659-671 [ Links ]
58. Kobayashi Y, Yasuda K, Kondo E. Implantation of autogenous meniscal fragments wrapped with a fascia sheath enhances fi brocartilage regeneration in vivo in a large harvest site defect. Am J Sports Med. 2010; 38: 740-748 [ Links ]
59. Kon E, Chiari C, Marcacci M. Tissue engineering for total meniscal substitution: animal study in sheep model. Tissue Eng Part A. 2008; 14: 1067-1080 [ Links ]
60. Kopf S, Birkenfeld F, Becker R. Local treatment of meniscal lesions with vascular endothelial growth factor. J Bone Joint Surg Am. 2010; 92: 2682-2691 [ Links ]
61. Linke RD, Ulmer M, Imhoff AB. [Replacement of the meniscus with a collagen implant (CMI)]. Oper Orthop Traumatol. 2006; 18: 453-462 [ Links ]
62. Maher SA, Rodeo SA, Doty SB. Evaluation of a porous polyurethane scaffold in a partial meniscal defect ovine model. Arthroscopy. 2010; 26: 1510-1519 [ Links ]
63. Martinek V, Ueblacker P, Braun K. Second generation of meniscus transplantation: in-vivo study with tissue engineered meniscus replacement. Arch Orthop Trauma Surg. 2006; 126: 228-234 [ Links ]
64. Mizuno K, Muneta T, Morito T. Exogenous synovial stem cells adhere to defect of meniscus and differentiate into cartilage cells. J Med Dent Sci. 2008; 55: 101-111 [ Links ]
65. Ochiai S, Mizuno T, Deie M, Igarashi K, Hamada Y, Ochi M. Oxidative stress reaction in the meniscus of Bach 1 defi cient mice: potential prevention of meniscal degeneration. J Orthop Res. 2008; 26: 894-898 [ Links ]
66. Petersen W, Pufe T, Starke C. The effect of locally applied vascular endothelial growth factor on meniscus healing: gross and histological findings. Arch Orthop Trauma Surg. 2007; 127: 235-240 [ Links ]
67. Reckers LJ, Fagundes DJ, Cohen M. The ineffectiveness of fibrin glue and cyanoacrylate on fixation of meniscus transplants in rabbits. Knee. 2009; 16: 290-294 [ Links ]
68. Rodkey WG, DeHaven KE, Montgomery WH 3rd. Comparison of the collagen meniscus implant with partial meniscectomy. A prospective randomized trial. J Bone Joint Surg Am. 2008; 90: 1413-1426 [ Links ]
69. Scotti C, Pozzi A, Mangiavini L. Healing of meniscal tissue by cellular fi brin glue: an in vivo study. Knee Surg Sports Traumatol Arthrosc. 2009; 17: 645-651 [ Links ]
70. Stapleton TW, Ingram J, Fisher J, Ingham E. Investigation of the regenerative capacity of an acellular porcine medial meniscus for tissue engineering applications. Tissue Eng Part A. 2011; 17: 231-242 [ Links ]
71. Tienen TG, Heijkants RG, de Groot JH. Replacement of the knee meniscus by a porous polymer implant: a study in dogs. Am J Sports Med. 2006; 34: 64-71 [ Links ]
72. Tienen TG, Heijkants RG, de Groot JH. Meniscal replacement in dogs. Tissue regeneration in two different materials with similar properties. J Biomed Mater Res B Appl Biomater. 2006; 76: 389-396 [ Links ]
73. Weinand C, Peretti GM, Adams SB Jr, Bonassar LJ, Randolph MA, Gill TJ. An allogenic cell-based implant for meniscal lesions. Am J Sports Med. 2006; 34: 1779-1789 [ Links ]
74. Weinand C, Peretti GM, Adams SB Jr, Randolph MA, Savvidis E, Gill TJ. Healing potential of transplanted allogeneic chondrocytes of three different sources in lesions of the avascular zone of the meniscus: a pilot study. Arch Orthop Trauma Surg. 2006; 126: 599-605 [ Links ]
75. Weinand C, Xu JW, Peretti GM, Bonassar LJ, Gill TJ. Conditions affecting cell seeding onto three-dimensional scaffolds for cellular-based biodegradable implants. J Biomed Mater Res B Appl Biomater. 2009; 91: 80-87 [ Links ]
76. Welsing RT, van Tienen TG, Ramrattan N. Effect on tissue differentiation and articular cartilage degradation of a polymer meniscus implant: A 2-year follow-up study in dogs. Am J Sports Med. 2006; 36: 1978-1989 [ Links ]
77. Yamasaki T, Deie M, Shinomiya R, Yasunaga Y, Yanada S, Ochi M. Transplantation of meniscus regenerated by tissue engineering with a scaffold derived from a rat meniscus and mesenchymal stromal cells derived from rat bone marrow. Artif Organs. 2008; 32: 519-524 [ Links ]
78. Zaffagnini S, Giordano G, Vascellari A. Arthroscopic collagen meniscus implant results at 6 to 8 years follow up. Knee Surg Sports Traumatol Arthrosc. 2007; 15: 175-183 [ Links ]
79. Zaffagnini S, Muccioli GM Marcheggiani, Lopomo N. Prospective Long-Term Outcomes of the Medial Collagen Meniscus Implant Versus Partial Medial Meniscectomy: A Minimum 10-Year Follow-Up Study. Am J Sports Med. 2011; [ Links ]
80. Zellner J, Mueller M, Berner A. Role of mesenchymal stem cells in tissue engineering of meniscus. J Biomed Mater Res A. 2010; 94: 1150-1161 [ Links ]
81. Zhang H, Leng P, Zhang J. Enhanced meniscal repair by overexpression of hIGF-1 in a full-thickness model. Clin Orthop Relat Res. 2009; 467: 3165-3174 [ Links ]
82. Zur G, Linder-Ganz E, Elsner JJ. Chondroprotective effects of a polycarbonate-urethane meniscal implant: histopathological results in a sheep model. Knee Surg Sports Traumatol Arthrosc. 2011; 19: 255-263 [ Links ]
83. Verdonk R, Verdonk P, Huysse W, Forsyth R, Heinrichs EL. Tissue ingrowth after implantation of a novel, biodegradable polyurethane scaffold for treatment of partial meniscal lesions. Am J Sports Med. 2011; 39: 774-782 [ Links ]
84. Monllau JC, Gelber PE, Abat F. Outcome After Partial Medial Meniscus Substitution With the Collagen Meniscal Implant at a Minimum of 10 Years' Follow-up. Arthroscopy. 2011; 27: 933-943 [ Links ]
85. Galley NK, Gleghorn JP, Rodeo S, Warren RF, Maher SA, Bonassar LJ. Frictional Properties of the Meniscus Improve After Scaffold-augmented Repair of Partial Meniscectomy: A Pilot Study. Clin Orthop Relat Res. 2011; [ Links ]
86. Song F, Parekh S, Hooper L. Dissemination and publication of research findings: an updated review of related biases. Health Technol Assess. 2010; 14: 1-193 [ Links ]
87. Sridharan L, Greenland P. Editorial policies and publication bias: the importance of negative studies. Arch Intern Med. 2009; 169: 1022-1023 [ Links ]
88. Verdonk PC, Forsyth RG, Wang J. Characterisation of human knee meniscus cell phenotype. Osteoarthritis Cartilage. 2005; 13: 548-560 [ Links ]
89. Katsuragawa Y, Saitoh K, Tanaka N. Changes of human menisci in osteoarthritic knee joints. Osteoarthritis Cartilage. 2010; 18: 1133-1143 [ Links ]
90. Baker BM, Nathan AS, Huffman GR, Mauck RL. Tissue engineering with meniscus cells derived from surgical debris. Osteoarthritis Cartilage. 2009; 17: 336-345 [ Links ]
91. Pereira H, Frias AM, Caridade SG. Cellular and biomechanical segmental characterization of human meniscus. 2011 World Congress on Osteoarthritis - Osteoarthritis Research Society International OARSI. San Diego, CA, USA; 2011. [ Links ]
92. Pereira H, Frias AM, Caridade SG. Building the basis for human meniscus regeneration. 4th Joint ESAO-IFAO Congress 2011 XXXVIII Congress of the European Society for Artificial Organs (ESAO 2011) and IV Biennial Congress of the International Federation on Artificial Organs (IFAO 2011); Porto, Portugal; 2011. [ Links ]
93. Harada Y, Tokuda O, Fukuda K. Relationship between cartilage volume using MRI and Kellgren-Lawrence radiographic score in knee osteoarthritis with and without meniscal tears. AJR Am J Roentgenol. 2011; 196: 298-304 [ Links ]
94. Schiphof D, Boers M, Bierma-Zeinstra SM. Differences in descriptions of Kellgren and Lawrence grades of knee osteoarthritis. Ann Rheum Dis. 2008; 67: 1034-1036 [ Links ]
95. Mesiha M, Zurakowski D, Soriano J, Nielson JH, Zarins B, Murray MM. Pathologic characteristics of the torn human meniscus. Am J Sports Med. 2007; 35: 103-112 [ Links ]
96. Sweigart MA, Zhu CF, Burt DM. Intraspecies and interspecies comparison of the compressive properties of the medial meniscus. Ann Biomed Eng. 2004; 32: 1569-1579 [ Links ]
97. Gelber PE, Gonzalez G, Lloreta JL, Reina F, Caceres E, Monllau JC. Freezing causes changes in the meniscus collagen net: a new ultrastructural meniscus disarray scale. Knee Surg Sports Traumatol Arthrosc. 2008; 16: 353-359 [ Links ]
98. Bursac P, Arnoczky S, York A. Dynamic compressive behavior of human meniscus correlates with its extra-cellular matrix composition. Biorheology. 2009; 46: 227-237 [ Links ]
99. Ifkovits JL, Wu K, Mauck RL, Burdick JA. The infl uence of fibrous elastomer structure and porosity on matrix organization. PLoS One. 2010; 5 [ Links ]
100. Gunja NJ, Athanasiou KA. Effects of hydrostatic pressure on leporine meniscus cell-seeded PLLA scaffolds. J Biomed Mater Res A. 2010; 92: 896-905 [ Links ]
101. Gunja NJ, Uthamanthil RK, Athanasiou KA. Effects of TGF-beta1 and hydrostatic pressure on meniscus cell-seeded scaffolds. Biomaterials. 2009; 30: 565-573 [ Links ]
102. Upton ML, Chen J, Guilak F, Setton LA. Differential effects of static and dynamic compression on meniscal cell gene expression. J Orthop Res. 2003; 21: 963-969 [ Links ]
103. Leping Yan, Oliveira Joaquim M, Oliveira Ana L., Caridade Sofia G., Mano João F., Reis RL. Macro/micro porous silk fi broin scaffolds obtained via combined methodologies for articular cartilage and meniscus tissue engineering. Acta Biomaterialia. 2011; [ Links ]
104. Bai Feng, Zhang Jinkang, Wang Zhen. The effect of pore size on tissue ingrowth and neovascularization in porous bioceramics of controlled architecture in vivo. Biomed Mater. 2011; [ Links ]
105. Ribatti D, Nico B, Vacca A, Presta M. The gelatin sponge-chorioallantoic membrane assay. Nat Protoc. 2006; 1: 85-91 [ Links ]
106. Chevrier A, Nelea M, Hurtig MB, Hoemann CD, Buschmann MD. Meniscus structure in human, sheep, and rabbit for animal models of meniscus repair. J Orthop Res. 2009; 27: 1197-1203 [ Links ]
107. Burger C, Mueller M, Wlodarczyk P. The sheep as a knee osteoarthritis model: early cartilage changes after meniscus injury and repair. Lab Anim. 2007; 41: 420-431 [ Links ]
Conflito de interesse:
Nada a declarar.
Hélder Pereira
3B's Research Group
AvePark, Zona Industrial da Gandra
S. Cláudio do Barco
4806-909 Caldas das Taipas ]]>
Guimarães
Portugal
heldermdpereira@gmail.com
Data de Aceitação: 2011-09-01
]]>