Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Arquivos de Medicina
versão On-line ISSN 2183-2447
Arq Med vol.27 no.2 Porto abr. 2013
ARTIGO DE REVISÂO
Consentimento dos doentes para a publicação de Casos Clínicos: revisão da literatura
Patients Consent for publication of Case reports: a literature review
Maria João Bernardes1, Rui Nunes1
1 Serviço de Bioética e ética Médica, Faculdade de Medicina da Universidade do Porto
RESUMO
Introdução: Apesar de nos estudos observacionais ou experimentais realizados em humanos, publicados nas revistas com fator de impacto mais elevado, ser normalmente mencionado o cumprimento da regra de consentimento informado, o mesmo não acontece na publicação de casos clínicos. Neste trabalho efetuou-se uma revisão da literatura sobre as diversas dimensões do consentimento dos doentes para a publicação de casos clínicos.
Métodos: Desenvolveu-se uma revisão sistemática de publicações baseada em normas propostas para estudos de ordem argumentativa ou normativa, tendo-se realizado uma pesquisa bibliográfica na PubMed com as palavras MeSH [(informed consent or ethics) and (case report) and (publication)] ou com as palavras de texto [(report or reports) and publication and consent], escrutinada por dois avaliadores, com os limites English, Portuguese e humans. Resultados: Foram selecionados 36 artigos para análise em extenso, que incidiram essencialmente em opiniões de editores e de autores, tendo-se registado um reconhecimento consensual do direito dos doentes à autonomia e à confidencialidade, na publicação de casos clínicos, apesar de ser controverso o consentimento obrigatório em todos os casos. Em 7 dos 36 artigos, foi avaliada a referência ao consentimento, nas publicações de casos clínicos, em revistas de diversas áreas médicas, tendo-se registado valores de 0 a 23%. Conclusões: Apesar de existirem muitos pontos de consenso sobre o assunto, é necessária mais investigação, designadamente entre doentes e seus familiares, para melhor se elucidar como lidar com o consentimento para publicação de casos clínicos, sem se comprometer o dever de publicar em nome do progresso da medicina e do interesse público.
Palavras-chave: Caso clínico; consentimento; publicação
ABSTRACT
Introduction: Although reporting of patients consent for the publication of observational and experimental research studies involving humans is usual in medical journals with highest impact factor, the same does not seem to occur in case reports. The objective of this paper was the development of a literature review on patients consent for the publication of case reports.
Methods: A systematic review of publications was developed based on guidelines proposed for argumentative or normative studies. A PubMed search was performed using a query with the MeSH words [(informed consent or ethics) and (case report) and (publication)] or the text words [case and consent and (report or reports)], scrutinized by two assessors, with the limits English, Portuguese and humans, closely following the PRISMA and MOOSE guidelines.
Results: Thirty six papers were selected for full analysis, mostly authors and editors opinions, putting in evidence a consensual acknowledgment on the patients right to autonomy and confidentiality, although the obligation of a written consent for all case reports was controversial. In 7 of the 36 analysed papers, reporting of patients consent for the publication of case reports was explicitly assessed, ranging between 0 to 23%.
Conclusions: Although there are many points of consensus, more research is still needed, namely among patients and their relatives, to elucidate which is the best way to deal with the patients consent for the publication of case reports versus the doctors duty of publishing on behalf of the progress of medicine and of the public interest.
Key-Words: Case report; consent; publication
INTRODUÇÃO
O direito dos doentes à privacidade e á confidencialidade é um valor Hipocrático consagrado no Código Nuremberga, na Convenção de Genebra e nas sucessivas revisões da Declaração de Helsínquia sobre investigação em humanos, publicada originalmente em 1964.1,2
Contudo, apesar de ser normalmente o cumprimento da regra de consentimento informado nos estudos de investigação em humanos, nas revistas médicas com fator de impacto mais elevado, o mesmo não se verifica relativamente à publicação de casos clínicos.3-5 Esta situação tem preocupado autores e editores, na medida em que nos casos clínicos existe, de facto, um risco considerável de violação da privacidade e da confidencialidade, mesmo quando se anonimizam os dados e se acautela a divulgação de fotografias, de árvores genealógicas ou de outros elementos que permitam identificar os doentes envolvidos.6,7 Para além do desrespeito pelo doente, numa perspetiva não consequencialista, mais pura, ou Kantiana, a quebra da confidencialidade pode ter sentidos consequencialistas preocupantes , ao revelar comportamentos, fatores de risco ou doenças, que podem vir a condicionar a vida pessoal, , social e profissional dos doentes, limitando-lhes as suas relações interpessoais e o acesso a empregos ou a seguros de vida, entre outros,1 ainda que tal seja esporadicamente reportado na literatura.8
Por outro lado, há que assegurar o dever de publicar casos clínicos, em nome do benefício dos doentes, em particular em situações clinicas de maior raridade idiossincrasia.27,33De facto, nessas situações muitas vezes não é possível outro tipo de divulgação científica, sendo essa condição devidamente reconhecida por normas e autores que se têm dedicado ao assunto.9,27,30,33
Neste artigo apresenta-se uma revisão da literatura sobre a problemática do consentimento do doente para a publicação de casos clínicos.
MATERIAL E MÉTODOS
Desenvolveu-se uma revisão sistemática de publicações sobre um tema de ordem argumentativa ou normativa -a obrigatoriedade de consentimento informado para publicação de casos clínicos-com base em orientações propostas recentemente por Strech e Sofaer,45 tendo em consideração princípios estabelecidos nas normas PRISMA e MOOSE, propostas para revisões sistemáticas de estudos quantitativos.46
Realizou-se uma pesquisa bibliográfica na Pub-Med, com as palavras de MeSH e de texto [((informed consent) or ethics) and publication and (case report) or ((report or reports) and publication and consent)], até 30 de Abril de 2012, com limites para as línguas English e Portuguese e para os participantes humans (Figura 1).
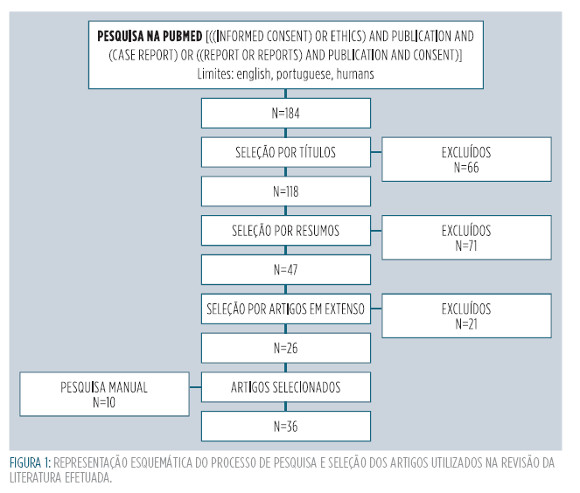
Os títulos e os resumos das referências obtidas na PubMed foram analisados, tendo sido excluídas as referências que se referiam inequivocamente a assuntos não relacionados com os objetivos do trabalho, tais como estudos sem qualquer relação com casos clínicos. Os artigos restantes foram analisados em extenso, tendo sido selecionados para análise final os artigos que cumpriam os critérios de inclusão, isto é, que se referiam a qualquer dimensão concetual do consentimento do doente para a publicação de casos clínicos, nomeadamente se foi verificada a competência, informação, compreensão, voluntariedade e consentimento dos doentes (Figura 1).
Concluído o processo referido, complementou-se a seleção obtida com uma pesquisa manual efetuada entre as referências bibliográficas dos artigos apurados (Figura 1).
Na pesquisa inicial, obtiveram-se 184 artigos, dos quais se excluíram, numa primeira fase, 66 artigos, por análise exclusiva dos títulos e numa segunda fase, outros 71, por análise dos resumos. Restaram 47 artigos para análise em extenso, dos quais foram excluídos 21. Aos 26 artigos restantes juntaram-se 10 artigos, obtidos por pesquisa manual das referências bibliográficas apuradas, tendo-se chegado ao número final de 36 artigos para análise de conteúdo temático e extração das principais normas e opiniões sobre consentimento dos doentes para a publicação de casos clínicos (Figura 1).
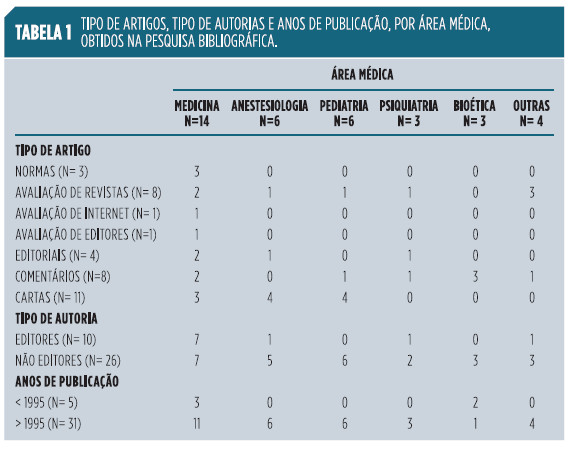
Construiu-se a Tabela 1 com distribuição dos artigos analisados, por tipo de artigo, e de autoria, e por área médica e a Tabela 2 com transcrição resumida das normas internacionais publicadas sobre o assunto, categorizadas e subcategorizadas por conteúdo temático. As avaliações de autores, editores ou internet corresponderam a artigos em que se avaliaram opiniões e práticas de consentimento na publicação de casos clínicos, entre autores3,4,12,13,15,16,18 e editores6 e na internet.14 A distribuição por área médica considerou, dentro do possível, as grandes áreas de especialização médica.
Construiu-se ainda a Tabela 3 com uma categorização e subcategorização global de todas as normas e opiniões de autores e editores extraídas, ordenadas por conteúdo temático-resumido e por força de concordância entre autores e importância relativa das publicações analisadas, tendo-se atribuído 3 pontos às publicações de normas, 2 às avaliações de autores, editores ou internet e 1 aos comentários ou editoriais (Tabela 1).
A seleção de artigos e a análise de conteúdos foi escrutinada por dois avaliadores, de forma independente. As discordâncias foram ultrapassadas de forma iterativa até se obter um consenso final.
RESULTADOS
Na Tabela 1, apresenta-se a distribuição dos artigos analisados, por tipo de artigo, e de autoria, e por área médica. Dos 36 artigos analisados, 3 corresponderam a normas internacionais,9-11 10 a estudos de avaliação de editores, internet ou revistas,3,4,6,12-18 11 a cartas,19-29 8 a comentários30-37 e 4 a editoriais.7, 38-40 A maior parte dos artigos provieram da Medicina Geral/Medicina interna e da Anestesiologia, seguidas da Pediatria, Psiquiatria, bioética, otorrinolaringologia, Dermatologia, Medicina Física e Acupuntura. Vinte e seis artigos foram obtidos pela pesquisa da PubMed e 10 por pesquisa manual, estando incluídas neste último grupo as três normas internacionais analisadas.9-11
As Tabela 2 e 3 permitem constatar que, apesar de existirem vários pontos de consenso entre as normas, os autores e os editores, permanecem questões controversas. De facto, parece ser consensual o reconhecimento do direito dos doentes à autonomia conhecimento do direito dos doentes à autonomia problemática a obrigatoriedade de se obter o consentimento informado escrito dos doentes para a publicação de todos os casos clínicos. Alguns autores e editores defendem o consentimento informado escrito em todos os casos,28,36,39,40 enquanto outros sustentam uma avaliação, caso a caso, do risco de violação da privacidade versus o dever de publicação de ocorrências relevantes para o bem dos doentes,27,29 sendo ainda consideradas as situações em que poderá ser impossível a obtenção de consentimento do próprio, como acontece em caso de morte do doente.10,31,40 Na Tabela 3, pode ainda verificar-se que em 7 dos 36 artigos analisados, foi avaliada a referência ao consentimento, nas publicações de casos clínicos, em revistas de diversas áreas, tendo-se registado valores de 0 a 23%.3,4,12,13,15,16,18
DISCUSSÃO E CONCLUSÕES
A análise das questões relacionadas com o consentimento do doente para a publicação de casos clínicos parece-nos pertinente, na sociedade global em que vivemos, com acesso quase ilimitado e instantâneo à informação sobre tudo o que se passa, sendo necessário encontrar um balanço adequado entre o dever de publicar, em prol do progresso do tratamento dos doentes, e o risco de violação do direito à autonomia e à confidencialidade, através de revistas, rádio, televisão ou internet. Para esse fim, desenvolvemos uma revisão sistemática de publicações sobre um tema de ordem argumentativa ou normativa com base em orientações propostas recentemente por Strech e Sofaer,45 tendo em consideração as normas PRISMA e MOOSE, propostas para revisões sistemáticas de estudos quantitativos46 (Figura 1). Este processo é cada vez mais difícil, dado o crescimento imparável do número de publicações, e de bases de dados disponíveis, mas parece-nos ter sido conseguido, a avaliar pela consistência dos resultados obtidos na pesquisa realizada na PubMed e na análise manual efetuada entre as referências bibliográficas dos artigos selecionados. Contudo, importa salientar que, se não se tivesse complementado a pesquisa das bases de dados com uma pesquisa manual, não se teria chegado a nenhum documento com o valor de norma internacional,9-11 o que alerta para a necessidade de, nos trabalhos de revisão, particularmente em revisões qualitativas da literatura, se utilizar sempre uma metodologia semelhante à proposta por Strech e Sofaer.45
A maior parte dos artigos analisados corresponderam a comentários, cartas e editoriais, isto é, a opiniões de autores e de editores (Tabela 1). Não estranhando esta situação na área da bioética, em que, como já foi referido por outros autores,41 a investigação qualitativa avulta em relação à quantitativa, pensamos que algumas dúvidas poderiam ter tido resposta com estudos quantitativos. Seria, por exemplo, importante avaliar, em estudos de coorte, de séries de casos, de casos-controlos ou mesmo em estudos aleatorizados, se os doentes que prestam consentimento para publicação o fazem de uma forma efetivamente competente, informada, esclarecida, livre e consentida, questionando-os sobre o assunto algum tempo depois de terem prestado o consentimento, ou depois de confrontados com a publicação efetiva dos casos, ou em comparação com doentes a quem não foi solicitado consentimento.
A área médica em que se publicaram mais artigos (Tabela 1) foi a Medicina Geral/Medicina interna, seguida pelas áreas de Anestesiologia, Pediatria, Psiquiatria e bioética, que cobrem doentes particularmente vulneráveis, como os sujeitos a anestesia, as crianças e os doentes psiquiátricos. Acresce que os doentes dos dois últimos grupos são frequentemente considerados incompetentes, do ponto de vista legal, para efeitos da prestação de consentimento. Para além das áreas referidas, foram publicados artigos em Medicina Física, Acupuntura, otorrinolaringologia e Dermatologia, estando ainda por avaliar outras áreas com doentes especialmente vulneráveis como a Genética e a Geriatria.
Quanto aos anos de publicação dos artigos (Tabela 1), registou-se um predomínio significativo no período superior a 1995, ano em que se publicaram as normas éticas, relacionadas com a publicação de casos clínicos, do international Committee of Medical Journal Editors (ICMJE).9,30 Este aspeto sugere alguma lentidão no processo de regulamentação ética, relacionado com a publicação de casos clínicos, desde a primeira edição da Declaração de Helsínquia publicada em 1964.2 Sugere ainda, como pode ser difícil chegar a consensos, nomeadamente no que respeita à obrigatoriedade do consentimento ser ou não escrito, para todos ou apenas para alguns casos clínicos (Tabela 2 e 3). Contudo, há que ter em conta o crescimento explosivo do número de publicações médicas indexadas registado nas últimas décadas, que poderá, por si só, explicar as diferenças encontradas na análise temporal efetuada, sem esquecer outros aspetos de maior complexidade, relacionados com as diferenças económicas, sociais e culturais, existentes entre os diversos autores e editores do mundo, como, por exemplo, as que poderão ter estado subjacentes à cisão registada entre os Estados unidos da América e os outros países que assinaram a revisão de Tóquio de 2004 da Declaração de Helsínquia, relacionada com a realização de ensaios clínicos em países mais desfavorecidos.47
O resultado da análise que efetuámos revela aspetos consensuais e controvérsias, entre as normas internacionais e as opiniões de autores e de editores (Tabela 2 e 3). É razoavelmente consensual que não devem ser publicadas informações identificadoras de doentes, tais como, nomes, iniciais, números hospitalares, fotografias ou árvores genealógicas, a menos que sejam essenciais para fins científicos e o doente (ou seu representante legal) dê consentimento informado escrito.9-11 O caso da publicação de árvores genealógicas é especialmente preocupante, na medida em que envolve várias pessoas, de várias gerações, de uma família.37,42 No entanto, alguns autores põem em causa a necessidade de consentimento obrigatório, sejam quais forem as circunstâncias,27,29 defendendo que, embora a sua obtenção seja teoricamente desejável, podendo proteger autores e editores de problemas médico-legais, o mesmo poderá não ser possível10,31,40 e não ser verdadeiramente livre, informado e indicado, não contribuindo para uma proteção efetiva dos doentes, mas funcionando antes como um elemento de garantia exclusiva do cumprimento de quesitos de índole legal pura.30 Além disso, em caso de dúvida quanto à anonimização dos dados dos doentes, alguns autores consideram que se deverá obter consentimento, sem especificarem se este deverá ou não ser escrito,11 enquanto outros consideram que o consentimento deverá ser sempre também na forma escrita.9,10 É também razoavelmente consensual que o consentimento informado pressupõe que o doente tenha conhecimento dos dados relacionados com a divulgação do seu caso, designadamente se tal ocorrerá por escrito, numa conferência médica ou na internet, não se devendo utilizar os dados para fins que não tenham obtido consentimento explícito.9,11 No entanto, algumas normas e autores, consideram que, quando não for possível obter consentimento, poderá justificar-se a divulgação de casos, em situação de interesse público.10,11 outros autores consideram que a situação anterior só poderá acontecer se, adicionalmente, se julgar não existirem razões para que um indivíduo razoável se oponha à publicação,10 havendo ainda quem considere que nenhum caso clínico, em circunstância alguma, deverá ser publicado sem consentimento escrito, nomeadamente quando está em causa a publicação em revistas de acesso aberto na internet.40 Parece ser também consensual que nos casos em que seja necessária a obtenção de um consentimento escrito, esse consentimento deva registar-se em formulário universalmente aceite por todas as revistas, e não apenas por umas revistas, sem ser aceite por outras, como ainda é prática corrente. Na verdade, uma vez rejeitado um artigo, dificilmente os autores conseguirão o preenchimento de um novo formulário para submissão a uma outra revista.19,23,26
Um aspeto que merece reflexão é o de em 7 dos 36 artigos analisados, em que foi avaliada a referência ao consentimento nas publicações de casos clínicos se tenham registado valores de 0 a 23%,3,4,12,13,15,16,18 sendo que, tal só ocorreu em 1 em cada 32 casos divulgados pela internet,14 tendo todos estes estudos sido realizados depois da publicação das normas da ICMJE em1995,9 tal como aconteceu em estudo recentemente realizado entre revistas portuguesas, com resultados semelhantes.48 De igual modo, deverão ser considerados os dados de um estudo de Nylenna e colaboradores, segundo o qual apenas 7 em 75 editores referiram requerer consentimento informado para a publicação de casos clínicos,6 para além dos dados reportados por Murray e colaboradores, segundo os quais 67% dos médicos de cuidados não primários referiam que reportariam casos sem consentimento, enquanto apenas 25% dos doentes esperaria que tal acontecesse.25 Estes números, relativamente baixos, de referência ao consentimento dos doentes para a publicação de casos clínicos, que não implicam necessariamente que o consentimento não tenha sido obtido, ou que tenha havido má conduta ética,16 deverão ser reavaliados em trabalhos futuros. Acresce que, para além do imperativo ético, não se deverá negligenciar a importância da referência explícita ao consentimento, em todos os casos,22 para a análise de vieses de seleção,43,44 na medida em que os casos em que é dado o consentimento poderão corresponder a situações de maior ou menor gravidade da doença ou vulnerabilidade do doente.
Em conclusão, a análise das questões relacionadas com o consentimento dos doentes para a publicação de casos clínicos é um tema ainda pouco estudado, com um número escasso de artigos publicados sobre o assunto, maioritariamente de opinião. Embora seja evidente uma dinâmica no sentido de se obterem consensos, registam-se ainda controvérsias, faltando estudos mais sistematizados, que incluam não só autores e editores, mas também doentes e seus familiares. Falta, também, uma análise do cumprimento das normas internacionais, que cubra um espectro mais alargado das especialidades médicas. Finalmente, falta provar inequivocamente que o consentimento escrito obrigatório proteja melhor o direito do doente à autonomia e à confidencialidade do que o simples consentimento não escrito ou, mesmo, a ausência de consentimento.
AGRADECIMENTOS
Aos Professores Linda Ohler, Madison Powers, Marjan Kljakovic e Sara Douglas agradece-se a disponibilização dos artigos por nós solicitados.
REFERÊNCIAS
1. Pedroni JA, Pimple KD. A brief introduction to informed Consent in Research with Human Subjects The trustees of indiana university 2001. (Disponível em http://mypage.iu.edu/~pimple/eis/ic.pdf, acedido em 29 de Setembro de 2011) [ Links ]
2. World Medical Association (WMA) Declaration of Helsinki – Ethical Principles for Medical Research involving Human Subjects. (Disponível http://www.wma.net/en/30publications/10policies/b3/index.html.pdf?print-media-type&footer-right=[page]/[toPage, acedido em 1 de Novembro de 2011) [ Links ]
3. Myles PS, tan N. Reporting of ethical approval and informed consent in clinical research published in leading anesthesia journals. Anesthesiology 2003;99:1209-13. [ Links ]
4. Henley lD, Frank DM. Reporting ethical protections in physical therapy research. Phys Ther 2006;86:499-509. [ Links ]
5. Bauchner H, Sharfstein J. Failure to report ethical approval in child health research: review of published papers. Bmj 2001;323:318-9. [ Links ]
6. Nylenna M and Riis P. Identification of patients in medical publications: need for informed consent. Bmj 1991; 302: 1182. [ Links ]
7. Goldim JR, Fleck MP. Ethics and publication of single case reports. Rev bras Psiquiatr 2010;32:2-3. [ Links ]
8. Mogul KM. Ethics complaints against female psychiatrists. Am J Psychiatry 1992;149:651-3. [ Links ]
9. International Committee of Medical Journal Editors (icmje). Uniform Requirements for Manuscripts Submitted to biomedical Journals: Ethical Considerations in the Conduct and Reporting of Research: Privacy and Confidentiality. (Disponível em http://www.icmje.org/ethical_5privacy.html, acedido em 1 de Novembro de 20011)
10. Committee on Publication Ethics (cope). Cope code of conduct for editors of biomedical journals. (Disponível em http://www.publicationethics.org/files/u2/New_Code.pdf, acedido em 1 de Novembro de 2011) [ Links ]
11. General Medial Council Supplementary Guidance. Confidentiality: disclosing information for education and training purposes. (Disponível em http://www.gmc-uk.org/static/documents/content/Confidentiality_disclosing_info_education_2009.pdf, acedido em 1 de Novembro de 20011)
12. Walter G, Rey JM, Dekker F. The humble case report. Aust N Z J Psychiatry 2001;35:240-5. [ Links ]
13. Schroter S, Plowman R, Hutchings A, Gonzalez A. Reporting ethics committee approval and patient consent by study design in five general medical journals. J Med Ethics 2006;32:718-23. [ Links ]
14. Markovitz bP, Goodman KW. Case reports on the Web redux: confidentiality still in jeopardy. AMiA Annu Symp Proc 2003:926. [ Links ]
15. Noone MC, Walters KC, Gillespie Mb. Research subject privacy protection in otolaryngology. Arch otolaryngol Head Neck Surg 2004;130:266-9. [ Links ]
16. Albrecht J, Meves A, Bigby M. A survey of case reports and case series of therapeutic interventions in the Archives of Dermatology. Int J Dermatol 2009;48:592-7. [ Links ]
17. Kljakovic M. Single cases in general practice and general medical journals. Aust Fam physician 2002;155:585-92. [ Links ]
18. Dingemann J, Dingemann C, Ure B. Failure to report ethical approval and informed consent in paediatric surgical publications. Eur J Pediatr Surg 2011;21:215-9. [ Links ]
19. Aldridge RW. Simplifying consent for publication of case reports. BMJ 2008 1;337:a1878. doi: 10.1136/bmj.a1878. [ Links ]
20. Ghai b, Saxena AK. Patients consent for publication. Anaesthesia 2005;60:289. [ Links ]
21. Honan D. Consent for publication of a case report. Anaesthesia 2004;59:1143. [ Links ]
22. Hubregtse G, Collins SJ. Patient consent for case reports. Anaesthesia 2001;56:906-7. [ Links ]
23. John CM. Mathew DE. Universal patient consent form for case reports. Acta Paediatr 2009;98:612. [ Links ]
24. Markovitz bP. Editors and authors vexed and confused by consent. bMJ 2008;337:774. [ Links ]
25. Murray J. Consent for publication. JAMA 1982;248:3093-4. [ Links ]
26. Saxena AK, Ghai b, Makkar JK. Patients consent for publication of case report: need for developing a universal consent form. Arch Dis Child 2006;91:717. [ Links ]
27. Tierney e. Consent for publication of a case report. Anaesthesia 2004;59:822-3. [ Links ]
28. Weiss b. Consent for publication. JAMA 1982;248:3094. [ Links ]
29. Coulthard MG, San lazaro C. Case reports of factitious illness are unlikely to be published in the UK. Arch Dis Child 2009;94:171. [ Links ]
30. Levine Sb, Stagno SJ. Informed consent for case reports: the ethical dilemma of right to privacy versus pedagogical freedom. J Psychother Pract Res 2001;10:193-201. [ Links ]
31. Singer PA. Consent for publication of patient information. bMJ 2004;329:566-8. [ Links ]
32. Chambers t. Questionable ethics-whistle-blowing or tale-telling? J Med Ethics 1997;23:382-3. [ Links ]
33. Gibson E. Publication of case reports: is consent required? Paediatr Child Health 2008;13:666-7. [ Links ]
34. Herrera CD. Patient vignettes in bioethics literature. J Clin Ethics 2000;11:213-8. [ Links ]
35. Richards t. Court sanctions use of anonymised patient data. bMJ 2000;320:77b. [ Links ]
36. White A. Writing case reports. Acupunct Med 2004;22:83-6. [ Links ]
37. Powers M. Publication-related risks to privacy: ethical implications of pedigree studies. IRb 1993;15:7-11. [ Links ]
38. Bevan JC, Hardy JF. Permission to publish case reports/case series. Can J Anaesth 2004;51:861-6. [ Links ]
39. Frizelle F. Consent for case reports and medical images. N Z Med J 2009;122:8-10. [ Links ]
40. Kidd MR, Hrynaszkiewicz i. Journal of Medical Case Reports policy on consent for publication. Journal of Medical Case Reports 2010; 4:173. [ Links ]
41. Racine E, Karczewska M, Seidler M, Amaram R, illes J. How the public responded to the Schiavo controversy: evidence from letters to editors. J Med Ethics 2010;36:571-3. [ Links ]
42. Botkin JR, McMahon WM, Smith KR, Nash JE. Privacy and confidentiality in the publication of pedigrees: a survey of investigators and biomedical journals. JAMA 1998;279:1808-12. [ Links ]
43. Edlund MJ, Craig TJ, Richardson MA. Informed consent as a form of volunteer bias. Am J Psychiatry 1985;142:624-7. [ Links ]
44. Douglas S, Briones J, Chronister C. The incidence of reporting consent rates in nursing research articles. Image J Nurs Sch 1994;26:35-40. [ Links ]
45. Strech D, Sofaer N. How to write a systematic review of reasons. J Med Ethics 2012;38:121-6. [ Links ]
46. Liberati A, Altman DG, Tetzlaff J, Mulrow C, Gøtzsche PC, Ioannidis JP, Clarke M, Devereaux PJ, Kleijnen J, Moher D.The PRiSMA statement for reporting systematic reviews and metaanalyses of studies that evaluate health care interventions: explanation and elaboration. PloS Med 2009;6:e1000100. [ Links ]
47. Veloso AJb. Ética e ensaios clínicos à luz da Declaração de Helsínquia. Revista da ordem dos Médicos 2010; 2:52-56. [ Links ]
48. Bernardes MJ, Nunes R. Reporting of ethical committee approval and patient consent in the Portuguese Journal of Pulmonology and in the other Portuguese medical journals with impact factor. Rev Port Pneumol 2012;18:289-93. [ Links ]
Rui Nunes
Serviço de Bioética e ética Médica Faculdade de Medicina da Universidade do Porto
Al. Prof. Hernâni Monteiro 4200-319 Porto
Email: ruinunes@med.up.pt














