Serviços Personalizados
Journal
Artigo
Indicadores
Links relacionados
Compartilhar
Jornal Português de Gastrenterologia
versão impressa ISSN 0872-8178
J Port Gastrenterol. v.17 n.2 Lisboa mar. 2010
Relato de um caso – Síndrome de Ogilvie associada a adenocarcinoma de pâncreas
Luís Alberto Schlittler1, Nicolas Silva Lazaretti1, Rodrigo Ughini Villaroel1, Claudia Schavinski3, Paulo Sérgio Osório2, Tais Mazzini4, Viviane Weiller Dallagasperina4
1Médico Oncologista do Hospital da Cidade de Passo Fundo/RS/Brazil;
2Médico Radiologista do Hospital da Cidade de Passo Fundo/ RS/Brazil;
3Médica Residente em Clínica Médica do Hospital da Cidade de Passo Fundo;
4Estudante de Medicina da Universidade de Passo Fundo; Serviço de Oncologia do Hospital da Cidade, Passo Fundo, Rio Grande do Sul, Brazil
Resumo
A pseudo-obstrução cólica aguda (Síndrome de Ogilvie) é caracterizada por um conjunto de sinais e sintomas de obstrução do cólon sem uma causa mecânica identificável. Os autores relatam o caso de um doente do sexo feminino, 78 anos com quadro clínico de abdómen agudo obstrutivo associado a adenocarcinoma de pâncreas tratado com descompressão endoscópica.
Olgivies syndrome associated with pancreatic adenocarcinoma
Abstract
Acute colonic pseudo-obstruction (Ogilvies Syndrome) is characterized by signs and symptoms of large bowel obstruction without a mechanical cause. Authors report one case of a 78-year-old female patient, with acute colonic pseudo-obstruction associated with pancreatic adenocarcinoma treated with endoscopic decompression.
INTRODUÇÃO
A pseudo-obstrução intestinal ou síndrome de Ogilvie é caracterizada por dilatação do cólon, simulando oclusão intestinal, sem que se encontre uma causa mecânica para a obstrução1. Em 1948, Henage Ogilvie descreveu uma síndrome clínica que chamou de pseudo-obstrução do intestino grosso devido à privação de inervação do simpático, e descreveu dois casos com sintomas fortemente sugestivos de obstrução do cólon, porém opaco normal e que posteriormente foram submetidos a laparotomia, que evidenciou um cólon normal, havendo envolvimento maligno no plexo celíaco. Na época, Olgivie concluiu que o tumor interrompeu a inervação simpática do intestino grosso, levando o sistema parassimpático com seus ramos sagrados a actuar em sentido oposto produzindo um espasmo regional2.
Os mecanorreceptores localizados na parede do intestino grosso, quando estimulados pela distensão, ativam uma via reflexa cujo efeito final (via nervos simpáticos eferentes através do plexo mioentérico ou placas nervosas em músculos lisos) é a inibição da motilidade do cólon (reflexo do cólon). O mecanismo fisiopatológico resume-se a um desequilíbrio na inervação autonómica3, de origem multifactorial: inibição do reflexo motor através dos ramos aferentes esplâncnicos em resposta a um estímulo nocivo, excesso de resposta inibitória motora simpática, diminuição do estímulo excitatório e excesso de resposta inibitória sobre o parassimpático, inibição da libertação do oxido nítrico (NO) pelos neurónios, além da estimulação periférica excessiva dos receptores de opióides4. Apesar destes dados, ainda há necessidade de estudos para um melhor entendimento fisiopatológico.
A incidência exacta da Síndrome de Olgivie não é conhecida. A maioria dos casos afecta idosos, predominantemente do sexo masculino (60%), hospitalizados ou institucionalizados, com uma patologia clínica grave5 (hipotiroidismo, amiloidose, enfarte agudo do miocárdio, ascite vascular cerebral, hipóxia, inflamação sistémica ou localizada no peritoneu, intestino delgado, tracto urinário ou tórax, entre outras.), intervenção cirúrgica recente (traumática, ortopédica, pélvica, cesariana e torácica), uso de clonidina e a gravidez. Num estudo retrospectivo de 400 casos, as condições predisponentes mais comuns foram: traumas (11%), infecções (10%) e doenças cardíacas (10%)5.
MATERIAL E MÉTODOS
Mulher, 78 anos, procedente de Passo Fundo, Rio Grande do Sul, Brasil, foi submetida a tratamento com quimioterapia paliativa com gemcitabina por adenocarcinoma da cabeça do pâncreas com metástases hepáticas aquando do diagnóstico. Após seis ciclos de quimioterapia paliativa, com boa resposta clínica – diminuição importante da dor, aumento apetite e melhoria da performance clínica inicial, também foi evidenciada diminuição do marcador tumoral CA 19-9 (queda de 70% do valor inicial ao diagnóstico) e uma regressão parcial das lesões hepáticas e pancreática na tomografia computorizada abdominal de para reestadiamento. A paciente estava assintomática, indicado acompanhamento clínico periódico na Oncologia.
Após quatro meses em ambulatório, quase um ano após o diagnóstico da neoplasia, a doente apresentou-se no serviço de urgência com um quadro súbito de dor e distensão abdominal associado à paragem da emissão de fezes e gases. Ao exame físico, os ruídos hidroaéreos estavam ausentes e tínhamos aumento do volume abdominal, com dor difusa e distensão. A doente permanecia apirética, sem sinais clínicos de infecção. Laboratorialmente encontrava-se anemia leve e alterações discretas da enzimologia hepática, provavelmente relacionado a presença de metástases hepáticas. A Radiografia do abdómen evidenciou distensão gasosa com acumulação de resíduos fecais no cólon, ausência de níveis hidroaéreos em ortostatismo e ausência de sinais de liquido livre na cavidade peritoneal (Fig. 1). Novo exame de controle após 24 horas mostrou dólico-megacólon com importante distensão gasosa e presença de gás no recto (Fig. 2) e em 48 horas notava-se um aumento da distensão de ansa cólicas e pequena distensão do intestino delgado (Fig. 3). Não foi realizado tomografia computorizada ou ecografia abdominal. Foi mantido suporte clínico com hidratação endovenosa, suspensão da dieta entérica, drenagem nasogástrica e analgesia.
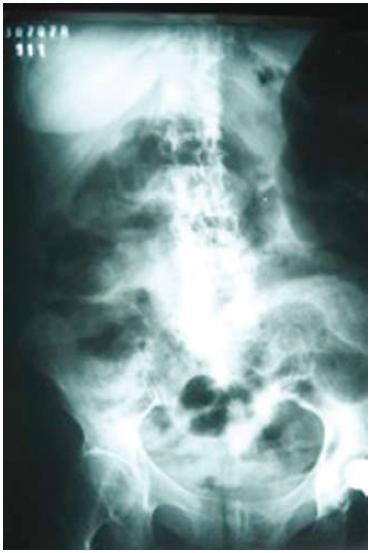
Fig. 1. Distensão gasosa e acumulação de resíduos fecais nos cólons. Ausência de níveis hidroaéreos em ortotatismo. Ausência de sinais de líquido livre.
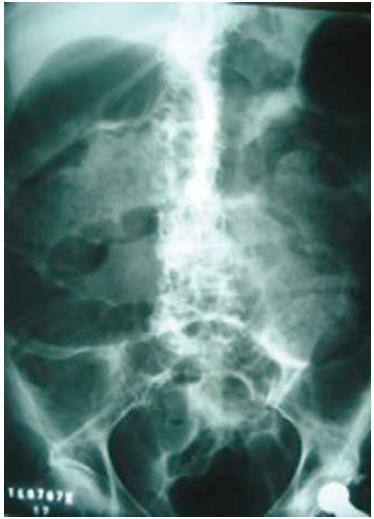
Fig. 2. Dólico megacólon com importante distensão gasosa e acumulação de resíduos fecais. Presença de gás no recto. Sem sinais de pneumoperitoneu.
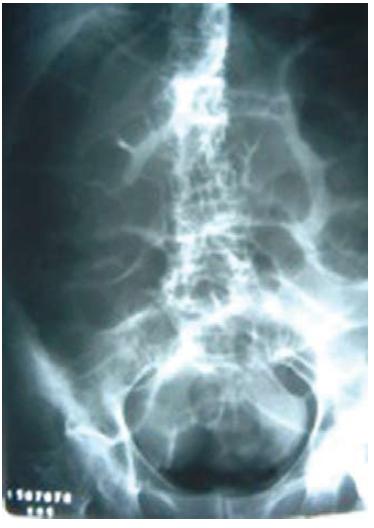
Fig. 3. Importante distensão de ansas de intestino grosso e pequena distensão de intestino delgado.
Com a hipótese de pseudoobstrução intestinal tentou-se tratamento com neostigmina por via endovenosa, sem resposta clínica. Logo em seguida, foi realizado tratamento endoscópico descompressivo. A Colonoscopia avaliou todo o cólon, sendo realizada aspiração do grande conteúdo gasoso encontrado e, logo após o exame, notava-se uma melhora clínica parcial dos sintomas iniciais.
Cerca de 48 horas após endoscopia ocorreu agravamento do quadro de distensão abdominal e da dor. Associado aos sintomas abdominais, a paciente desenvolveu uma broncopneumonia nosocomial grave que culminou no óbito.
DISCUSSÃO
Manifestações Clínicas
Os principais achados clínicos da síndrome de Olgivie incluem distensão abdominal (100%), náuseas e vómitos (15% a 71%) e dor abdominal (80%). A eliminação de gases e fezes é descrita em mais de 40% dos doentes5. A distensão abdominal é o primeiro sinal, ocorrendo usualmente entre 3-7 dias após início da doença. Em doentes cirúrgicos desenvolve-se em média, após cinco dias de pós-operatório5. A paragem de eliminação fecal é um sinal importante, mas pode eventualmente ser intercalada com esteatorreia. Os ruídos intestinais estão ausentes em 12% dos casos e presentes, de qualidade normal ou até exacerbada, em 88% das vezes6.
Ao exame físico, o abdómen muitas vezes é timpânico, doloroso, com contractura muscular involuntária da parede abdominal. Pode haver febre e leucocitose, que são mais comuns em doentes com isquemia ou perfuração1.
Apesar da grande importância do exame objectivo nesta condição, o seu diagnostico é difícil e muitas vezes desvalorizado1. O reconhecimento precoce e o manejo apropriado são imprescindíveis para minimizar complicações.
A paciente do caso exposto neste artigo apresentou quadro de dor e distensão abdominal associado à paragem na eliminação de fezes e gases. Náuseas e vómitos não estavam presentes, o que corrobora os dados da literatura prévia, a qual demonstra grande variabilidade na frequência destes sintomas na Síndrome de Ogilvie.
Diagnóstico
O diagnóstico deve ser confirmado através de exames complementares, sendo indispensável a radiografia simples de abdómen, que mostrará graus variados de dilatação cólica. O cólon direito e cego usualmente apresentam distensão mais acentuada, além disso, cut-offs no ângulo esplénico e colon descendente são comuns. A distribuição da dilatação cólica pode ser definida pelas diferentes origens do nervo parassimpático proximal e distal que suprem o colon. Níveis hidroaéreos e dilatação também podem ser visualizados no intestino delgado dependendo da competência da válvula ileocecal7.
No caso apresentado, a radiografia de abdómen demonstrou distensão gasosa com acumulação de resíduos fecais no cólon, ausência de níveis hidroaéreos em ortostatismo e ausência de sinais de liquido livre na cavidade peritoneal.
Os diagnósticos diferenciais da distensão cólica aguda em doentes hospitalizados incluem: obstrução mecânica, megacolon tóxico devido à infecção grave por Clostridium difficile7 e pseudo-obstrução intestinal aguda.
Exames Complementares
Exame contrastado pode ser realizado caso não seja visualizado ar em todos os segmentos do cólon na radiografia simples. A acuidade do exame é de 97% com risco de perfuração intestinal de 1,2%4.
A Colonoscopia é um bom método para diagnóstico diferencial com colite pseudomembranosa, enquanto se aguarda sorologia para o microorganismo8. É também, uma alternativa ao exame contrastado, podendo ser utilizado concomitantemente como tratamento. Vale lembrar que os riscos de complicações são consideráveis.
Tomografia Computadorizada tem especificidade de 93% para evidenciar dilatações cólicas9. Além disso, evidencia a presença de ar e liquido livres na cavidade sem a necessidade de contrastes ou risco de ruptura visceral.
Manejo
O manejo apropriado implica a exclusão de obstrução mecânica e outras causas de megacolon tóxico, investigar sinais de peritonite ou perfuração que podem exigir intervenção cirúrgica urgente e determinar a duração e o grau de distensão cólica5. Um dos dilemas clínicos num paciente com pseudo-obstrução intestinal é quando indicar procedimentos como a descompressão cirúrgica ou endoscópica do cólon.
Prognóstico
Em 1986, numa revisão de 400 casos, Vanek5 observou mortalidade de 14% nos casos tratados conservadoramente e 30% nos casos que receberam tratamento cirúrgico, sendo a causa de óbito diretamente relacionada com a patologia de base dos doentes, concluindo que a patologia de base é o principal determinante no prognóstico.
A complicação mais grave da pseudo-obstrução intestinal é a perfuração de ceco, com mortalidade de 40 a 50%, indicando-se a cecostomia quando o diâmetro cecal é maior que 12 cm ou a dilatação permanece por mais de três dias.
Tratamento
A terapia de suporte inclui: suspensão da dieta entérica, correção dos desequilíbrios hidroeletrolíticos e drenagem nasogástrica1. Em caso de dilatação do recto e sigmóide, um tubo rectal deve ser inserido e mantido para drenagem. Medicações que afectem a motilidade cólica como opiáceos, anti-colinérgicos e antagonistas dos canais de cálcio devem ser descontinuados, se possível. A deambulação e movimentação dos doentes são encorajadas, para tentar estimular a motilidade e promover o esvaziamento cólico8. O exame físico seriado agregado à radiografia de abdomen diária ajudam a monitorizar ar a evolução da doença.
O risco de perfuração cólica é maior com diâmetro do cego > 12cm e quando a distensão estiver presente por mais de seis dias10. Os doentes com esta apresentação e aqueles que não melhoram após 24-48 horas de terapia de suporte poderiam ser candidatos a intervenções.
Descompressão Farmacológica
Na ausência de sintomas de perfuração ou peritonite, a terapia medicamentosa com neostigmina (parassimpaticomimético indireto) deve ser considerada como escolha inicial. O suporte ao uso de neostigmina está no desequilíbrio na regulação autonómica da função cólica que ocorre na pseudo-obstrução intestinal.
Um estudo randomisado, duplamente cego, controlado com placebo11 avaliou o uso de neostigmina em doentes com pseudo-obstrução intestinal com diâmetro cecal maior que 10 cm e sem resposta ao tratamento conservador em 24h. Resposta clinica foi observada em 10 de 11 doentes randomisados para receber neostigmina e a média de tempo para resposta terapêutica foi de 4 minutos. A redução média do diâmetro cecal (de cinco para dois cm) foi significativa no grupo que usou neosigmina. Oito doentes não responderam à terapia inicial sendo permitido o uso de neostigmina e todos tiveram descompressão prontamente. Dos 18 que receberam neostigmina, 17 tiveram resposta clínica com recorrência em 11% dos casos.
Descompressão Endoscópica
Indicada quando o tratamento conservador e o farmacológico falharem. Uma revisão12 avaliou os doentes com pseudo-obstrução intestinal tratados com colonoscopia. Dos 292 doentes estudados, 69% tiveram sucesso na descompressão inicial, determinada pela redução do diâmetro cecal na radiografia, sendo que, 40% dos doentes tratados sem o tubo descompressor tiveram ao menos uma recorrência, necessitando de colonoscopia adicional. Para aumentar o beneficio terapêutico, a descompressão com tubo é fortemente recomendada. O índice de complicações é de 1 a 5%.
Cecostomia Percutânea
Esta técnica deve ser individualizada principalmente em doentes que não responderam ao tratamento conservador, farmacológico e colonoscópico13.
Descompressão Cirúrgica
A descompressão cirúrgica, que inclui cecostomia, colostomia ou ressecção é associada a um mau prognóstico, possivelmente devido à sua aplicação ocorrer somente em doentes com a forma mais severa da doença, que tenham falhado a resposta aos demais tratamentos ou quando há suspeita de perfuração cólica ou peritonite1.
Após o diagnóstico da síndrome foi instituído tratamento com descompressão endoscópica e a paciente faleceu por complicações da doença de base, confirmando que o prognóstico está relacionado diretamente à doença de base, a qual geralmente é grave nos doentes com síndrome de Ogilvie.
Referências
1. Saunders MD. Acute colonic pseudo-obstruction. Best Pract Res Clin Gastroenterol 2007;21:671-87. [ Links ]
2. Ogilvie WH. Large-intestine colic due to sympathetic deprivation. Br Med J 1948;2:671-673.
3. De Giorgio R, Barbara G, Stanghellini V, et al.. The pharmacologic treatment of acute colonic pseudo-obstruction. Aliment Pharmacol Ther 2001;15:1717-1727.
4. Delgado-Aros S, Camilleri M. Pseudo-obstruction in the critically ill. Best Pract Res Clin Gastroenterol 2003;17:427-44.
5. Vanek VW, Al-Salti M. Acute pseudo-obstruction of the colon (Ogilvies syndrome). An analysis of 400 cases. Dis Colon Rectum. 1986;29:203-10.
6. Grassi R, Cappabianca S, Porto A, et al. Ogilvies syndrome (acute colonic pseudo-obstruction): review of the literature and report of 6 additional cases. Radiol Med 2005;109:370-375.
7. Sheikh RA, Yasmeen S, Pauly MP, et al.. Pseudomembranous colitis without diarrhea presenting clinically as acute intestinal pseudo-obstruction. J Gastroenterol 2001;36:629-632.
8. Eisen GM, Baron TH, Dominitiz JA, et al.. Acute colonic pseudo-obstruction. Gastrointest Endosc 2002;56:789-792.
9. Frager D, Rovno HD, Baer JW, et al.. Prospective evaluation of colonic obstruction with computed tomography. Abdominal Imaging 1998;23:141-146.
10. Sloyer AF, Panella VS, Demas BE, et al.. Ogilvies syndrome. Successful management without colonoscopy Dig Dis Sci 1988;33:1391-1396.
11. Johnson CD, Rice RP. The radiographic evaluation of gross cecal distention. Am J Radiol 1985;145:1211-1217.
12. Ponec RJ, Saunders MD, Kimmey MB. Neostigmine for the treatment of acute colonic pseudoobstruction. N Engl J Med 1999;341:137-141.
13. Rex DK. Colonoscopy and acute colonic pseudo-obstruction. Gastrointest Endosc Clin N Am 1997;7:499–508.
14. Van der Spoel J, Oudemans-van Straaten H, Stoutenbecek C, et al.. Neostigmine resolves critical illness-related colonic ileus in intensive care patients with multiple organ failure – a prospective, double- blind, placebo-controlled trial. Intensive Care Med 2001;27:822-827.
Correspondência: Viviane Weiller Dallagasperina; Avenida: Aspirante Jenner, número 987; Bairro: Lucas Araújo; Passo Fundo/Rio Grande do Sul/ Brasil; 99074-360; E-mail: vividallagasperina@hotmail.com
Recebido para publicação: 11/09/2008 e Aceite para publicação: 15/04/2009.













